(2013?聊城一模)研究CO
2与CH
4反应使之转化为CO和H
2,对减缓燃料危机、减小温室效应具有重要的意义.
(1)已知:2CO(g)+O
2(g)=2CO
2(g)△H=-566kJ?mol
-12H
2(g)+O
2(g)=2H
2O(g)△H=-484kJ?mol
-1CH
4(g)+2O
2(g)=CO
2(g)+2H
2O(g)△H=-890kJ?mol
-1则:CH
4(g)+CO
2(g)=2CO(g)+2H
2(g)△H=
+160kJ?mol-1
+160kJ?mol-1
.
(2)在密闭容器中通入物质的量浓度均为0.1mol/L的CH
4 与CO
2,在一定条件下发生反应
CH
4(g)+CO
2(g)=2CO(g)+2H
2(g),测得CH
4的平衡转化率与温度及压强的关系如图1:
①下列事实能说明该反应一定达到平衡的是
ac
ac
.
a.CO
2的浓度不再发生变化
b.υ
正(CH
4)=2υ
逆(CO)
c.混合气体的平均相对分子质量不发生变化
d.CO与H
2的物质的量比为1:1
②据图可知,P
1、P
2、P
3、P
4由大到小的顺序为
P4>P3>P2>P1
P4>P3>P2>P1
.
③在压强为P
4、1100℃的条件下,该反应5min时达到平衡X点,则用CO表示该反应的速率为
0.032mol/(L?min)
0.032mol/(L?min)
,该温度下,反应的平衡常数为
1.64
1.64
.
(3)用CO与H
2可合成甲醇(CH
3OH),以甲醇和氧气反应制成的燃料电池如图2所示,该电池工作过程中O
2应从
c
c
(填“c或b”)口通入,电池负极反应式为
2CH3OH+2H2O-12e-=2CO2↑+12H+
2CH3OH+2H2O-12e-=2CO2↑+12H+
,若用该电池电解精炼铜,每得到6.4g铜,转移电子数目为
0.2NA
0.2NA
.



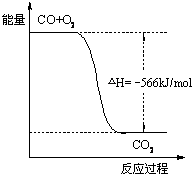 已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol,Na2O2(s)+CO2(g)=Na2CO3(s)+
已知:2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol,Na2O2(s)+CO2(g)=Na2CO3(s)+