
题目列表(包括答案和解析)
把7.4 g Na2CO3·10H2O和NaHCO3组成的混合物溶于水,配成100 mL溶液,其中c(Na+)=0.6 mol/L,若把等质量的混合物加热到恒重时,残留物的质量为 ( )
A.3.18 g B.2.12 g C.5.28 g D.4.22 g
某研究性学习小组设想将少量Cl2通入Fe2+和I-的混合溶液,来探究Fe2+和I-的还原性强弱.
[提出假设]
假设1:________;
假设2:________;
假设3:Fe2+和I-的还原性一样强.
[验证假设]
(1)利用以下装置进行试验,

实验必须的装置是:A→________(按氯气流向的顺序用序号书写)
(2)实验开始后,控制通入少量氯气,通过观察溶液颜色的变化,________(能或不能)判断反应的先后顺序.
(3)请在下表中填写实验步骤及预期现象与结论.

(4)该实验成功的关键是控制各反应物的用量.该小组称量1
.52 g FeSO4(M=152 g/mol)和1.66 g KI(M=166 g/mol)固体溶于水中,为了验证上述假设,通入的氯气的体积最多不能超过________.(标准状况)(5)有同学质疑,上述实验只能验证氯气分别与Fe2+和I-反应的速率的大小.并不能证明Fe2+和I-的还原性强弱.于是提出另一验证方案:往KI溶液中滴加________溶液,如果能发生反应,就可证明二者的还原性强弱,该反应的离子方程式是________.
我国在青藏高原发现了名为“可燃冰”的环保型新能源。
(1)“可燃冰”属于化石燃料,主要成分是CH4。另外还有两种化石燃料,它们的名称分别是 和 。
(2)CH4可与Cl2反应,反应历程如下
①Cl—Cl→2Cl· ΔH= 243 kJ·mol-1
②Cl·+CH3—H→·CH3+H—Cl ΔH= 4 kJ·mol-1
③·CH3+Cl—Cl→CH3——Cl+Cl· ΔH= -106 kJ·mol-1
则CH4与Cl2反应生成CH3—Cl(g)的热化学方程式为 。
(3)CH4可用于设计燃料电池,甲烷燃料电池的工作原理如下图所示:
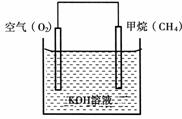
则通入CH4的一极为原电池的 (填“正极”或“负极”),正极的电极反应式为 。
(4)CH4与H2O在隔绝空气、高温和催化剂条件下反应:
CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=m kJ·mol-1
则反应的平衡常数表达式K= , K的大小与温度(T)的关系如右图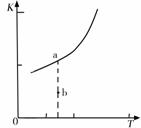 中曲线所示,则m 0(填“>”“=”或“<”);改变某一条件,使状态从a点到达b点,若保持温度不变,反应再次达到平衡时,则CH4的转化率 (填“增大”、“减小”、“不变”或“不确定”),反应的焓变(△H)将 (填“增大”、“减小”或“不变”)。
中曲线所示,则m 0(填“>”“=”或“<”);改变某一条件,使状态从a点到达b点,若保持温度不变,反应再次达到平衡时,则CH4的转化率 (填“增大”、“减小”、“不变”或“不确定”),反应的焓变(△H)将 (填“增大”、“减小”或“不变”)。
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H1=" +" 49.0 kJ·mol -1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) △H2=-192.9 kJ·mol -1
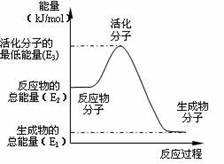
下列说法正确的是
|
钢铁“发蓝”是将钢铁制品浸到某些氧化性的溶液中,在钢铁的表面形成一层四氧化三铁的技术过程.其中一种办法是将钢铁制品浸到亚硝酸钠和浓氢氧化钠的混合溶液中加热到130℃反应.其过程可以用如下化学方程式表示: ①3Fe+NaNO2+5NaOH=3Na2FeO2+H2O+NH3↑ ②6Na2FeO2+NaNO2+5H2O=3Na2Fe2O4+NH3↑+7NaOH ③Na2FeO2+Na2Fe2O4+2H2O=Fe3O4+4NaOH 下列说法不正确的是 | |
A. |
反应①②③均是氧化还原反应 |
B. |
该生产过程不产生任何污染 |
C. |
整个反应过程中,每有16.8 g Fe参加反应转移0.8 mol电子 |
D. |
反应②中的氧化剂是NaNO2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com