
题目列表(包括答案和解析)
某学生两次分别用2.6 g锌与硝酸溶液进行反应,两次所用的硝酸溶液中均含有6.3 g的HNO3,但浓度不同,均恰好完全反应。又已知第一次实验中有1/5的HNO3被还原,第二次实验中只有1/10的HNO3被还原。试写出相应的反应方程式___________________________
_______________________________________________________________________________。
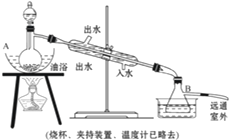 乙酸乙酯是无色具有水果香味的液体,沸点77.2℃,某同学制取它用冰醋酸14.3mL,95%的乙醇 23mL,还用到浓硫酸、饱和碳酸钠以及极易与乙醇结合成六水合物的氯化钙溶液.主要仪器如图所示.
乙酸乙酯是无色具有水果香味的液体,沸点77.2℃,某同学制取它用冰醋酸14.3mL,95%的乙醇 23mL,还用到浓硫酸、饱和碳酸钠以及极易与乙醇结合成六水合物的氯化钙溶液.主要仪器如图所示.乙酸乙酯是无色具有水果香味的液体,沸点77.2℃,某同学制取它用冰醋酸14.3 mL,95%的乙醇23 mL,还用到浓硫酸、饱和碳酸钠以及极易与乙醇结合成六水合物的氯化钙溶液.主要仪器如图所示.

实验步骤是:
①先向A中蒸馏烧瓶注入少量乙醇和浓硫酸后摇匀,再将剩下的所有乙醇和冰醋酸注入分液漏斗里待用.这时分液漏斗里两种有机物的物质的量之比约为5∶7.
②加热油浴保温约135℃~145℃.
③将分液漏斗中的液体缓缓滴入蒸馏烧瓶里,调节加料速度使蒸出酯的速度与进料速度大体相等,直到加料完全.
④保持油浴温度一段时间,至不再有液体流出后,停止加热.
⑤取下B中的锥形瓶,将一定量饱和Na2CO3溶液分批、少量、多次地加到馏出液里,边加边摇荡,至无气泡产生为止.
⑥将⑤的液体混合物分液,弃去水层.
⑦将饱和CaCl2溶液(适量)加入到分液漏斗中,摇荡一段时间后静置,放出水层(废液).
⑧分液漏斗里得到的是初步提纯的乙酸乙酯粗品.
试回答:
(1)实验中浓硫酸的主要作用是________.
(2)用过量乙醇的主要目的是________.
(3)用饱和Na2CO3溶液洗涤粗酯的目的是________.如果用NaOH浓溶液代替Na2CO3溶液将引起的后果是________.
(4)用饱和CaCl2溶液洗涤粗酯的目的是________.
(5)为什么操作③要使加料与馏出的速度大致相等?
________.
(6)在⑧所示的粗酯里还含有的杂质是________.

| 高温 |
| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试 管中滴入几滴KSCN溶液. |
|
| 第二步 | 若溶液紫色褪去,则说明含有Fe2+; 若无明显变化,则说明不含Fe2+. |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com