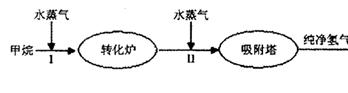
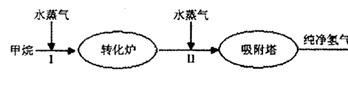
(9分)美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如
下图:
(1)此流程的第II步反应为:CO(g)+H
2O(g)

H
2(g)+CO
2(g),该反应的化学平衡常数表达式为K=
;反应的平衡常数随温度的变化如表一,
温度/℃
| 400
| 500
| 830
| 1000
|
平衡常数K
| 10
| 9
| 1
| 0.6
|
从上表可以推断:此反应是_______________ (填“吸”、“放”)热反应。在830℃下,若开始时向恒容密闭容器中充入CO与H
zO均为1 mo1,则达到平衡后CO的转化率为_____。
(2)此流程的第II步反应CO(g)+H
2O(g)

H
2(g)+CO
2(g),在830℃,以表二的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有
(填实验编号);
实验编号
| N(CO)
| N(H2O)
| n(H2)
| N(CO2)
|
A
| 1
| 5
| 2
| 3
|
B
| 2
| 2
| 1
| 1
|
C
| 0.5
| 2
| 1
| 1
|
(3)在一个不传热的固定容积的容器中,判断此流程的第II步反应达到平衡的标志是
①体系的压强不再发生变化 ②混合气体的密度不变 ③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变 ⑤体系的温度不再发生变化 ⑥ v(CO
2正)= v(H
2O逆)
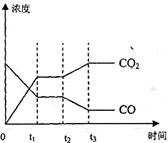
(4)图表示该反应此流程的第II步反应在时刻t
达到平衡、在时刻t
分别因改变某个条件而发生变化的情况:图中时刻t
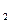
发生改变的条件是_________。(写出两种)
(5)若400℃时,第Ⅱ步反应生成l mol氢气的热量数值为 33.2(单位为kJ),第Ⅰ步反应的热化学方程式为: CH
4(g)+H
2O(g)=3H
2(g)+CO(g)△H="-103.3" kJ·mol
-1。则400℃时,甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式为
。

![]() 的分子、分母的第一项不含“-”号,则
的分子、分母的第一项不含“-”号,则![]() ________.
________.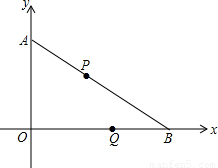
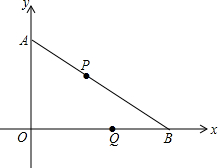 速度均为1厘米/秒,设移动的时间为t(0≤t≤4)秒.
速度均为1厘米/秒,设移动的时间为t(0≤t≤4)秒.
 H2(g)+CO2(g),该反应的化学平衡常数表达式为K= ;反应的平衡常数随温度的变化如表一,
H2(g)+CO2(g),该反应的化学平衡常数表达式为K= ;反应的平衡常数随温度的变化如表一, H2(g)+CO2(g),在830℃,以表二的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有 (填实验编号);
H2(g)+CO2(g),在830℃,以表二的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有 (填实验编号); 达到平衡、在时刻t
达到平衡、在时刻t 分别因改变某个条件而发生变化的情况:图中时刻t
分别因改变某个条件而发生变化的情况:图中时刻t 发生改变的条件是_________。(写出两种)
发生改变的条件是_________。(写出两种)
 H2(g)+CO2(g),该反应的化学平衡常数表达式为K= ;反应的平衡常数随温度的变化如表一,
H2(g)+CO2(g),该反应的化学平衡常数表达式为K= ;反应的平衡常数随温度的变化如表一, H2(g)+CO2(g),在830℃,以表二的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有 (填实验编号);
H2(g)+CO2(g),在830℃,以表二的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有 (填实验编号);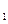 达到平衡、在时刻t
达到平衡、在时刻t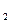 分别因改变某个条件而发生变化的情况:图中时刻t
分别因改变某个条件而发生变化的情况:图中时刻t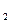 发生改变的条件是_________。(写出两种)
发生改变的条件是_________。(写出两种)