
题目列表(包括答案和解析)

(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是________ (填标号)。
A.碳酸氢钠难溶于水?
B.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出?
C.碳酸氢钠受热易分解?
(2)某探究活动小组根据工业制取碳酸钠的原理,进行碳酸氢钠的制备实验, 同学们按各自设计的方案实验。?
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。?
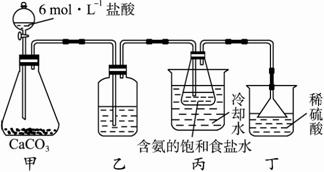
i.乙装置中的试剂是_______________(填标号)。?
A.烧碱溶液?
B.澄清石灰水?
C.浓氨水?
D.蒸馏水?
ii.丁装置的作用是_________________________。?
iii.实验结束后,分离出NaHCO3晶体的操作是_________________(填名称)。
②另一位同学用下图中戊装置(其他装置未画出)进行实验。
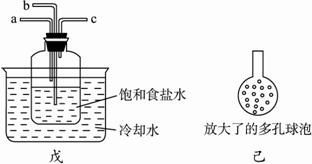
i.实验时,须先从a管通入_________气体,再从b管通入____________气体。?
ii.有同学建议在b管下端连接上图中己装置,理由是__________________________。?
(3)请你再写出一种实验室制取少量碳酸氢钠的方法。____________________________。
碳酸钠与工农业生产、日常生活紧密相关。工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题:
方案一:沉淀分析法
(1)把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀________(填操作)、洗涤、烘干、称量。洗涤沉淀的操作是 ______________________________ 。
方案二:气体分析法
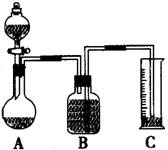
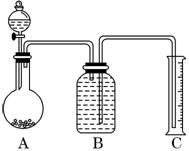
(2)把一定量的样品与足量盐酸反应后,用下图装置测定产生CO2气体的体积,为了测量结果准确,B中的溶液最好采用___________________,但选用该溶液后实验结果仍然不够准确,其原因是_______________________。
方案三:质量差分析法
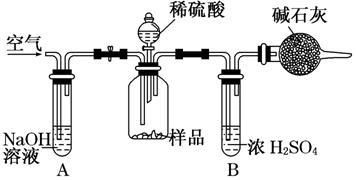
(3)把一定质量的样品和足量的稀硫酸反应,采用下图所示装置,通过称量反应前后盛有碱石灰的干燥管质量,利用其质量差求算样品的纯度。
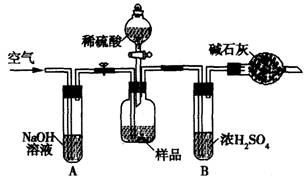
该实验的操作步骤有:①在干燥管内填满碱石灰,质量为mg ②取ng样品装入广口瓶中
③检验装置的气密性 ④缓慢鼓人空气数分钟,再称量干燥管质量为Mg ⑤关闭止水夹
⑥打开止水夹 ⑦缓慢加入稀硫酸至不再产生气体为止 ⑧缓慢鼓人空气数分钟
Ⅰ.正确的操作顺序是(填写序号):③→_________→⑥→______⑤→________⑦→______
Ⅱ.在操作④中,要缓慢鼓人空气数分钟,鼓人空气的作用是_________ ;装置A的作用是 _________;装置B的作用是 _____________。
Ⅲ.若去掉装置A,测定结果______________ ;若去掉装置B,测定结果_________ (填“偏大”、“偏小”或“无影响”)。
(9分)碳酸钠与工农业生产、日常生活紧密相关.工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案.请回答下列有关问题:
方案一:沉淀分析法
(1)把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀________(填操作)、洗
涤、烘干、称量.洗涤沉淀的操作是______________________________________
________________________________________________________________________.
方案二:气体分析法
(2)把一定量的样品与足量盐酸反应后,用如图装置测定产生CO2气体的体积,为了测
定结果准确,B中的溶液最好采用________,但选用该溶液后实验结果仍然不够准确,
其原因是_______________________________________________________.
方案三:质量差分析法
(3)把一定质量的样品和足量的稀硫酸反应,采用如图所示装置,通过称量反应前后盛有碱石灰的干燥管质量,利用其质量差求算样品的纯度.
该实验的操作步骤有:①在干燥管内填满碱石灰,质量为m g ②取n g样品装入广口
瓶中 ③检验装置的气密性
④缓慢鼓入空气数分钟,再称量干燥管质量为w g ⑤关闭止水夹 ⑥打开止水夹 ⑦
缓慢加入稀硫酸至不再产生气体为止 ⑧缓慢鼓入空气数分钟
Ⅰ.正确的操作顺序是(填写序号):
③→________→⑥→________→⑤→________→⑦→________→④
Ⅱ.若去掉装置A,测定结果________;若去掉装置B,测定结果________(填“偏大”、
“偏小”或“无影响”).
(9分)碳酸钠与工农业生产、日常生活紧密相关.工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案.请回答下列有关问题:
方案一:沉淀分析法
(1)把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀________(填操作)、洗
涤、烘干、称量.洗涤沉淀的操作是______________________________________
________________________________________________________________________.
方案二:气体分析法
(2)把一定量的样品与足量盐酸反应后,用如图装置测定产生CO2气体的体积,为了测
定结果准确,B中的溶液最好采用________,但选用该溶液后实验结果仍然不够准确,
其原因是_______________________________________________________.
方案三:质量差分析法
(3)把一定质量的样品和足量的稀硫酸反应,采用如图所示装置,通过称量反应前后盛有碱石灰的干燥管质量,利用其质量差求算样品的纯度.
该实验的操作步骤有:①在干燥管内填满碱石灰,质量为m g ②取n g样品装入广口
瓶中 ③检验装置的气密性
④缓慢鼓入空气数分钟,再称量干燥管质量为w g ⑤关闭止水夹 ⑥打开止水夹 ⑦
缓慢加入稀硫酸至不再产生气体为止 ⑧缓慢鼓入空气数分钟
Ⅰ.正确的操作顺序是(填写序号):
③→________→⑥→________→⑤→________→⑦→________→④
Ⅱ.若去掉装置A,测定结果________;若去掉装置B,测定结果________(填“偏大”、
“偏小”或“无影响”).


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com