
题目列表(包括答案和解析)
下图为某市售盐酸试剂瓶标签上的部分数据。问:
| 盐 酸 分子式:HCl 相对分子质量:36.5 外观合格 密度约:1.18 g/cm3 HCl的质量分数:36.5% 符合GB622~89 试剂生产许可证编号: |
(1)该盐酸的物质的量浓度为多少?(列式计算)
(2)取该盐酸25.5 mL与2.00 mol/L的氢氧化钠溶液100 mL混合,再将混合后溶液稀释至1.00 L,此时溶液的pH约为多少?
(5分)下图为某市售盐酸试剂瓶标签上的部分数据。问:

(1)该盐酸的物质的量浓度为多少?
(2)取该盐酸25.4 mL与2.00 mol·L-1的氢氧化钠
溶液100 mL混合,再将混合液稀释到1.00 L,
此时溶液的pH约为多少?
盐 酸 分子式:HCl 相对分子质量:36.5 外观合格 密度约: HCl的质量分数:36.5% 符合GB622-89 试剂生产许可证编号: |
(1)该盐酸的物质的量浓度为多少?(列式计算)
(2)取该盐酸25.4 mL与2.00 mol·L-1的氢氧化钠溶液100 mL混合,再将混合后溶液稀释至
(5分)下图为某市售盐酸试剂瓶标签上的部分数据。问:
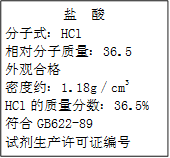
(1)该盐酸的物质的量浓度为多少?
(2)取该盐酸25.4 mL与2.00 mol·L-1的氢氧化钠
溶液100 mL混合,再将混合液稀释到1.00 L,
此时溶液的pH约为多少?
(5分)下图为某市售盐酸试剂瓶标签上的部分数据。问:
(1)该盐酸的物质的量浓度为多少?
(2)取该盐酸25.4 mL与2.00 mol·L-1的氢氧化钠
溶液100 mL混合,再将混合液稀释到1.00 L,
此时溶液的pH约为多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com