
题目列表(包括答案和解析)
下列说法中错误的是( )
A.根据对角线规则,铍和铝的性质具有相似性
B.P4和CH4都是正四面体分子且键角都为109o28ˊ
C.元素电负性越大的原子,吸引电子的能力越强
D.在H3O+和NH4+ 中都存在配位键
【解析】P4的键角是60°的,B不正确。所以答案选B。
氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如下图所示。常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体。下列说法错误的是 ( )
A.S2Cl2的结构式为Cl-S-S-Cl
B.S2Cl2为含有极性键和非极性键的非极性分子
C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2
D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
【解析】根据氯化二硫的结构示意图可判断,硫和硫之间形成的是非极性键,硫和氯之间形成的是极性键,但氯化二硫不是直线型结构,因此属于极性分子,形成的晶体是分子晶体,所以A正确,B不正确。S2Br2与S2Cl2结构相似,所以S2Br2也是分子晶体,但S2Br2的相对分子质量比S2Cl2的大,因此C正确。能使品红褪色的气体是二氧化硫,而在S2Cl2中硫的化合价是+1价,所以S2Cl2和水的反应是氧化还原反应。由于二氧化硫是氧化产物,所以还应该有还原产物单质硫生成,孤选项D也正确。答案是B。
氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如下图所示。常温下S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体。下列说法错误的是 ( )
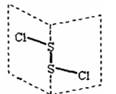
A.S2Cl2的结构式为Cl-S-S-Cl
B.S2Cl2为含有极性键和非极性键的非极性分子
C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2
D.S2Cl2与H2O反应的化学方程式可能为: 2S2Cl2+2H2O=SO2↑+3S↓+4HCl
【解析】根据氯化二硫的结构示意图可判断,硫和硫之间形成的是非极性键,硫和氯之间形成的是极性键,但氯化二硫不是直线型结构,因此属于极性分子,形成的晶体是分子晶体,所以A正确,B不正确。S2Br2与S2Cl2结构相似,所以S2Br2也是分子晶体,但S2Br2的相对分子质量比S2Cl2的大,因此C正确。能使品红褪色的气体是二氧化硫,而在S2Cl2中硫的化合价是+1价,所以S2Cl2和水的反应是氧化还原反应。由于二氧化硫是氧化产物,所以还应该有还原产物单质硫生成,孤选项D也正确。答案是B。
已知反应:mX(g)+ nY(g) qZ(g) △H<0,m+n>q,在恒容的密闭容器中反应达到平衡时,下列说法正确的是( )
A、通入稀有气体,压强增大,平衡正向移动
B、X的正反应速率是Y的逆反应速率的m/n倍
C、降低温度,混合气体的平均相对分子质量变小
D、增加X的物质的量,Y的转化率降低
【解析】考查外界条件对平衡的影响。该反应是体积减小的放热的可逆反应,若降低温度,则平衡向正反应方向移动,所以混合气体的平均相对分子质量变大,C不正确。通入稀有气体,压强增大,但物质的浓度没有变化,平衡不移动,A不正确。增加X的物质的量,可以增大其他物质的转化率,D也不正确。平衡时正逆反应速率相等,所以根据反应速率之比是相应的化学计量数之比可判断,B是正确的。答案选B。
已知反应:mX(g)
+ nY(g)  qZ(g) △H<0,m+n>q,在恒容的密闭容器中反应达到平衡时,下列说法正确的是
( )
qZ(g) △H<0,m+n>q,在恒容的密闭容器中反应达到平衡时,下列说法正确的是
( )
A、通入稀有气体,压强增大,平衡正向移动
B、X的正反应速率是Y的逆反应速率的m/n倍
C、降低温度,混合气体的平均相对分子质量变小
D、增加X的物质的量,Y的转化率降低
【解析】考查外界条件对平衡的影响。该反应是体积减小的放热的可逆反应,若降低温度,则平衡向正反应方向移动,所以混合气体的平均相对分子质量变大,C不正确。通入稀有气体,压强增大,但物质的浓度没有变化,平衡不移动,A不正确。增加X的物质的量,可以增大其他物质的转化率,D也不正确。平衡时正逆反应速率相等,所以根据反应速率之比是相应的化学计量数之比可判断,B是正确的。答案选B。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com