
题目列表(包括答案和解析)
 )中形成的,电池总反应方程式为:8Li+3SOCl2
)中形成的,电池总反应方程式为:8Li+3SOCl2A.若电解质溶液中混入水,对电池反应无影响?
B.金属锂作电池的正极,石墨作电池的负极?
C.电池工作过程中,亚硫酰氯(SOCl2)被还原为S?
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4∶1?
A.电解质溶液中混入碱溶液,对电池反应无影响
B.电池的正极为:Li-e-![]() Li+
Li+
C.电池工作过程中,亚硫酰氯(SOCl2)仅被还原为Li2SO3
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4∶1
A.电解质溶液中混入水,对电池反应无影响
B.金属锂作电池的正极,石墨作电池的负极
C.电池工作过程中,SOCl2被还原为Li2SO3
D.电池工作过程中,金属锂提供的电子与正极区析出的S的物质的量之比为4∶1
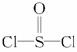 )中而形成的,电池总反应方程式为8Li+3SOCl2====6LiCl+Li2SO3+2S,下列叙述中正确的是( )
)中而形成的,电池总反应方程式为8Li+3SOCl2====6LiCl+Li2SO3+2S,下列叙述中正确的是( )A.电解质溶液中混入水,对电池反应无影响
B.金属锂作电池的正极,石墨作电池的负极
C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4∶1
溶解在亚硫酰氯(![]() )中形成的,电池总反应方程式为:8Li+3SOCl2====6LiCl+
)中形成的,电池总反应方程式为:8Li+3SOCl2====6LiCl+
Li2SO3+2S,下列叙述中正确的是( )
A.电解质溶液中混入碱溶液,对电池反应无影响
B.电池的正极为:Li-e-====Li+
C.电池工作过程中,亚硫酰氯(SOCl2)仅被还原为Li2SO3
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4:1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com