
题目列表(包括答案和解析)

请回答:
(1)装置A中发生反应的化学方程式为_______________。
(2)装置D中试管中放置的棉花中应浸一种液体,这种液体是__________,其作用是__________。
(3)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是__________。B中应放置的液体是__________(填选项序号)。
a.水 b.酸性KMnO4溶液
c.浓溴水 d.饱和NaHSO3溶液
(4)实验中,他们取
①有一定量的余酸但未能与铜片完全反应,你认为原因是__________。
②下列药品中能够用来证明反应结束后的烧瓶中确有余酸的是__________(填选项序号)。
a.Fe粉 b.BaCl2溶液 c.Ag粉 d.NaHCO3溶液
(5)为定量测定余酸的物质的量浓度,某同学进行了如下设计:先测定铜与浓硫酸反应产生SO2的量,再计算余酸的物质的量浓度。而测定SO2的量的方法有多种,你认为下列实验方案中可行的是________(填选项序号)。
a.将装置A产生的气体缓缓通过预先称量过盛有碱石灰的干燥管,结束反应后再次称量
b.将装置A产生的气体缓缓通入足量的用硫酸酸化的KMnO4溶液,再加入BaCl2溶液,过滤、洗涤、干燥、称量沉淀
c.用排水法测定装置A产生气体的体积(已折算成标准状况)
d.用排饱和NaHSO3溶液的方法测出装置A产生气体的体积(已折算成标准状况)
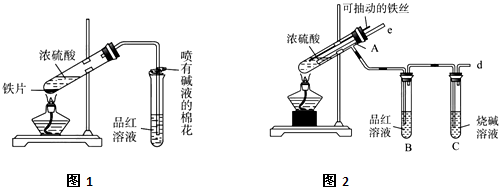
Ⅰ.(1)某兴趣小组甲设计了以下装置和方法测定空气中SO2含量。你认为可行的操作是 (填序号)
|
序号 |
A |
B |
C |
|
装置 |
|
|
|
|
原理 |
通入V升空气,测定生成沉淀的质量 |
当KMnO4溶液刚好褪色时,测定通入空气的体积V |
通入V升空气,测定U型管增加的质量 |
(2)兴趣小组乙取336mL(标准状况)某由SO2和N2组成的混合气体Y,将其通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g。由此推知气体Y中SO2的体积分数为 。
Ⅱ某化学兴趣小组丙为探究Fe3+是否能氧化SO2,设计了如下实验装置。
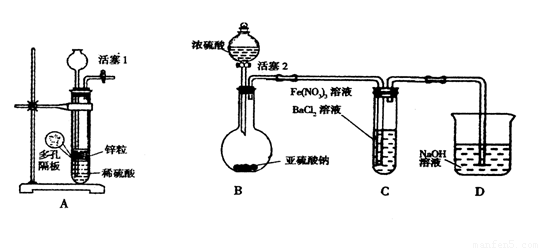
(1)如上图连接好装置。实验前应进行 操作
(2)观察到装置C中产生了白色沉淀,同学们提出了以下猜想(每个猜想只考虑一种物质的氧化性)。
猜想1: ;
猜想2:SO2被Fe3+氧化了;
猜想3:SO2被NO3—氧化了
(3)甲同学认为猜想1正确,并利用上述装置A进行了排除干扰的探究实验。
(4)乙同学认为猜想2正确,则装置C中反应的离子方程式是
(5)丙同学认为猜想3正确,他利用甲同学的实验装置,设计实验验证猜想。请在答题卡上写出实验步骤以及预期现象和结论。限选实验试剂:NaNO3溶液、KSCN溶液、FeCl3溶液、BaCl2溶液、
|
实验步骤 |
预期现象和结论 |
|
|
|
Fe(NO3)3溶液
Ⅰ.(1)某兴趣小组甲设计了以下装置和方法测定空气中SO2含量。你认为可行的操作是 (填序号)
| 序号 | A | B | C |
| 装置 |  |  |  |
| 原理 | 通入V升空气,测定生成沉淀的质量 | 当KMnO4溶液刚好褪色时,测定通入空气的体积V | 通入V升空气,测定U型管增加的质量 |

| 实验步骤 | 预期现象和结论 |
| | |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com