
题目列表(包括答案和解析)
编号 | Ⅰ | Ⅱ | Ⅲ |
实验 |
|
|
|
图1-1-5
(1)实验Ⅰ的目的是______________________。
(2)实验Ⅱ证明了___________离子之间发生了化学反应,根据什么现象证明溶液中的另两种离子没有发生化学反应。__________________________________________________。
(3)实验Ⅲ中反应的离子方程式为____________________________________________。
为了确认电解质溶液中部分离子相互间能否发生反应,做了如下三组实验:

(1)实验Ⅰ的目的是________.
(2)实验Ⅱ证明了________离子和________离子发生了化学反应,根据什么现象证明溶液中的另两种离子没有发生化学反应________.
(3)实验Ⅲ中反应的离子方程式为________.
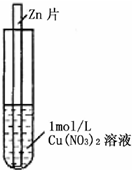 (2011?上饶二模)如图,将一锌片放入1mol?L-1蓝色Cu(NO3)2溶液中,观察到下列实验现象:①反应初期锌片上有大量气泡冒出,同时液面的上一层Cu(NO3)2溶液开始呈现绿色,并且逐渐向液面下的深处扩散,试管底部有红色固体出现.②与锌片接触的溶液温度明显升高,反应越来越剧烈,并在红色固体上方开始出现一层蓝色沉淀,并逐渐增多.③反应后期溶液逐渐变为无色,试管底部又有部分白色沉淀物.
(2011?上饶二模)如图,将一锌片放入1mol?L-1蓝色Cu(NO3)2溶液中,观察到下列实验现象:①反应初期锌片上有大量气泡冒出,同时液面的上一层Cu(NO3)2溶液开始呈现绿色,并且逐渐向液面下的深处扩散,试管底部有红色固体出现.②与锌片接触的溶液温度明显升高,反应越来越剧烈,并在红色固体上方开始出现一层蓝色沉淀,并逐渐增多.③反应后期溶液逐渐变为无色,试管底部又有部分白色沉淀物.现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、A13+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过比较分析,认为无须检验就可判断五种物质中肯定有的两种物质是_____________和__________。
(2)物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体。则X为__________(填字母)。
A.Br- B.SO42- C.CH3COO- D.HCO3-
(3)将19.2g Cu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式__________,若要将Cu完全溶解,至少应加入H2SO4的物质的量是_____ __。
(4)若用惰性电极电解C和D的混合溶液,若溶质的物质的量均为0.1 mol,通电后,当在阴极产生气体1.12L时,阳极产生的气体体积为___________L。(气体体积均为标准状况,且不考虑气体在水中的溶解)
(5)将E溶液蒸干后并将所得固体灼烧,最终得到的固体成分是(填化学式)__________。
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子K+、Fe3+、Cu2+、Ba2+、A13+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过比较分析,认为无须检验就可判断五种物质中肯定有的两种物质是_____________和__________。
(2)物质C中含有离子X。为了确定X,现将(1)中的两种物质记为A和B,当C与A的溶液混合时产生蓝色沉淀,向该沉淀中滴入足量稀HNO3,沉淀部分溶解,剩余白色固体。则X为__________(填字母)。
A.Br- B.SO42- C.CH3COO- D.HCO3-
(3)将19.2g Cu投入装有足量D溶液的试管中,Cu不溶解,再滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现,写出Cu溶解的离子方程式__________,若要将Cu完全溶解,至少应加入H2SO4的物质的量是_____ __。
(4)若用惰性电极电解C和D的混合溶液,若溶质的物质的量均为0.1 mol,通电后,当在阴极产生气体1.12L时,阳极产生的气体体积为___________L。(气体体积均为标准状况,且不考虑气体在水中的溶解)
(5)将E溶液蒸干后并将所得固体灼烧,最终得到的固体成分是(填化学式)__________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com