
题目列表(包括答案和解析)
 (2010?湘潭三模)“神七”登天标志着我国的航天事业进入了新的篇章.请你解答有关问题:
(2010?湘潭三模)“神七”登天标志着我国的航天事业进入了新的篇章.请你解答有关问题: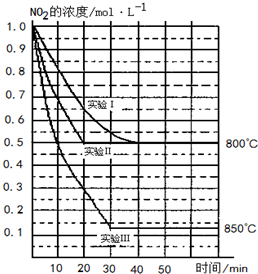 某条件下,在2L密闭容器中发生如下反应2NO2(g)?2NO(g)+O2(g)
某条件下,在2L密闭容器中发生如下反应2NO2(g)?2NO(g)+O2(g)| c(NO)2×c(O2) |
| c(NO2)2 |
| c(NO)2×c(O2) |
| c(NO2)2 |
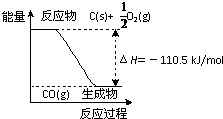 反应2C+O2=2CO 的能量变化如图所示.下列说法正确的是( )
反应2C+O2=2CO 的能量变化如图所示.下列说法正确的是( )| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com