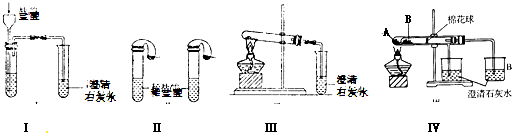
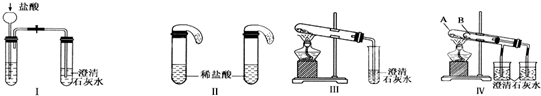
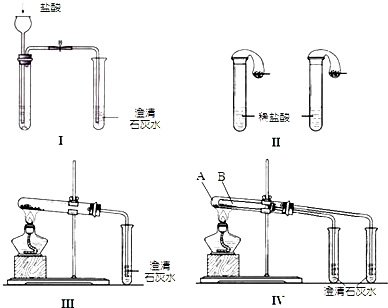
某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验.如图I~Ⅳ所示.

(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的是(填装置序号)
Ⅱ
Ⅱ
;
(2)①图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为
;
②与实验Ⅲ相比,实验Ⅳ的优点是(填选项序号)
D
D
;
A.Ⅳ比Ⅲ复杂 B.Ⅳ比Ⅲ安全 C.Ⅳ比Ⅲ操作简便
D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是(填化学式)
NaHCO3
NaHCO3
.
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应.当碳酸氢钠与氢氧化钙的物质的量之比为2:1时,所得溶液中溶质的化学式为
Na2CO3
Na2CO3
,请设计实验检验所得溶液中溶质的阴离子
取上层清液于洁净的试管中加入适量CaCl2溶液,振荡,若有白色沉淀生成,则证明溶液中含有CO32-
取上层清液于洁净的试管中加入适量CaCl2溶液,振荡,若有白色沉淀生成,则证明溶液中含有CO32-
.
(5)请设计一个可鉴别碳酸钠和碳酸氢钠实验(写出实验原理).

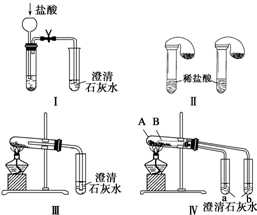 某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示.
某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示.