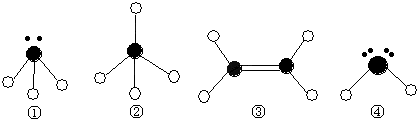
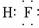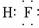有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,其中B是地壳中含量最多的元素.已知A、C及B、D分别是同主族元素,且B、D两元素原子核内质子数之和是A、C两元素原子核内质子数之和的2倍;在处于同周期的C、D、E三元素中,E的原子半径最小;通常条件下,五种元素的单质中有三种气体,两种固体.
(1)B、C两元素按原子个数1:1组成的化合物F中的阴阳离子比为
1:2
1:2
,F中既存在离子键又存在
非极性
非极性
共价键(填“极性”或“非极性”).
(2)试比较D、E两元素的最高价氧化物对应水化物的酸性强弱(填写化学式):
HClO4
HClO4
>
H2SO4
H2SO4
.
(3)将E单质通入A、B、C三种元素组成的化合物的水溶液中,写出反应的离子方程式:
Cl2+2OH-═Cl-+ClO-+H2O
Cl2+2OH-═Cl-+ClO-+H2O
.
(4)写出两种均含A、B、C、D四种元素的化合物在溶液中相互反应,且生成气体的化学方程式:
NaHSO4+NaHSO3═Na2SO4+H2O+SO2↑
NaHSO4+NaHSO3═Na2SO4+H2O+SO2↑
.
(5)D的氢化物分子中,D原子的杂化方式是
sp3
sp3
,空间构型是
V形
V形
.







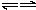 A+E(3)D+E→B+C
A+E(3)D+E→B+C