根据以下事实,回答下列问题
(1)工业接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO
2(g)+O
2(g)?2SO
3(g)△H=-190kJ?mol
-1该热化学反应方程式的意义是
在450℃时,2molSO2气体和1molO2气体完全反应生成2molSO3气体时放出的热量为190kJ,
在450℃时,2molSO2气体和1molO2气体完全反应生成2molSO3气体时放出的热量为190kJ,
.
(2)在25℃、101kPa下,1g甲醇[CH
3OH(l)]燃烧生成CO
2和液态水时放热.22.68kJ.则表示甲醇燃烧热的热化学方程式为
CH
3OH(l)+
O
2(g)═CO
2(g)+2H
2O(l)△H=-725.8 kJ?mol
-1CH
3OH(l)+
O
2(g)═CO
2(g)+2H
2O(l)△H=-725.8 kJ?mol
-1.
(3)已知25℃、l01kPa时下列反应的热化学方程式为:
①CH
3COOH(l)+2O
2(g)=2CO
2(g)+2H
2O(l)△H=-870.3kJ/mol
②C(s)+O
2(g)=CO
2(g)△H=-393.5kJ/mol
③H
2(g)+
O
2(g)=H
2O(l)△H=-285.8kJ/mol,则C(s)与H
2(g)、O
2(g)反应生成CH
3COOH(l)在该条件下的热化学方程式为
2C(s)+2H2(g)+O2(g)=CH3COOH(l)△H=-488.3kJ/mol
2C(s)+2H2(g)+O2(g)=CH3COOH(l)△H=-488.3kJ/mol
.
(4)由N
2和H
2合成1molNH
3时可放出46.2kJ的热量.从手册上查出N≡N键的键能是948.9kJ/mol,H-H键的键能是436.0kJ/mol,则N-H键的键能是
391.6kJ/mol
391.6kJ/mol
.

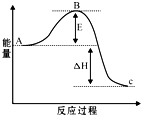 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行: 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行: