
题目列表(包括答案和解析)
铜在自然界存在于多种矿石中,如黄铜矿(CuFeS2)、辉铜矿(Cu2S)、孔雀石(CuCO3·Cu(OH)2)等。
(1)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,由黄铜矿冶炼铜的反应为:8 CuFeS2+21O2=8Cu+4FeO+2Fe2O3+16 SO2。
① 在反应产物中加入过量的盐酸溶解,其溶液中含有的阳离子为 。
② 上述冶炼过程产生大量的SO2。某实验小组欲探究二氧化硫的化学性质,设计如下实验,请完成实验报告。
| 序号 | 二氧化硫的性质 | 主要操作和现象 | 化学方程式 | |||||
| Ⅰ | 将二氧化硫通入装有品红溶液的试管中,品红由红色变为无色 | |||||||
| Ⅱ | 氧化性[来源:学科网] | |||||||
| Ⅲ | 将二氧化硫通入装有新制氯水的试管中,氯水由浅黄绿色色变为无色 | |||||||
| ||||||||
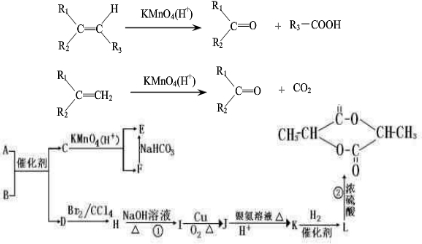
(2)孔雀石在一定条件F能发生分解反应,其产物有如下转化关系。E为相对分子质量为44且能和新制的氢氧化铜在加热下反应的化合物。

① D跟G反应的化学方程式为: :
② B和F反应的化学方程式为: 。
铜在自然界存在于多种矿石中,如黄铜矿(CuFeS2)、辉铜矿(Cu2S)、孔雀石(CuCO3·Cu(OH)2)等。
(1)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,由黄铜矿冶炼铜的反应为:8 CuFeS2+21O2=8Cu+4FeO+2Fe2O3+16 SO2
① 在反应产物中加入过量的盐酸溶解,其溶液中含有的阳离子为 。
② 上述冶炼过程产生大量的SO2。某实验小组欲探究二氧化硫的化学性质,设计如下实验,请完成实验报告
|
序号 |
|
二氧化硫的性质 |
|
主要操作和现象 |
化学方程式 |
|||
|
Ⅰ |
|
|
|
将二氧化硫通入装有品红溶液的试管中,品红由红色变为无色 |
|
|||
|
Ⅱ |
|
氧化性 |
|
|
|
|||
|
Ⅲ |
|
|
|
将二氧化硫通入装有新制氯水的试管中,氯水由浅黄绿色色变为无色 |
|
|||
|
|
|
|
|
|
||||
(2)孔雀石在一定条件F能发生分解反应,其产物有如下转化关系。E为相对分子质量为44且能和新制的氢氧化铜在加热下反应的化合物

① D跟G反应的化学方程式为: :
② B和F反应的化学方程式为: .
铜在自然界存在于多种矿石中,如黄铜矿(CuFeS2)、辉铜矿(Cu2S)、孔雀石(CuCO3·Cu(OH)2)等。
(1)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,由黄铜矿冶炼铜的反应为:8 CuFeS2+21O2=8Cu+4FeO+2Fe2O3+16SO2
① 在反应产物中加入过量的盐酸溶解,其溶液中含有的阳离子为 。
② 上述冶炼过程产生大量的SO2。某实验小组欲探究二氧化硫的化学性质,设计如下实验,请完成实验报告
| 序号 |
| 二氧化硫的性质 |
| 主要操作和现象 | 化学方程式 | |||
| Ⅰ |
|
|
| 将二氧化硫通入装有品红溶液的试管中,品红由红色变为无色 |
| |||
| Ⅱ |
| 氧化性 |
|
|
| |||
| Ⅲ |
|
|
| 将二氧化硫通入装有新制氯水的试管中,氯水由浅黄绿色色变为无色 |
| |||
|
|
|
|
|
| ||||
(2)孔雀石在一定条件F能发生分解反应,其产物有如下转化关系。E为相对分子质量为44且能和新制的氢氧化铜在加热下反应的化合物

① D跟G反应的化学方程式为: :
② B和F反应的化学方程式为: .


| 一定条件 |
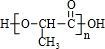 +(n-1)H2O
+(n-1)H2O| 一定条件 |
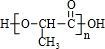 +(n-1)H2O
+(n-1)H2O

| 25 |
| 2 |
| 25 |
| 2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com