
题目列表(包括答案和解析)
某黑色物质可能是CuO、C中的一种或两种,小宇.小林同学为研究该黑色物质,设计如下方案(若有C存在,含量较少):
【研究成分】小宇.小林同学分别设计的两个实验方案如下:小宇:黑色粉末
加稀盐酸 —— 观察溶液颜色
小林:黑色粉末(通入氢气,并加热)产物与白色硫酸铜接触
试回答:
(1)小宇方案中证明有氧化铜的实验现象是________ _________ 。
(2)小林方案中仅有氧化铜的实验现象是____________________ 。
(3)以上两个方案中,你认为哪个方案更好,理由是什么?
_______________________________________________________________________ (4)小新同学也设计了一个方案:直接将黑色粉末放在空气中加热,请你帮小新判断一下是否可以 (填行或不行),理由
(1)溶液由无色变为蓝色
(2)黑色粉末全部变为红色粉末
(3)小宇的方案 安全。节能
(4)不行,因为没有明显的现象
30、(17分)6月5日是世界环境日,2005年世界环境日主题为“营造绿色城市,呵护地球家园”,开发海洋,维持海洋的可持续发展是每个地球公民的神圣职责。请回答下面关于海洋的几个问题:
【问题一】近年,我国沿海经常发生大面积的“赤潮”,造成养殖业重大损失。赤潮的发生主要是与因为藻类的疯狂生长,与藻类疯长的密切相关的元素是 和 。(填元素符号)
【问题二】海水中资源丰富,含量最多的金属阳离子是 (填符号),含量最多的分子是 (填符号)。
【问题三】盐场海水晒盐的原理是 。
A、氯化钠的溶解度受温度影响较大
B、因氯化钠溶解度受温度影响不大,故采取蒸发水分的方法
 |
(1)操作①的名称是 ,操作②的名称是 。
(2)A溶液是 ,B溶液是 。(选择合适序号填空)
a、NaOH 和Na2CO3 b、KOH和 K2CO3 c、H2SO4 d、HCl
【问题四】经勘察,深海下含有丰富的“可燃冰”,可满足人类1000年的能源需要。该物质是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳1个CH4分子或1个游离H2O分子。若晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为 。
A、CH4?14H2O B、 CH4?8H2O
C、 CH4?(23/3)H2O D、 CH4?6H2O
|
【问题五】海水淡化是国际上研究的热点问题,我国科学家在利用高分子膜进行海水淡化的研究上取得了一些成绩。如图,左侧为海水,右侧为经过一段时间后由左侧经高分子膜渗透得到的淡水,该变化是
变化(填物理或化学)。

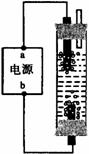
【问题六】如图为某学生制作的一种家用环保型消毒液发生器:原理是电解饱和氯化钠溶液,制得的消毒液有较强的杀菌能力,该反应是利用氯化钠和水在电解条件下生成NaOH、H2和Cl2,请完成化学方程式。
。
请你帮该同学写出实验室用铁和稀硫酸制取氢气的化学方程式
该反应属于基本反应类型中的
反应。
某校化学研究性学习小组探究气体制取的实验原理与方法。
(1)甲同学将课本的基础知识进行整理如下图,请你帮助他完成相关内容。

制取气体 | 所需药品 | 装置连接顺序 | 反应的化学方程式 |
氧气 | 氯酸钾和二氧化锰 | ||
二氧化碳(干燥) | 大理石和稀盐酸 |
(2)乙同学设计的实验装置(如右图),既可用于制取
气体,又可用于验证物质性质。当打开K1、关闭
K2时,利用I、Ⅱ装置可直接进行的实验是
(填序号)。
①大理石与稀盐酸反应制取二氧化碳
②锌与稀硫酸反应制取氢气
(3)丙同学认为在不改变I、Ⅱ、Ⅲ装置的仪器及
位置的前提下,该装置可用于过氧化钠 (Na2O2)与水反应制取氧气,另一产物为氢氧化钠,则该反应的化学方程式为: ;她的改进措施是 。
(4)丁同学打开K2、关闭K1,利用I、Ⅲ装置来验证生成的二氧化碳中含有水蒸气,此时C中盛放的物质是 ,可以观察到的现象是 .
(5)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应)作如下回收处理:
①通过以下四步实验操作回收二氧化锰。正确操作的先后顺序是 (填写选项序号)。
a.烘干 b.溶解 c.过滤 d.洗涤
②用所得氯化钾晶体配制50 g质量分数为5%的氯化钾溶液,需要氯化钾的质量为 。
③过滤、蒸发时都需用到的仪器是 (填序号)。
A.酒精灯 B.烧杯 C.玻璃棒 D.漏斗 E.量筒
(6)小明用6.5 g可能含有铜、铝、铁、镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2 g氢气,则此锌粉中一定含有的金属杂质是 .

某校化学研究性学习小组探究气体制取的实验原理与方法。
(1)甲同学将课本的基础知识进行整理如下图,请你帮助他完成相关内容。

|
制取气体 |
所需药品 |
装置连接顺序 |
反应的化学方程式 |
|
氧气 |
氯酸钾和二氧化锰 |
||
|
二氧化碳(干燥) |
大理石和稀盐酸 |
(2)乙同学设计的实验装置(如右图),既可用于制取
气体,又可用于验证物质性质。当打开K1、关闭
K2时,利用I、Ⅱ装置可直接进行的实验是 (填序号)。
①大理石与稀盐酸反应制取二氧化碳
②锌与稀硫酸反应制取氢气
(3)丙同学认为在不改变I、Ⅱ、Ⅲ装置的仪器及位置的前提下,该装置可用于过氧化钠 (Na2O2)与水反应制取氧气,另一产物为氢氧化钠,则该反应的化学方程式为: ;她的改进措施是 。
(4)丁同学打开K2、关闭K1,利用I、Ⅲ装置来验证生成的二氧化碳中含有水蒸气,此时C中盛放的物质是 ,可以观察到的现象是 .
(5)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应)作如下回收处理:
①通过以下四步实验操作回收二氧化锰。正确操作的先后顺序是 (填写选项序号)。
a.烘干 b.溶解 c.过滤 d.洗涤
②用所得氯化钾晶体配制50 g质量分数为5%的氯化钾溶液,需要氯化钾的质量为 。
③过滤、蒸发时都需用到的仪器是 (填序号)。
A.酒精灯 B.烧杯 C.玻璃棒 D.漏斗 E.量筒
(6)小明用6.5 g可能含有铜、铝、铁、镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2 g氢气,则此锌粉中一定含有的金属杂质是 .
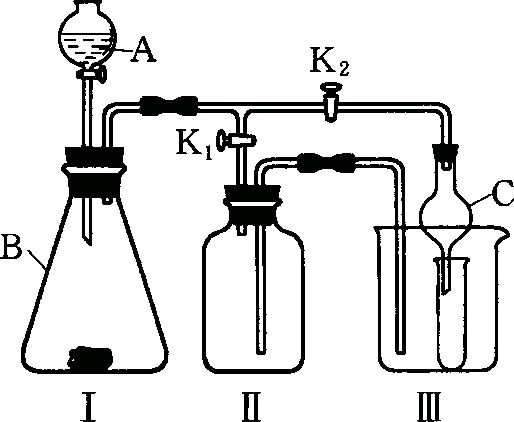
科学探究是一种重要的学习方式。锁定探究目的,理清探究思路是探究过程中分析问题时常用的方法。请利用图30中的装置对相关问题展开探究。

【实验目的】①探究二氧化碳的制备和性质。②探究酸碱盐的性质。
【实验信息】①大理石中的![]() 杂质不参加反应且难溶于水。
杂质不参加反应且难溶于水。
②B装置中铜网用粗铜丝固定,铜网和粗铜丝不参加反应。
③探究过程不考虑空气中的二氧化碳对实验的影响。
【实验步骤】
①连接仪器,检查装置气密性。将块状大理石置于B装置的铜网上。
②关闭止水夹![]() K2,打开止水夹K1,打开分液漏斗活塞,向B装置中装入稀盐酸,使其浸没大理石后关闭分液漏斗活塞。
K2,打开止水夹K1,打开分液漏斗活塞,向B装置中装入稀盐酸,使其浸没大理石后关闭分液漏斗活塞。
(1)B装置中发生反应的化学方程式为 ① ,该反应属于基本反应类型中的 ② 。
(2)A装置中的实验现象是 ① ,发生反应的化学方程式为 ② 。21世纪教育网
③当B装置中的物质仍在反应时,关闭止水夹K1,打开止水夹K2。一段时间后观察到:B装置中反应逐渐停止,C、D装置中溶液为红色,且D装置中有沉淀生成。
(3)D装置中发生反应的化学方程式为 。
【实验拓展】反应结束后对C、D装置中的溶液进![]() 行以下探究。(提示:溶质不考虑酚酞)
行以下探究。(提示:溶质不考虑酚酞)
![]() (4)C装置溶液中一定含的离子有
(4)C装置溶液中一定含的离子有
(5)D装置溶液中一定含有溶质NaCl,原因有 。
(6)D装置溶液中溶质组成的可能有 。
(7)如需完全除去D装置溶液中除NaCl以外的其它溶质,你选择的物质是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com