
题目列表(包括答案和解析)
| 项 目 | 铁 | 铝 | 铜 |
| 密度(g∕cm3) | 7.86 | 2.70 | 8.92 |
| 熔点(℃) | 1535 | 660 | 1083 |
| 硬度(最硬的金刚石为10) | 4-5 | 2.5-3 | 2-2.9 |
| 实验一 | 实验二 | 实验三 | |
实验 方案 |
 |
 |
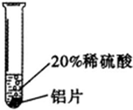 |
| 实验 现象 |
铬片表面产生气泡缓慢,溶液变蓝色. | 无现象 无现象 |
铝片表面产生气泡较快. |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢. | 铜不与稀硫酸反应 | 铝能和稀硫酸发生反应,反应速率较快 铝能和稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中由强到弱的相对位置关系是 AlCrCu AlCrCu | |||
| 实验步骤 | 实验现象 | 实验结论 |
将铝片和铬片分别置于两只试管中,向其中分别加入相同的硫酸铜溶液 将铝片和铬片分别置于两只试管中,向其中分别加入相同的硫酸铜溶液 |
铝片表面很快出现紫红色的固体,铬片出现紫红色固体较慢 铝片表面很快出现紫红色的固体,铬片出现紫红色固体较慢 |
三种金属的金属活动性顺序 是Al、Cr、Cu 三种金属的金属活动性顺序 是Al、Cr、Cu |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com