
题目列表(包括答案和解析)
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| CaCl2 | NaCl | MgCl2 | AlCl3 |
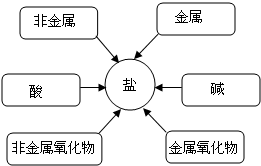
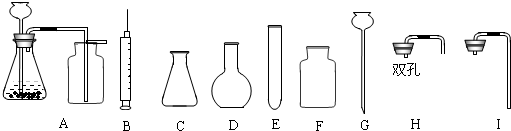
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| KCl | CaCl2 | NaCl | MgCl2 | A1C13 | ______ | ______ | ______ |
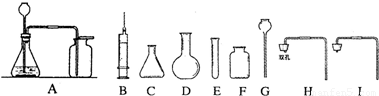
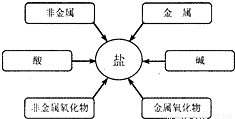
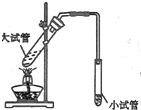 (2010?莱芜)淡水资源的缺乏已成为制约社会发展的重要因素,从浩瀚的海洋里获取淡水,对解决淡水危机具有重要意义.某小组针对这一现状,提出问题并在实验室进行了以下探究.
(2010?莱芜)淡水资源的缺乏已成为制约社会发展的重要因素,从浩瀚的海洋里获取淡水,对解决淡水危机具有重要意义.某小组针对这一现状,提出问题并在实验室进行了以下探究.| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1-2ml,滴入1-2ml滴无色酚酞试液,振荡 | 无色酚酞试液变 红 红 |
溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈 酸性或中性 酸性或中性 |
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1-2ml,滴入1-2ml滴无色酚酞试液,振荡 | 无色酚酞试液变______ | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈______ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com