
题目列表(包括答案和解析)
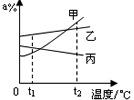
溶液的应用非常广泛。K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下: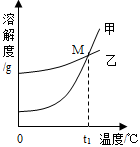
(1)硝酸钾溶液中的溶剂是_______________。
(2)图中能表示KNO3溶解度曲线的是__________(填“甲”或“乙”)。
(3)溶解度曲线上M点的含义是___________。
(4)现有200g溶质质量分数为10%的碳酸钾溶液,若使溶液的溶质质量分数增加一倍,应该蒸发掉 g水。
(5)40℃时,向两个分别盛有相同质量的硝酸钾和碳酸钾的烧杯中,各加入100g水,充分溶解后,恢复至40℃,其结果如右图所示。下列有关说法中,正确的是_________(填字母序号)。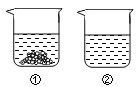
| A.烧杯②中溶液一定是不饱和溶液 |
| B.若使烧杯①中固体全部溶解,溶液中溶质质量分数一定增大 |
| C.将烧杯②中溶液降温至20℃时,溶液中溶质质量分数可能增大 |
| D.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数可能增大 |
(1)我们已学过的可用于分离或提纯物质的方法有:过滤、降温结晶、蒸发结晶等。为了达到下列实验目的,请将适当的方法填写在相应的横线上:
①工业上从海水中提取食盐 ________ ;
②硫酸铜溶液中加入氢氧化钠溶液后分离出氢氧化铜 。
(2)实验室要配制一定量8%的Na2SO4溶液,一学生已开出的实验用品为:硫酸钠固体、烧杯、等质量的纸、托盘天平(含砝码、镊子)、量筒、胶头滴管、药匙和试剂瓶(带标签)。还缺少的必要试剂是 ,仪器是 。
(6分)水和溶液在生产生活中有着重要的作用。
(1)水是一种最常见的溶剂。将少量下列物质分别加入水中,不能形成溶液的是 (填
字母序号)。
A.植物油 B.食盐 C.面粉 D.蔗糖
(2)电解水实验证明了水由 组成。
(3)生活中可以用 检验某水样是硬水还是软水。
(4)工业生产中常配制10%的稀盐酸来除铁锈,该反应的化学方程式为 。
(5)20℃时,将等质量的甲、乙固体,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2(不考虑水分蒸发),甲、乙固体溶解度曲线如图3。

下列说法正确的是 (填字母序号)。
图3中N表示的是甲的溶解度曲线
图2中的甲溶液是不饱和溶液
图2中甲、乙溶液的溶质质量分数相等
将图2中两溶液降温至30℃一定都不会析出晶体
图1中甲溶液溶质质量分数大于乙溶液溶质质量分数
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com