
题目列表(包括答案和解析)
 氢氧化钠俗名苛性钠,是一种重要的化工原料.下列研究从其结构、制备方法、性质以及变化规律等角度进行,请根据要求回答相应问题.
氢氧化钠俗名苛性钠,是一种重要的化工原料.下列研究从其结构、制备方法、性质以及变化规律等角度进行,请根据要求回答相应问题.| 实验步骤 | 实验现象 |
| ①取少量白色固体于试管中,加水振荡后,至全部溶解 | 无色溶液 |
| ②向试管的溶液中滴加适量物质X的溶液 | 现象A |
| ③再向试管中滴加几滴酚酞试液. | 现象B |
| 实验步骤 | 实验现象 |
| ①取少量白色固体于试管中,加水振荡后,至全部溶解 | 无色溶液 |
| ②向试管的溶液中滴加适量物质X的溶液 | 现象A |
| ③再向试管中滴加几滴酚酞试液. | 现象B |

| ||
| ||
氢氧化钠俗名苛性钠,是一种重要的化工原料.下列研究从其结构、制备方法、性质以及变化规律等角度进行,请根据要求回答相应问题。
Ⅰ.结构:
NaOH含有钠元素,钠在元素周期表中处于第三周期的 (填“开头”、“中间”或“结尾”)。
NaOH属于碱,碱在溶液中都可以电离出相同的离子,该离子是 (填离子符号)。
Ⅱ.制备:
实验室用纯碱制备烧碱的化学反应方程式为 。Ⅲ.性质及变化:
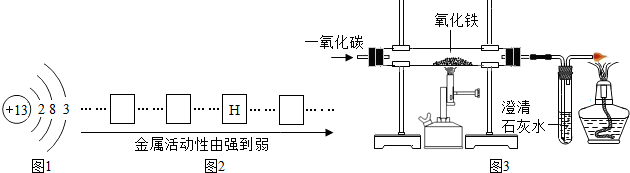
(1)氢氧化钠固体曝露在空气中容易 ,因此它与生石灰一起用作某些气体的干燥剂
(2)如右图所示,NaOH溶液可与稀酸反应的方程式为 。
该反应没有明显的现象,为了说明该反应确实能够发生,下列哪种物质肯定无法帮助你达到目的 。
a.镁条 b.酚酞 c.CuSO4 d.Ba(NO3)2
Ⅳ.保存:
张老师整理药品时,意外发现实验桌上有瓶敞口放置的NaOH固体,他让同学们对这瓶NaOH固体进行探究
【提出猜想】
猜想I:没有变质
猜想Ⅱ:部分变质为Na2CO3,依据是 (用方程式表示);猜想Ⅲ:全部变质
【实验设计、现象和推断】
| 实验步骤 | 实验现象 |
| ①取少量白色固体于试管中,加水振荡后,至全部溶解 | 无色溶液 |
| ②向试管的溶液中滴加适量物质X的溶液 | 现象A |
| ③再向试管中滴加几滴酚酞试液. | 现象B |

氢氧化钠俗名苛性钠,是一种重要的化工原料.下列研究从其结构、制备方法、性质以及变化规律等角度进行,请根据要求回答相应问题。
Ⅰ.结构:
NaOH含有钠元素,钠在元素周期表中处于第三周期的 (填“开头”、“中间”或“结尾”)。
NaOH属于碱,碱在溶液中都可以电离出相同的离子,该离子是 (填离子符号)。
Ⅱ.制备:
实验室用纯碱制备烧碱的化学反应方程式为 。Ⅲ.性质及变化:
(1)氢氧化钠固体曝露在空气中容易 ,因此它与生石灰一起用作某些气体的干燥剂
(2)如右图所示,NaOH溶液可与稀酸反应的方程式为 。
该反应没有明显的现象,为了说明该反应确实能够发生,下列哪种物质肯定无法帮助你达到目的 。
a.镁条 b.酚酞 c.CuSO4 d.Ba(NO3)2
Ⅳ.保存:
张老师整理药品时,意外发现实验桌上有瓶敞口放置的NaOH固体,他让同学们对这瓶NaOH固体进行探究
【提出猜想】
猜想I:没有变质
猜想Ⅱ:部分变质为Na2CO3,依据是 (用方程式表示);猜想Ⅲ:全部变质
【实验设计、现象和推断】
|
实验步骤 |
实验现象 |
|
①取少量白色固体于试管中,加水振荡后,至全部溶解 |
无色溶液 |
|
②向试管的溶液中滴加适量物质X的溶液 |
现象A |
|
③再向试管中滴加几滴酚酞试液. |
现象B |
(1)若现象A为有气泡产生,则加入的X溶液是 ,说明猜想 可排除。
(2)若X是Ca(OH)2溶液,现象A有白色沉淀,现象B为无色变红色,该实验 (填“能”或“不能”)说明猜想Ⅱ成立。
(3)若X是CaCl2溶液,则猜想Ⅱ成立的实验现象是 。
(4)定量研究:根据上述实验,可通过测定 ,
再通过计算得到氢氧化钠的变质情况。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com