
题目列表(包括答案和解析)
(1)50℃时熟石灰的溶解度________20℃时的溶解度。
(2)20℃时,100克水里溶解31.6克硝酸钾,则此时溶液中溶质的质量分数________31.6%。
(3)10%的食盐溶液100克,取出50克,剩下溶液溶质的质量分数________10%。
(4)50毫升酒精和50毫升水混合后体积_________________100毫升。
某校化学小组同学从家中带来淀粉、食盐、纯碱、泡打粉、去污粉和部分变质的熟石灰6种固体物质。老师从中取出任意3种并编号,让小组同学通过实验确认分别为哪种固体。
【查阅资料】
1.该去污粉主要成分为碳酸钠和碳酸钙
2.该泡打粉的主要成分是碳酸氢钠和有机酸
3.熟石灰变质的原因是 (用化学方程式表示)。
【实验准备】
为顺利完成任务,小组同学在老师指导下进行了如下预备实验。部分现象记录如下:
| | 实验1 取样,加足量水充分溶解 | 实验2 取样,加入适量稀盐酸 |
| 淀粉 | 白色浑浊,试管底部有不溶物 | 无明显现象 |
| 泡打粉 | 有气体产生,试管底部有白色不溶物 | 有气体产生 |
| | 实验1 取样,加足量水充分溶解 | 实验2 取样,加入适量稀盐酸 | 实验3 取实验1上层清液,加入3滴酚酞溶液 |
| 固体Ⅰ | 有气体产生,试管底部有白色不溶物 | 有气体产生 | |
| 固体Ⅱ | 固体溶解,形成无色溶液 | 有气体产生 | 溶液变红 |
| 固体Ⅲ | 有白色浑浊,试管底部有白色不溶物 | 有气体产生 | 溶液变红 |
某校化学小组同学从家中带来淀粉、食盐、纯碱、泡打粉、去污粉和部分变质的熟石灰6种固体物质。老师从中取出任意3种并编号,让小组同学通过实验确认分别为哪种固体。

【查阅资料】
1.该去污粉主要成分为碳酸钠和碳酸钙
2.该泡打粉的主要成分是碳酸氢钠和有机酸
3.熟石灰变质的原因是 (用化学方程式表示)。
【实验准备】
为顺利完成任务,小组同学在老师指导下进行了如下预备实验。部分现象记录如下:
| 实验1 取样,加足量水充分溶解 | 实验2 取样,加入适量稀盐酸 |
淀粉 | 白色浑浊,试管底部有不溶物 | 无明显现象 |
泡打粉 | 有气体产生,试管底部有白色不溶物 | 有气体产生 |
【实验过程】
小组同学对老师提供的三种固体进行实验探究。部分现象记录如下:
| 实验1 取样,加足量水充分溶解 | 实验2 取样,加入适量稀盐酸 | 实验3 取实验1上层清液,加入3滴酚酞溶液 |
固体Ⅰ | 有气体产生,试管底部有白色不溶物 | 有气体产生 |
|
固体Ⅱ | 固体溶解,形成无色溶液 | 有气体产生 | 溶液变红 |
固体Ⅲ | 有白色浑浊,试管底部有白色不溶物 | 有气体产生 | 溶液变红 |
【得出结论】
1.固体Ⅱ、Ⅲ加水形成的溶液pH 7 (填“>”、“<”或“=”);
2.分析以上实验现象得知,固体Ⅰ是 ,固体Ⅱ是 。
3.小组同学通过讨论认为固体Ⅲ不能确定。请你设计确认该固体的实验方案 。
【实验反思】
检验和鉴别也是实际生活中经常遇到的问题。面对多种物质的检验和鉴别,上述实验活动给我们的启示是 。
金属与人类生活密切相关。请分析回答下列问题:
(1)我国稀土储量居世界前列。下图是一种稀土元素铈(Ce)在元素周期表中的信息示意图,则铈原子的质子数是 ;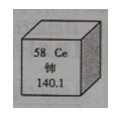
(2)将黄铜片和纯铜片相互刻画,发现纯铜片表面留下较深的划痕,则它们的硬度大小关系是:黄铜 纯铜(填“>”、“<”或“=”);
(3)工业炼铁的反应原理是:Fe203+3C0 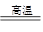 2Fe+3C02,该反应中体现了C0具有 性;
2Fe+3C02,该反应中体现了C0具有 性;
(4)铝制品具有很好的抗腐蚀性能,其原因是(用化学方程式表示) ;
(5)往AgN03溶液中加入一定量锌和铜的混合粉末,充分反应后,过滤,滤液为蓝色,则滤液中含有的金属离子是 (写出所有存在的可能组合)。
汽车、电动车一般使用铅酸蓄电池。某铅酸蓄电池使用的酸溶液是质量分数为20%的稀硫酸。请回答下列有关问题:
(1)若用100g质量分数为98%的浓硫酸(密度为1.84g/cm3)配制该稀硫酸时,需要蒸馏水(密度为1g/cm3)的体积为 mL(精确到0.1);
(2)该实验的主要步骤有计算、量取、稀释配制、装瓶并贴标签。
请填写下侧的标签;
(3)用量筒量取水时俯视读数,所配溶液溶质质量分数______ 20%(填“>”、“<”或“=”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com