
题目列表(包括答案和解析)

| 实验操作 | 实验现象 | 实验结论 |
| 4号溶液是部分变质的NaOH溶液. |
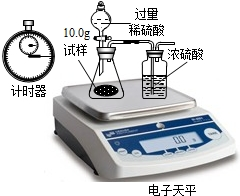
| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 试样 | 10.00 | |
| 装置+稀硫酸质量 | 241.30 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 248.20 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 248.00 |
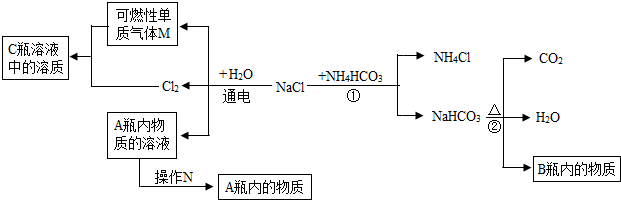
同学们运用对比的学习方法探究碱的性质。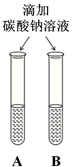
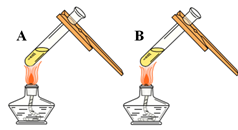
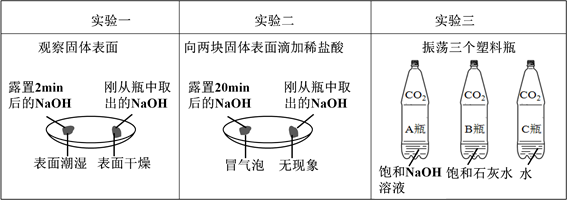
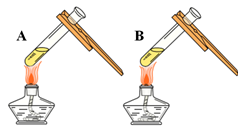
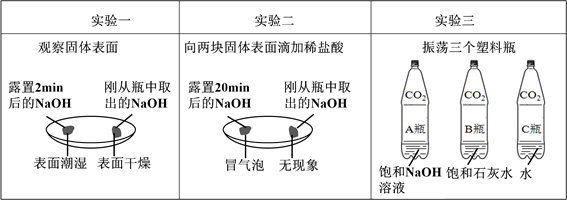
(1)由上图实验一、二可知,氢氧化钠会吸收空气的 ,因此要密封保存。
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C, A瓶内发生反应的化学方程式为 ,对比A瓶与 (选填“B”或“C”)瓶的实验现象可证明CO2能与NaOH发生反应。
(3)同学们设计如下两种方案鉴别氢氧化钠溶液与氢氧化钙溶液(分别编号为A、B)。
| 方案一 | 方案二 | 分析 |
| 微热(不考虑水分蒸发) | 两种方案中均观察到A试管内出现白色浑浊,A中试剂为 ; 方案二的设计原理是利用了 。 |
 2NaOH + H2↑ + Cl2↑,
2NaOH + H2↑ + Cl2↑,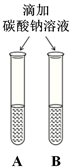
| 方案一 | 方案二 | 分析 |
| 微热(不考虑水分蒸发) | 两种方案中均观察到A试管内出现白色浑浊,A中试剂为 ; 方案二的设计原理是利用了 。 |
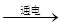 2NaOH + H2↑ + Cl2↑,
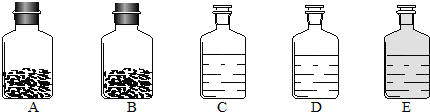
2NaOH + H2↑ + Cl2↑,化学兴趣小组同学发现实验台上按如下顺序摆放着7瓶不同的无色溶液(如图所示),其中4、5号试剂瓶标签破损.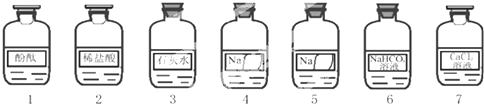
[提出问题]这两瓶试剂分别是什么?
[查阅资料]
①碱性的亚硫酸钠(Na2SO3)溶液、Na2CO3溶液都能与中性的CaCl2溶液发生复分解反应,产生白色沉淀.②Na2SO3+2HCl=2NaCl+SO2↑+H2O.
③CO2与SO2均可以使澄清石灰水变浑浊,SO2是一种有刺激性气味的气体.
[作出猜想]4、5号溶液可能分别是NaOH、Na2CO3、Na2SO3或NaCl溶液中的一种.
[实施方案]取少量4、5号溶液分别于试管中,然后分别进行下列三组实验.
实验1:在两支试管中分别滴入上述七种溶液中的______号溶液,两试管中的溶液均变成红色,说明4、5号溶液均不可能是上述猜想中的______溶液.实验2:在两支试管中分别滴入上述七种溶液中的3号溶液,两试管中均产生白色沉淀,4、5号溶液可能分别是Na2SO3溶液和Na2CO3溶液中的一种.写出其中一个反应的化学方程式______.
实验3:在两支试管中分别滴入上述七种溶液中的2号溶液,在盛4号溶液的试管中有______现象,说明4号是Na2CO3溶液;在盛5号溶液的试管中有______现象,说明5号是Na2SO3溶液.
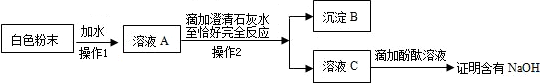
[实验反思]同学们经过分析,认为4号溶液还可能是变质的NaOH溶液.请你利用上述图中的试剂设计鉴定实验方案,完成实验报告.
| 实验操作 | 实验现象 | 实验结论 |
4号溶液是部分变质的NaOH溶液. |
25.某化学兴趣小组的同学参照教科书内容,在学校实验室里完成了以下两个实验:
实验一:配制溶质质量分数为6%的NaCl溶液50g,按如下步骤进行操作:
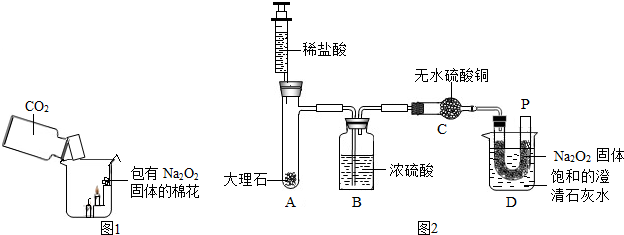
实验二:称取5.0g粗盐进行提纯.粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质.为了有效将粗盐提纯,实验的各步操作流程如图2所示: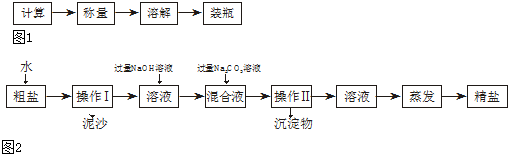
请你根据以上信息回答下述问题:
(1)配制50g溶质质量分数为6%的NaCl溶液,需NaCl______g,水______mL.
(2)NaCl溶解过程用到了玻璃棒,它的作用是______.
(3)粗盐提纯时,操作I的名称为______.
(4)某同学所得精盐比其他同学明显要少,原因可能是______.
A.溶解时将5.0g粗盐一次全部倒入水中,立即过滤
B.蒸发时有一些液体、固体溅出
C.提纯后所得精盐尚未完全干燥.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com