
题目列表(包括答案和解析)
2.在C+O2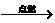 CO2中,参加反应的碳的质量和生成的CO2的质量关系是( )
CO2中,参加反应的碳的质量和生成的CO2的质量关系是( )
A.C的质量<CO2的质量 B.C的质量=CO2的质量
C.C的质量>CO2的质量 D.无法判断
1.在化学反应A+2B=C中,1.5克A与足量的B充分反应后生成9.5克C,参加反应的B的质量为( )
A.3克 B.9.5克 C.8克 D.4克
18、把氯化钠和氯化钙混合物的粉末20克,放到盛有96克水的烧杯中完全溶解后,再向其中加入100克浓度为10.6%的碳酸钠溶液,恰好完全反应。试求:
(1)原混合物中氯化钠的质量分数;(2分)
17、(8分)实验室里除了用氢气还原氧化铜之外还可以用氨气来还原氧化铜。某课外兴趣小组的同学欲设计一实验,在实验室制取氨气,用氨气来还原氧化铜,并通过测量相关物质的质量计算铜的近似相对原子质量。一同学查阅资料得知实验室可以用加热熟石灰与氯化铵固体的方法获得氨气,并且如将纯净的氨气通过红热的氧化铜,可得到氮气,同时生成铜和水。反应方程式如下: 2NH3+3CuO  N2+3Cu +3H2O
;另一同学查阅资料得知碱石灰成分为氢氧化钠与生石灰的固体混合物,他也发现氨气极易溶于水,生成的氨水是一种弱碱,并且氨气还可以与酸直接化合生成铵盐,如:NH3 +HCl === NH4Cl
N2+3Cu +3H2O
;另一同学查阅资料得知碱石灰成分为氢氧化钠与生石灰的固体混合物,他也发现氨气极易溶于水,生成的氨水是一种弱碱,并且氨气还可以与酸直接化合生成铵盐,如:NH3 +HCl === NH4Cl
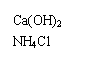
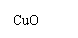
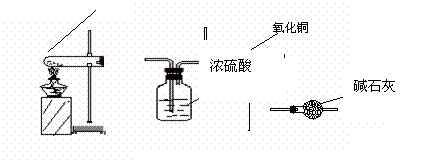
A B
A B C D
试回答:如果选用测定反应物CuO 和生成物H2O 的质量[m(CuO)、m(H2O)]
① 仪器连接的顺序(用字母编号表示,仪器可重复使用)_______________________ ;
② 写出生成氨气的化学方程式_______________________ ;
③ 实验完毕时观察到A中的主要现象是_______________________ ;
④ 列出计算Cu的相对原子质量的表达式(已知除铜以外各原子的相对原子质量)_______________________ ;如果实验中CuO 未完全还原成Cu 则测得的结果与CuO 完全还原成Cu 所得结果相比会________ (选填偏大、偏小、相同)。
⑤ 有位同学认为可利用上述装置可获得纯净的氮气,你认为仪器连接的顺序应有什么改动,新的顺序为(要求同第①小题)_______________________ 。
16、(3分)在化学研究课上,为了验证氨气(NH3)的某些性质,小李同学做了以下实验:下图中从左向右依次是他做的实验及相应现象。
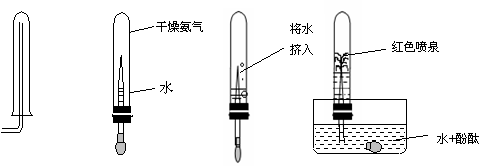
通过以上实验,小李得出了关于氨气的三点性质,你认为它们是:
__________________________________________________________________;
15、(7分)有四家化工厂排放的废水中溶质的主要成分如下表:
|
厂名 |
A厂 |
B厂 |
C厂 |
D厂 |
|
废水中溶质的主要成分 |
H2SO4 |
K2CO3 |
Ca(OH)2 |
CuCl2 |
为保护环境、防止污染,四厂决定联合处理废水,其处理方案如下:

(1)排气池中发生反应的化学方程式为:_________________________________________;
(2)沉淀池中出现的现象是________________,由此产生的废弃物是________________;
(3)若排气池中B厂废水过量,沉淀池中D厂废水过量,则混合时发生反应的化学方程式为:__________________________________________;
(4)若排气池中A厂废水过量,且沉淀池中______厂废水过量,会导致达标检测不合格。
14、(8分)年来出现的厄尔尼诺现象与大气中CO2含量的增多有关,请回答以下问题:
(1)空气中二氧化碳主要来源是 ________________;
(2)自然界中能消耗二氧化碳的是________ 作用,该反应用文字表述为:______________________________________________;
(3)为减缓此现象,你认为最理想的燃料是______;以水为原料,开发此燃料,你认为应研究的主要课题是_______________________。
(4) 汽车尾气(含有CO、SO2与NO等物质)是城市空气污染物,治理的方法之一是在汽车的排气管上装一个催化转换器,其特点是使CO和NO反应,生成可参与大气生态环境循环的无毒气体,写出CO和NO反应的化学方程式________________________ ;
控制城市汽车尾气对空气造成污染的方法是________ (填写序号):
①开发新能源; ②使用电动车; ③植树造林; ④戴呼吸面具。
13、(2分)我们已经学过碱性氧化物和酸性氧化物,到高中还要学习一类两性氧化物,如Al2O3 。当Al2O3 与酸、碱反应如下:
Al2O3 + 6HCl === 2AlCl3 + 3H2O Al2O3 + 2NaOH === 2NaAlO2 + H2O
你能否概括出两性氧化物的定义_____________________________________ 。
12、(3分)现有H2 、CO、CO2 三种气体,请从不同的角度指出其中任一气体与另外两种气体的不同之处。例如:CO2 无可燃性。
① ;② ;③ 。
11、(4分)根据对物质的存在或性质或用途的描述,写出该物质的化学式及物质的类别(单质、氧化物、酸、碱、盐、有机物)
|
物质的存在、性质、用途 |
化学式 |
物质类别 |
|
在自然界中以气、液、固三态存在,地球表面约70%被它覆盖 |
|
|
|
地壳中含量最多的金属元素 |
|
|
|
人体胃液中呈酸性的物质 |
|
|
|
在农业生产中,常用于改良土壤酸性的物质 |
|
|
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com