
题目列表(包括答案和解析)
9.等电子体具有原子数目相同、电子数目相同的特征。下列各组中的物质属于等电子体的是
A.NO和O2+ B.CO和N2 C.NO2和CO2 D.SO2和ClO2
8.两位美国科学家彼得·阿格雷和罗德里克·麦金农,因为发现细胞膜水通道,以及对离子通道结构和机理研究作出的开创性贡献而获得2003年诺贝尔化学奖。他们之所以获得诺贝尔化学奖而不生理学或医学奖是因为( )
A.他们的研究与化学物质水有关B.他们的研究有利于研制针对一些神经系统疾病和心血管疾病的药物C.他们的研究深入到分子、原子层次D.他们的研究深入到细胞层次
6.2003年10月16日6时23分,“神舟五号”载人飞船在内蒙古成功着陆,返回舱完好无损。飞船在返回大气层时由于同空气的剧烈摩擦,船体的表面温度将上升到2000℃――3000℃,因此飞船表面必须有良好的防高温措施。下列有关飞船防高温措施中不可取的是
A.使用陶瓷类的贴面覆盖船体B.使用在一定条件下能熔化或气化的表面覆盖材料
C.使用在一定条件下能与大气层中的氧气发生剧烈燃烧的覆盖材料
D.使用在一定条件下能发生分解反应的表面覆盖材料
3.在我们的日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品。这里的碘、铁、钙、硒、氟应理解为
A.元素 B.单质 C.分子 D.氧化物
2.目前我国许多城市和地区定期公布空气质量报告,在空气质量报告中,一般不涉及
A.二氧化硫 B.二氧化碳 C.氮氧化合物 D.可吸入颗粒
1.在盛放酒精的试剂瓶的标签上应印有下列警示标记中的
A. B.
B. C.
C. D.
D.
32.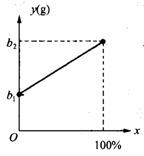 (7分)有一种金属样品,可能由镁和锌中的一种或两种组成。现取一定质量的该金属样品与足量稀硫酸反应,镁在金属样品中的质量分数(x)与反应生成氢气的质量(y)为右图所示的一次函数关系。根据图像回答下列问题:
(7分)有一种金属样品,可能由镁和锌中的一种或两种组成。现取一定质量的该金属样品与足量稀硫酸反应,镁在金属样品中的质量分数(x)与反应生成氢气的质量(y)为右图所示的一次函数关系。根据图像回答下列问题:
(1)若该金属样品由纯镁组成,生成的氧气为 g。
(2)若该金属样品由纯锌组成,生成的氧气为 g。
(3)若该金属样品由等质量的镁和锌组成,生成氢气的质量为 g 。(用带有b1、b2的代数式表示)
(4)现有一定质量的碳酸钙和碳酸钠组成的混合物与足量稀盐酸反应,其中碳酸钙在混合物中的质量分数(z)与反应生成二氧化碳的质量(y)仍为上图所示的一次函数关系。若碳酸钙和碳酸钠质量相等,则生成二氧化碳的质量为 g。(用带有b1、b2的代数式表示)
31.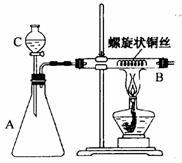 (7分)已知右图中,锥形瓶A中盛放的气体可能是CO2、CO、O2、H2中的一种;B管中放的是螺旋状的红色光亮铜丝;漏斗C中盛放某种液体,在实验时,液体不够时可以得到补充。问:
(7分)已知右图中,锥形瓶A中盛放的气体可能是CO2、CO、O2、H2中的一种;B管中放的是螺旋状的红色光亮铜丝;漏斗C中盛放某种液体,在实验时,液体不够时可以得到补充。问:
(1)先加热B管一段时间,发现铜丝表面略发黑。原因是 。
(2)打开漏斗C上的活塞,把其中的液体慢慢滴入A瓶中时,铜丝表面变得更黑。此时A中的气体和C中的液体所有可能的组合是: (可不填满)
①A中: C中: ;②A中: C中: 。
③A中: C中: ;④A中: C中: 。
(3)若A中盛放的是上述四种气体中的两种气体,当C中的液体滴入A中时,不管铜丝表面颜色如何变化,均有可能造成爆炸事故,则A中的气体和C中的液体所有可能的组合 是: (可不填满)
①A中: C中: ;②A中: C中:
③A中: C中: ;④A中: C中:
30.(7分)金坛盐矿是江苏省四大盐矿之一,其中氯化钠的储量在百亿吨以上。开采食盐的方法是先在地上钻孔至盐层,再把高压水打进盐层,便能得到饱和食盐水。
现有一座邻于水田与河流的采盐矿井,为了降低生产成本,企业用相邻河水作为生产用水向地下灌注,却发现得到的食盐水中多了一种对后继生产有害的杂质 铵盐。问:
(1)为什么使用河水会产生杂质铵盐?
(2)同学小钱想用学过的知识验证铵盐,他取用少量的盐水样品于试管中,再滴入足量的浓氢氧化钠溶液,加热后却没有闻到氨味。试分析原因。
(3)补充怎样的实验步骤,便能检出样品中的铵盐?
(4)开采过的矿井留下了硕大的封闭性好、能耐高压的穴腔。国家已将其作为“西气东输"工程的调峰储气库。到西气东输管道全面启用时,这个储气库的日储气量将达到6.7× 108 m3。从产生同样热量的角度分析,这个储气库相当于一天能储存 t原煤?
(已知:天然气的密度为0.6 6 kg/m3(25℃),天然气的热值为3.9×1 07 J/kg,原煤的热值为2.1×1 07 J/kg)
29.(7分)先在表中空白处填写相关的内容,再根据表中提供的信息研究下面的问题。
|
反应物I |
反应物Ⅱ |
反应现象 |
说 明 |
|
AgNO3溶液 |
NaCl溶液 |
生成白色沉淀 |
该沉淀为AgCl,不溶于稀H NO3 |
|
BaCl2溶液 |
Na2SO4溶液 |
生成白色沉淀 |
该沉淀为BaSO4,不溶于稀HCl |
|
Na2CO3溶液 |
|
生成白色沉淀 |
该沉淀为 ,溶于稀HCl |
由蒸发海水制得的食盐中,常含有Na2SO4、CaCl2等杂质,这些杂质对后继生产有害,需要除去。问:
(1)Na2SO4和CaCl2在溶液里能形成K+、SO42-、Ca2+和Cl-四种离子。要除去其中的Ca2+,可使用 溶液;除去其中的SO42-,可使用 溶液。
(2)在工业生产的除杂过程中,又会带进CO32-和OH-。要同时除去这两种杂质离子,最简便的方法是加入适量的 ,并用 测定溶液的酸碱性。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com