
题目列表(包括答案和解析)
2、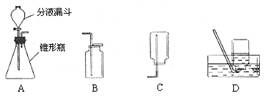 过氧化氢(化学式H2O2)溶液在MnO2作催化剂的条件下能迅速分解生成O2和H2O。分液漏斗可以通过调节活塞控制液体的滴加速度。
过氧化氢(化学式H2O2)溶液在MnO2作催化剂的条件下能迅速分解生成O2和H2O。分液漏斗可以通过调节活塞控制液体的滴加速度。
回答下列问题:(1)分液漏斗中应放入的物质是__________,锥形瓶中应放入的物质是___________。
(2)写出该方法制取O2的化学反应方程式________________;要收集一瓶纯净的O2,应选择装置___________(填字母)。
(3)某同学在观察到锥形瓶内有大量气泡时,开始用B装置收集O2,过一段时间后,用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃。其原因是___________。
(4)写出用该装置制取另外2种气体的化学式____________和___________。
(5)若实验时用此法代替KmnO4加热制取O2,优点是_____。①生成物只有氧气 ②不需加热 ③需加热
(6)装置A中反应很剧烈,据此提出实验安全注意事项是_____________(填编号)。
①控制液体的滴加速度 ②用体积较小的锥形瓶 ③加热反应物
1、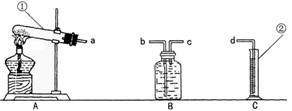 某校化学兴趣小组的同学利用下列装置进行实验。
某校化学兴趣小组的同学利用下列装置进行实验。
实验目的:(1)用高锰酸钾制取一瓶氧气,做细铁丝燃烧的实验。
(2)粗略测定加热2g高锰酸钾所收集到的氧气体积。
反应原理:(用化学方程式表示)
高锰酸钾制氧气: ;
细铁丝在氧气中燃烧: 。
仪器认识:写出仪器①②的名称:① ;② 。
装置连接:为达到实验目的(2),各装置的正确连接顺序是:(填接口的字母) a → ( ) ( ) → d
问题分析:(1)实验过程发现B瓶中的水变红了,原因是: ;
(2)用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作原因可能是: 。
(3)据化学方程式算出理论上2g高锰酸钾完全分解可生成氧气0.203g。而实际测得氧气在标准状况下的体积为177mL,换算成质量为0.253g,超过理论量为:0.253g一0.203g=0.05g。从理论上推测,你认为超过理论量的氧气可能来源于什么物质? 。(写出所有可能,空气、水因素忽略不计)
20.为了测定呼吸作用的气体产物,某学生设计了如下装置,假定装置中的气体能够按图中箭头所示方向稳定的运动,请回答下列问题:

(1)A瓶内NaOH溶液的作用是 ,B瓶内的澄清石灰水的作用是_______ 。D瓶内澄清石灰水的作用是 。
(2)如果将C瓶中的萌发的种子换成绿色植物,实验结果会怎样? ,原因是__
19.有一固体混合物,其中可能含有适量的炭粉、碳酸钙、氧化铜、氧化铁中的一种或几种,现进行下列实验:①取样,加热至高温,产生一种能使澄清石灰水变浑浊的气体;②把足量的稀盐酸滴入冷却后的固体残渣中,残渣部分溶解,同时产生一种可燃性气体。回答:
(1)混合物中一定含有 ;
(2)混合物中可能含有 ,为证明这一物质是否存在,应采取的方法是 。
18.在反应A+H2SO4=B¯+2HCl及A+2AgNO3=2C¯+Ba(NO3)2中,A、B、C各表示一种物质,这三种物质的化学式为:A ,B ,C 。
17.用化学方程式回答:
(1) 不能用铁桶装稀硫酸: 。
(2) 可用盐酸洗去试管壁上附着的不溶于水的氢氧化铜 。
(3) 用胃舒平[含Al(OH)3的药物]治疗胃酸(含HCl) 。
(4) 除去硝酸中的盐酸 。
(5) 除去炭粉中的氧化铜 。
16.某合作学习小组以“溶液的酸碱度及其用应”为题,开展研究性学习,请你做为该小组成员来解决以下问题:
(1)某同学说:“酸溶液呈酸性,碱溶液呈碱性,则盐溶液一定呈中性。”你认为这种推理 ____________(填“正确”或“不正确”)。
(2)从某工厂排除的废水中取出A、B两份水样,经测定,A水样的pH为4.8,B水样的pH为9.2,则A水样呈 性,B水样呈 性。已知某废水中含有少量硝酸银,为回收银单质,应加入适量的 。
(3)请你设计一个实验,能通过清晰可见的现象,验证氢氧化钠溶液和稀盐酸的反应,并能控制它们在恰好完全反应时停止实验。__________________________________________________
________________________________________________________________________________。
15.某溶液中含有Na+、H+、Cl- 、SO42-四种离子,若滴紫色石蕊试液,则显 色。欲证明两种阴离子确实存在,应先加适量的 溶液,使 完全沉淀过滤除去;再加入 溶液,以确定 离子的存在。原溶液中最多可以有 种溶质。
14.( )要制备CuCl2,可选用下列哪组物质相互作用
A. 铜和稀盐酸 B. 氧化铜和稀盐酸 C. 铜片和氯化银 D. 铜和氯化钠溶液
13.( )检验碳酸盐最简易的方法是
A. 加入氯化钡溶液,产生白色沉淀 B. 加入石灰水,产生无色气体
C. 加入稀盐酸产生了使石灰水变浑浊的气体 D. 放入水中,不溶解的是碳酸盐
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com