
题目列表(包括答案和解析)
4、过碳酸钠的化学式为Na2CO4,跟盐酸反应的化学方程式是: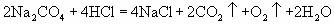
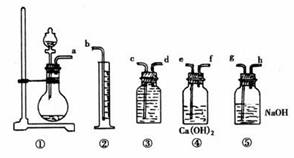 在商品中一般都含有Na2CO3,为了测定商品过碳酸钠的纯度,称取一定质量的样品,跟过量盐酸反应,通过测定O2的体积,计算出样品中Na2CO4的质量,并进而计算出Na2CO4的质量分数。实验中提供以下仪器和药品:
在商品中一般都含有Na2CO3,为了测定商品过碳酸钠的纯度,称取一定质量的样品,跟过量盐酸反应,通过测定O2的体积,计算出样品中Na2CO4的质量,并进而计算出Na2CO4的质量分数。实验中提供以下仪器和药品:
(1)根据如图提供的仪器,组装一套测定商品过碳酸钠纯度的实验装置,这套装置按接口的连接顺序是 。
(2)装置④的作用是 。
(3)若在实验中称取0.90g样品进行测定,实验室有50mL、100mL、500mL三种规格的量筒,该实验中所应选用的量筒的规格是 ,其理由是 。
(4)在测定O2的体积之前是否需要排尽装置①中的空气 。
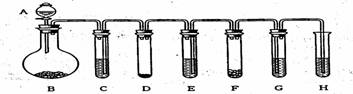
3、“化学多米诺实验”是利用化学反应中气体产生的压力,使多个化学反应依次发生。(整个反应只需要第一个反应发生,就好像多米诺骨牌游戏一样。)以下就是一个“化学多米诺实验”,已知H2O2在MnO2的催化作用下可分解产生O2和H2O。下页图所示的A~ H各装置中分别盛放的物质为:A稀硫酸;B.锌粒;C.3%H2O2溶液;D.MnO2;E.某溶液;F.某块状固体;G.滴有紫色石蕊的蒸馏水;H.足量澄清石灰水。请回答以下各题:(1)实验开始前必须进行的操作是_____________;
(2)反应开始后,若G中出现红色,H中有白色沉淀生成,E、F中的物质可能分别是______;___;
(3)按基本反应类型写出该实验中有关反应的化学方程式:(装置用字母表示)
化合反应_____________________________,发生在装置___________中;
分解反应_____________________________,发生在装置___________中;
置换反应_____________________________,发生在装置___________中;
复分解反应___________________________,发生在装置___________中。
2、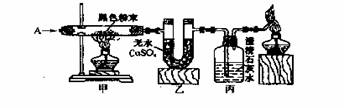 按下图进行实验,已知A为H2、CO中的一种或两者的混合物,甲装置中的黑色粉末为CuO、炭粉中的一种或两者的混合物。
按下图进行实验,已知A为H2、CO中的一种或两者的混合物,甲装置中的黑色粉末为CuO、炭粉中的一种或两者的混合物。
根据下列要求,回答问题:
(1)若黑色粉末是纯净物,甲、乙、丙装置中的固体或溶液依次出现红色、蓝色、浑浊,则气体A是_________,黑色粉末为_________。
(2)若A为纯净物,反应现象与(1)同,则A是______,黑色粉末为______。
(3)若第(1)问中,乙装置的物质增重3.6g,丙装置中的物质增重4.4g,则至少需通入_________g气体。
(4)若第(2)问中,甲装置生成6.4克红色物质,乙装置中物质增重0.9克,则至少需要___克黑色粉末。
1、超氧化钾(KO2)是一种黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用它作制氧剂,供人们呼吸之用。它与二氧化碳反应的化学方程式为:4KO2+2CO2 = 2K2CO3+3O2
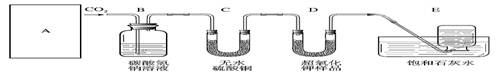
某学生为了验证这一实验,以大理石、足量的盐酸和超氧化钾为原料制取O2,设计出如下实验装置:
 (1)A是制取CO2的装置,应从下列图1、图2、图3中选择 。
(1)A是制取CO2的装置,应从下列图1、图2、图3中选择 。
B装置的作用是吸收A装置中产生的盐酸酸雾,C装置内可能出现的现象是 。为了检验E中收集到的气体,可以在取出集气瓶后,用 的木条伸入集气瓶内,木条会 。
(2)若E中的石灰水出现少量的白色沉淀,这是因为 。
(3)表明D中的超氧化钾样品接近反应完毕时的现象是 。
8、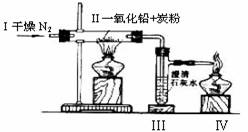
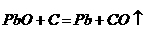 将黄色有毒的一氧化铅(PbO)与炭粉混合,在加热条件下能发生如下反应:
将黄色有毒的一氧化铅(PbO)与炭粉混合,在加热条件下能发生如下反应:
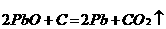
某学生设计了一个证明一氧化铅中含有氧元素(装置如下图所示)。具支试管中盛放澄清石灰水。
(1)通入干燥氮气的作用是将PbO和C反应生成的气体驱赶到仪器Ⅲ中。若改通空气则无法达到目的,原因是空气的 等成为氧的来源。
(2)若该学生实验时在Ⅲ处未见浑浊出现过,则在Ⅱ处发生的反应是(写出化学方程式) 。
(3)若要确保验证一氧化铅中一定存在氧元素的实验成功,请你对上述实验加以改进。具体方案是: 。
7、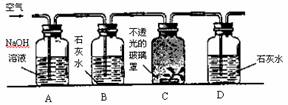 下图是测定植物的某一生命活动过程的装置。A瓶中NaOH溶液的作用是 , B瓶中的石灰水的作用是 ,D瓶中出现的现象是 。此实验说明植物具有 。
下图是测定植物的某一生命活动过程的装置。A瓶中NaOH溶液的作用是 , B瓶中的石灰水的作用是 ,D瓶中出现的现象是 。此实验说明植物具有 。
6、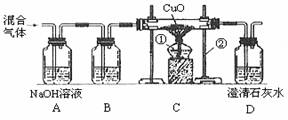 某课外活动小组利用一氧化碳测定。CuO的还原率。实验开始时,对参与实验的气体未作任何处理就直接使用,结果测得的CuO的还原率超过了l00%。后来经过分析讨论并改进实验装置,改进后的实验装置及测得的实验数据如下图、表。
某课外活动小组利用一氧化碳测定。CuO的还原率。实验开始时,对参与实验的气体未作任何处理就直接使用,结果测得的CuO的还原率超过了l00%。后来经过分析讨论并改进实验装置,改进后的实验装置及测得的实验数据如下图、表。
|
混合气体的量(g) |
7 |
|
CuO的量(g) |
20 |
|
沉淀的量(g) |
20 |
试回答: (1)指出图中所标示的仪器的名称:① ;② 。
(2)改进前测得的CuO的还原率超过了100%,其可能的原因是通入的一氧化碳气体中混有 气体。
(3)A装置中发生反应的化学方程式是_________________________________。
(4)若生成的气体在D装置中被完全吸收,则测得的CuO的还原率为 。
(5)为了保护环境,应在D装置的排气管口采取的措施是 :
5、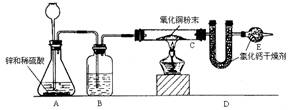 某同学用氢气还原氧化铜的方法测定水的组成,装置如下图。
某同学用氢气还原氧化铜的方法测定水的组成,装置如下图。
请回答:(1)B装置中盛放的液体是__________,其作用是__________。
(2)C装置中观察到的现象是________。
(3)E装置的作用是__________。如果不连接E装置,得出的实验结论中,氢、氧元素质量比将__________(填“>”“<”或“=”)理论值。
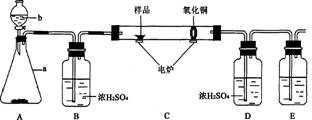
4、下图装置是用燃烧法来确定有机物组成的常用装置,这种方法是在电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成(已知:C中的氧化铜是确保有机物中的碳元素完全转化为二氧化碳; A中的反应为2H202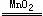 2H2O2+O2↑)。
2H2O2+O2↑)。
回答下列问题:(1)A装置中a仪器的名称 ,b中盛放的物质是 。
(2)若去掉B装置会对什么元素的测量结果有影响? 。
(3)E装置中所盛放物质最好选用________(选填:①氢氧化钙溶液②氢氧化钠溶液③水)。
(4)若准确称取1.12g样品(样品只含C、H、O三种元素中的两种或三种)。经充分燃烧后,D装置增重1.44g,E装置增重3.52g,则该有机物样品中所含的元素为 。
3、某同学使用下图所示装置,试验一氧化碳与氧化铜的反应.请回答下列有关问题:
 (1)有下列实验步骤:①加热;②通入一氧化碳.请用上述实验步骤的标号填空:实验开始时,应先________;然后________.
(1)有下列实验步骤:①加热;②通入一氧化碳.请用上述实验步骤的标号填空:实验开始时,应先________;然后________.
(2)实验进行一段时间后,A装置中出现的现象为__________,说明有______生成;B装置中出现的现象为___________,说明有____生成.
(3)由上述实验可知,一氧化碳具有___________性.在我们已经学习过的物质中,具有这种性质的还有___________和_____________,因此,它们在工业上常用来______________.
(4)在C处放置燃着的酒精灯,目的是________________________________.
 (5)如用该装置进行一氧化碳高温下与氧化铁的反应,请写出反应的化学方程式_______________.工业上运用该原理炼铁时,100吨含氧化铁80%的铁矿石在理论上可制得__________吨含杂质4%的生铁.(计算结果保留三个有效数字,不要求写出计算过程).
(5)如用该装置进行一氧化碳高温下与氧化铁的反应,请写出反应的化学方程式_______________.工业上运用该原理炼铁时,100吨含氧化铁80%的铁矿石在理论上可制得__________吨含杂质4%的生铁.(计算结果保留三个有效数字,不要求写出计算过程).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com