
题目列表(包括答案和解析)
6、有如下四种可供选择的仪器用于量取一定体积的溶液,要求所量的体积越准确越好,现在要量取10mL20%的NaOH溶液,你认为应选择的仪器是( )
 A 50mL烧杯 B 20mL量筒 C 10mL量筒 D 烧杯和托盘天平
A 50mL烧杯 B 20mL量筒 C 10mL量筒 D 烧杯和托盘天平
5、近年来发现海底蕴藏着大量天然气水合物----“可燃冰”,其贮藏量超过已知天然气、石油和煤蕴藏量总合的2倍,是目前开发前景十分诱人的新能源。天然气水合物是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼内可容纳1个甲烷分子或1个游离的水分子。若晶体中每8个笼有6个容纳了甲烷分子,另外两个被水分子填充。则“可燃冰”的平均分子组成为( )
A CH4•5H2O B CH4•6H2O C CH4•7H2O D CH4•8H2O
4、质子和中子都是由u夸克和d夸克组成,u夸克带电量为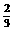 e,d夸克带电量为
e,d夸克带电量为 e,e为基元电荷。下列论断可能正确的是( )
e,e为基元电荷。下列论断可能正确的是( )
A 质子由1个u夸克和1个d夸克组成,中子由1个u夸克和2个d夸克组成
B质子由1个u夸克和2个d夸克组成,中子由2个u夸克和1个d夸克组成
C质子由2个u夸克和1个d夸克组成,中子由1个u夸克和2个d夸克组成
D质子由2个u夸克和1个d夸克组成,中子由1个u夸克和1个d夸克组成
3、人类的认识过程是一个不断深化的过程。在初中,我们从得氧失氧的角度认识了氧化还原反应;在高中,我们将从元素原子得失电子的角度来认识氧化还原反映,而元素原子得失电子表现为元素化合价的变化。因此“元素化合价有升降的化学反映是氧化还原反映。”据判断下列化学反应属于氧化还原的有 ( )
A Zn+H2SO4=ZnSO4+H2↑ B Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
C Na2CO3+2HCl=2NaCl+H2O+CO2↑ D CaCO3 CaO+CO2↑
CaO+CO2↑
2、下列符合“化学反应的绿色化原则”的是( )
A、2C2H4+O2→2C2H4O(C2H4O为期望产品)
B、实验室制取CO2
C、2M+N=CuSO4+H2O FE+CuSO4=FeSO4+Cu
D、用铁屑、氧化铜、稀硫酸为原料制取铜;
1、为了减少大气污染,许多城市推广汽车用清洁燃料。目前使用的清洁燃料主要有两类,一类是压缩天然气(CNG),另一类是液化石油气(LPG)。这两类燃料的主要成分都是( )
A、碳氢化合物 B、碳氧化合物 C、氢气 D、碳氢化合物
19、化学上利用氢化锂(LiH)和水在常温下反应制取氢气,同时生成氢氧化锂,反应的化学方程式为:LiH + H2O = LiOH + H2↑,在LiH中H的化合价是____________。
120g LiOH能和多少克质量分数为10%的稀盐酸恰好完全反应?
18.(6分)味精是烹调菜肴时常用的调味剂,其主要成份是谷氨酸钠。谷氨酸钠有鲜味,易溶于水。小颖发现某品牌味精包装上标注:“谷氨酸钠含量≥80%,氯化钠含量≤20%”。他想测定此味精中的NaCl的含量(谷氨酸钠的存在不影响NaCl的性质)。
(1)下面是他所做实验的有关步骤,请补全实验步骤②。
①称取该味精样品5.0g,并溶于蒸馏水; ②加入过量的__________ 溶液;
③过滤; ④用蒸馏水反复洗涤沉淀多次;
⑤将沉淀烘干、称量,测得固体质量为2.87g。
(2)根据上述实验步骤回答下列有关问题:
①过滤操作中所需要的仪器除了烧杯、铁架台(带铁圈)、玻璃棒外,还需要____________;
②检验沉淀是否洗净的方法是:向洗涤液中滴加 溶液,如果没有沉淀产生,则说明已洗净。
③此样品中NaCl的质量分数为___________,是否符合其包装上标注的标准?_________。
(3)味精的鲜味与溶液的酸碱度有关,当pH为6-7时鲜味最强;味精的鲜味还与温度有关,其水溶液经100℃以上长时间加热,不仅鲜味消失,而且对人体有害。因此试想一下,使用味精时应注意哪些问题?(答一条即可)_______________________________ 。
17、(4分)请你例举会对环境污染的物质或活动,并指明主要会造成哪方面的污染(至少写出两条,多写一条奖励2分,但试卷总分不超过60分)
|
造成污染的物质或活动 |
主要造成哪方面的污染 |
|
⑴ |
|
|
⑵ |
|
|
⑶ |
|
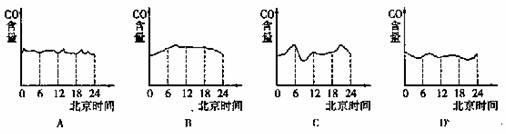
16、(3分)下图能正确表示环境监测人员描绘的某城市中心地区CO含量变化曲线的是________;理由是_____________________________________ ;请你就此现象提出一条你的设想或建议:___________________________ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com