
题目列表(包括答案和解析)
3.下列各组粒子中,属于同一种元素的是
A.Cl和Cl- B. CO2和CO C. H和He D. 和
2.下列粒子中,能保持氢气化学性质的是

 A.H B.H+ C.H2 D.H2O
A.H B.H+ C.H2 D.H2O
1.下列变化,属于化学变化的是
A.蜡烛熔化 B.空气液化制氧气
C.铜器在潮湿的空气中产生铜绿 D.利用干冰进行人工降雨
29.(7分)为测定某石灰石中碳酸钙的质量分数(杂质不与酸反应),向6.0g石灰石样品中逐滴加入稀盐酸
至不再产生气泡为止,共生成二氧化碳气体2.2g。问:
(1)该石灰石样品中碳酸钙的质量分数为多少?(写出计算过程,结果精确至0.1%)(相对原子质量:H
-1;C-12;O-16;Cl-35.5;Ca-40)
(2)若要计算上述反应所消耗盐酸溶液的质量,题中还缺少的一个数据是 。
28.(15分)友情提醒:解本题所用的部分盐的溶解性表见第19题。硫酸钡、氯化银都是不溶于水和稀硝酸
的白色沉淀。
随意丢弃废旧干电池会造成环境污染,而废旧干电池中的许多物质都是可以回收利用的。下面是某
化学兴趣小组探究废旧干电池的过程,请帮助他们完成相应的报告:
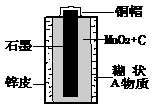 [提出问题] 废旧干电池的组成物质有什么?
[提出问题] 废旧干电池的组成物质有什么?
[探究活动1] 电池中含有的材料有哪些?请各举一例:金属 ;非金
属 ;氧化物 ;……
[探究活动2] 电池内白色糊状物是由什么物质组成的?
[猜想1] 甲同学在剥开电池锌壳时,闻到一股淡淡的刺激性气味,因此,电池的白色糊状物中含有NH4+。
[设计方案1] 取少量白色糊状物与NaOH固体混合置于试管中,加热,用湿润的红色石蕊试纸置于试管
口,观察到试纸变蓝,证明上述猜想正确。
[猜想2] 乙同学认为可能含有OH-、CO32-、Cl-、SO42-中的一种或几种,并需检验白色糊状物。
[设计方案2] 为了验证猜想2,设计如下实验,请完成表格中相应内容。
|
操作步骤 |
实验现象 |
相应的结论 |
|
1.取样。溶于适量的水,静置,过滤。取少量滤液于一支试管中,滴加紫色石蕊试液。 |
石蕊试液不变蓝色 |
|
|
2.另取少量滤液于另一支试管中,滴加稍过量的稀硝酸。 |
无明显现象 |
没有 存在 |
|
3.再向第2步所得溶液中继续滴加少量的
溶液 |
|
没有SO42-存在 |
|
4.向第3步所得溶液中再滴加少量硝酸银溶液 |
有白色沉淀产生 |
有 存在 |
|
5.取白色糊状物,滴加少量碘溶液 |
有蓝色出现 |
有 存在 |
[结论]电池内白色糊状物主要是由 (填一种盐的化学式)和 两种物质混合而成。
[交流与讨论] 通过探究,你认为电池内的白色糊状物有无回收价值? ;理由是 。
[探究活动3] 利用回收的废旧电池制取ZnSO4晶体。
[实验步骤](根据流程提示,填写空格内的内容。)
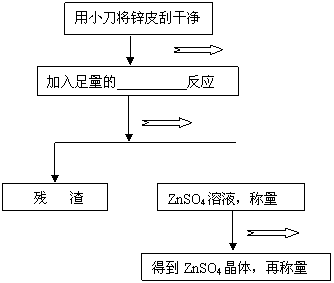
将锌皮放入烧杯中
 化学方程式:
化学方程式:
(填一种实验操作名称)
 加热,蒸发,晾干
加热,蒸发,晾干
[数据处理]丙同学测量的实验数据如下表:
|
|
废电池1个 |
蒸发皿 |
蒸发皿+ZnSO4溶液 |
蒸发皿+ZnSO4晶体 |
|
质量/g |
80 |
46.5 |
225.5 |
62.6 |
回收过程中得到ZnSO4晶体的质量为 g。
27.(3分)根据下表回答问题:
|
实验 内容 |
熄灭酒精灯 |
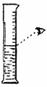
读出量筒内液体的体积数 |
加热液体药品 |
|
实验 操作图 |
 |
 |
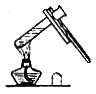 |
|
序号 |
A |
B |
C |
上表的实验操作图中各有一处错误,将造成不良后果,请指出各实验操作图的错误并回答其造成的后果是什么。填在下面的空格内:
(1)A: 。
(2)B: 。
(3)C: 。
26.(4分)下列是初中化学中常见的一些物质间的相互转化关系,其中A、E、F、G为单质,甲、乙、丙均
为黑色固体。
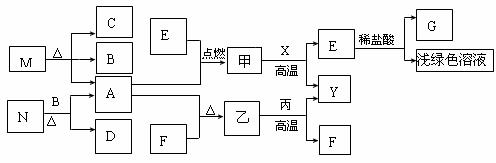
(1)写出下列物质的化学式:
M ,甲 。
(2)写出下列转化的化学方程式:
N→A+D: 。
乙+丙→F+Y 。
25.(6分)右图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
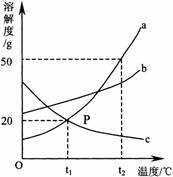 (1)P点的含义是
。
(1)P点的含义是
。
(2)t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是
(填写物质序号)。
(3)t2℃时30 g a物质加入到50 g水中不断搅拌,所得溶液的溶质质量分数是 。
(4)将t1℃时a、b、c三种物质饱和溶液的温度升高到t2℃时,三种溶
液的溶质质量分数大小关系是 (填写选项序号)。
A.c>a=b B.a=b>c C.a>b>c D.b>a>c
24.(4分)请根据燃烧的条件的表示方法,完成形成 “铁锈”和“饱和溶液”的条件,将适当的词语填在方框内。



23.(5分)下表是元素周期表的部分信息,请回答下列问题:
|
1 H 氢 |
|
2 He 氦 |
||||||
|
3 Li 锂 |
4 Be 铍 |
|
5 B 硼 |
6 C 碳 |
7 N 氮 |
8 O 氧 |
9 F 氟 |
10 Ne 氖 |
|
ll Na 钠 |
12Mg 镁 |
|
13 A1 铝 |
14 Si 硅 |
15 P 磷 |
16 S 硫 |
17 C1 氯 |
18 Ar 氩 |
|
19 K 钾 |
xCa 钙 |
…… |
|
|
|
|
|
|
(1)地壳中含量最多的金属元素的原子序数是___________ 。
(2)分析上表可发现:每一横行元素从左向右排列所遵循的一条规律是________________
______________________________。根据此规律,可知图中x = _________。
(3)元素的化学性质主要是由最外层电子数决定的。比较F、Ne、Na、Mg 4种元素的原子结构示意图
可知元素化学性质最稳定的是 。(填字母序号)

(4)许多元素是人体生命必需的元素,青少年缺乏钙元素易患_________(填序号)。
①甲状腺肿大 ②佝偻病 ③坏血病
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com