
题目列表(包括答案和解析)
8.已知20 ℃时KNO3的溶解度为31.6 g,溶解度曲线如右图所示。
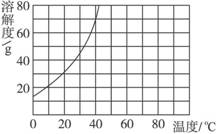
(1)20 ℃时,将25 g KNO3放入到100 g水里,搅拌,得到不饱和溶液。则该溶液中溶质的质量分数为____________。
(2)欲使其变为饱和溶液可采取的方法有:____________或____________或____________。
(3)20 ℃时,将35 g KNO3放入到100 g 水里,搅拌,得到的溶液是____________(填“饱和”或“不饱和”),该溶液中溶质的质量分数是____________。
解析:(1)依据溶质质量分数公式计算。
(2)不饱和溶液要变为饱和溶液,一般可采用:①加溶质;②蒸发溶剂;③降低温度的方法。
(3)从溶解度曲线可知,20 ℃时35 g KNO3放入到100 g水中KNO3不能全部溶解,得到饱和溶液,再用20℃时KNO3的溶解度31.6 g计算:31.6 g/(100+31.6) g×100%=24%。
答案:(1)20% (2)降低温度 蒸发溶剂 增加硝酸钾晶体 (3)饱和 24%
7.t℃时,分别向盛有10 g水的两支试管中,加入等量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象。
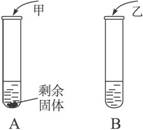

(1)t ℃时,____________(填“A”或“B”)试管中的溶液一定是饱和溶液。
(2)图中可表示甲物质的溶解度曲线的是____________(填“a”或“b”),要使A试管中剩余的固体继续溶解可采用____________或____________的方法。
解析:(1)根据饱和溶液与不饱和溶液的概念可判断A试管中的溶液一定是饱和溶液。
(2)从曲线图上可看出在t ℃时b的溶解度比a小,表示甲的是b;从曲线图上还可知b的溶解度随温度升高而增大,故溶质甲继续溶解,可采用升高温度或加水的方法。
答案:(1)A (2)b 加水 升高温度
6.A、B、C三种固体物质的溶解度曲线如图所示。据图完成下列问题:
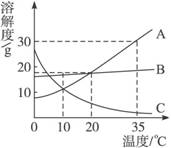
(1)升高温度,接近饱和的____________物质溶液会变得饱和。
(2)10 ℃时,三种物质溶解度大小关系为:________________________。
(3)35 ℃时,A物质的饱和溶液中:溶质、溶剂、溶液的质量比为____________。
(4)20 ℃时,25 g B物质放入到盛100 g水的烧杯中,充分溶解后溶液是(填“饱和”或“不饱和”)____________溶液。
(5)20 ℃时,取100 g A物质的饱和溶液,将温度升高到35 ℃,此时溶液中溶质的质量分数是(填“变大”“变小”或“不变”)____________。
(6)要将A从它的饱和溶液中结晶出来,最好采取____________的方法,而要将B从它的饱和溶液中大量析出,最好采取________________________的方法。
解析:要学会分析溶解度曲线图中的各种含义,能根据曲线图中的数据得出一些结论。
答案:(1)C (2)B>A=C (3)30∶100∶130 (4)饱和 (5)不变 (6)降温结晶 蒸发溶剂结晶
5.某温度下,在100 g水中加入 m g CuSO4或加入n g CuSO4·5H2O均可使溶液恰好达到饱和,则m与n的关系符合( )
A.m=160n/250 B.m=1 600n/(2 500+9n)
C.m=1 600n/(2 500+16n) D.m=1 600n/(2 500+25n)
解析:因为所得溶液均为硫酸铜的饱和溶液,在相同温度下溶质的质量分数相等,所以有:m÷(100+m)=(160n÷250)÷(100+n)。整理后即得答案是B项。本题关键是n g CuSO4·5H2O溶于水后如何确定溶质、溶剂和溶液的质量。
答案:B
4.20 ℃时,将不同质量的氯化钠固体分别放入100 g水中,充分溶解后过滤,所得溶液质量与加入氯化钠质量的对应关系如下表。其中所得溶液一定属于饱和溶液的是( )
|
|
A |
B |
C |
D |
|
加入食盐质量/g |
10 |
20 |
30 |
40 |
|
所得溶液质量/g |
110 |
120 |
130 |
136 |
解析:根据溶液质量等于溶质质量与溶剂质量之和,D组不相等,说明还有未溶解的氯化钠,所以一定属于饱和溶液。
答案:D
3.下列对“20 ℃时,硝酸钾溶解度为31.6 g”的解释正确的是( )
A.20 ℃时,31.6 g硝酸钾溶解在100 g水里
B.20 ℃时,100 g溶液中含31.6 g硝酸钾
C.31.6 g硝酸钾溶解在100 g水中达到饱和状态
D.20 ℃时,31.6 g硝酸钾溶解在100 g水中恰好达到饱和状态
解析:根据溶解度的概念包含以下四个内容:①温度一定;②溶剂一定(100 g);③饱和状态;④单位:克。D选项符合溶解度的概念。
答案:D
2.2004年6月5日世界环境日的主题为“海洋存亡,匹夫有责”。下列说法正确的是( )
A.海水是纯净物 B.海水中的溶质只有氯化钠一种
C.海水是饱和溶液 D.海水晒盐的原理是蒸发溶剂得到晶体
解析:海水中的溶质有多种,但氯化钠的含量较多,而氯化钠的溶解度受温度影响变化不大,应采用蒸发溶剂的方法得到晶体。
答案:D
1.在一个大萝卜中挖一个大孔,向其中注入一定量的饱和食盐水,过一段时间后将里面的食盐水倒出,再往倒出的食盐水中加入少量食盐晶体。则食盐水的质量会( )
A.不变,因为倒出的食盐水还是饱和的
B.增加,倒出的食盐水还是饱和的,但加入了食盐,故溶液的质量增加
C.增加,倒出的食盐水不饱和了,加入的食盐会溶解一部分
D.减少,因为有一部分食盐变成晶体析出
解析:根据生物知识可知,萝卜的水会向饱和食盐水中渗透,使饱和食盐水变得不饱和了,所以还可以继续溶解食盐。
答案:C
7.现有葡萄糖1 kg,经过完全氧化,释放的能量为________kJ.
6.淀粉的化学式为________,它是高分子化合物.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com