
题目列表(包括答案和解析)
22.某溶液中含n个K+、n个SO42-、n个Cl-,除还存在不等量的H+和OH-外,别无其它离子存在,请你推测此溶液
A.pH>7 B.pH=7 C.pH<7 D.pH≥7
21.中国科学技术大学钱逸泰教授等以CCl4和金属钠为原料,在700℃制造出纳米级金刚石粉末。该成果发表在世界最权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”。同学们对此的一些“理解”,不正确的是
A.金刚石属于金属单质 B.制造金刚石过程中发生了化学变化
C. CCl4是一种化合物 D.这个反应是置换反应
20.油炸食物不宜多吃,因为食物长时间煎炸后产生微量的丙烯醛(化学式C3H4O)等有毒物质,会损害人体健康。下列有关丙烯醛的说法不正确的是
A.该物质是由碳、氢、氧三种元素组成
B.该物质中碳、氢、氧元素间的质量比是9:1:2
C.该物质的分子中原子个数比依次为3:4:1
D.该物质在空气中完全燃烧的产物是二氧化碳和水
19.在万众一心,抗击非典的战斗中,人们常用0.04%~0.5%的过氧乙酸溶液对环境消毒。过氧乙酸是无色有强烈刺激性气味的酸性液体,对皮肤有腐蚀性,对眼睛有强烈刺激作用,温度稍高即分解并放出氧气,可作杀虫剂、杀菌剂。下列有关过氧乙酸的说法正确的是
A.过氧乙酸溶液可直接服用 B.可以用手直接接触过氧乙酸溶液
C.过氧乙酸性质稳定 D.过氧乙酸溶液不能直接喷洒到金属制品表面
18.应用储能介质(某种结晶水合物)储存和再利用太阳能是一项新技术,其原理是:当白天阳光照射时,储能介质熔化,同时吸收热能。当夜晚环境温度降低时,储能介质凝固,同时释放出热能,某地区的白天气气温可达40℃,夜晚可下降至-10℃以下,根据上述原理和表中几种常见储能介质的有关数据,该地区应用上述技术调节室温时,选用储能介质最好是
结晶水合物 熔点 熔化时吸热/KJ·g-1
A. CaCl2 ·6H2O 29 0.172
B. Na2SO4·10H2O 32.4 0.239
C. Na2HPO4·12H2O 36.1 0.282
D. Na2S2O3· 5H2O 48.5 0.200
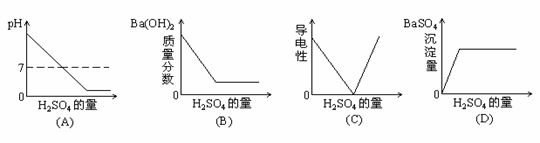
17.向一定量的Ba(OH)2溶液中逐滴加入稀H2SO4,与反应有关的变化关系用下图表示。其中错误的是
16.将一定量的铁粉加入到AgNO3和Cu(NO3)2的混合溶液中,当铁与Cu(NO3)2恰好完全反应后,过滤。则以下的分析中正确的是
A.滤纸上留下的物质是铜 B.滤纸上留下的物质有铜和银
C.滤液中的溶质是AgNO3 D.滤液中的溶质是Fe(NO3)3
15.下列基本操作正确的是
A.过滤时使用玻璃棒引流液体
B.给试管中的液体加热时液体体积不超过试管容积的1/2
C.将固体氢氧化钠固体直接放在托盘天平的左盘上称量
D.把胶头滴管伸入试管内滴加试液
14.下列各组物质不能发生化学反应的是
A.NaOH溶液和稀HNO3 B.AgCl和KNO3
C.CaCO3和稀HCl D.BaCl2溶液和稀H2SO4
13.能一次区别开NaOH、H2SO4和H2O的试剂是
A.锌粒 B.无色酚酞试液 C.氯化钡溶液 D.紫色石蕊试液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com