
题目列表(包括答案和解析)
5.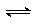 下列哪种说法可以证明N2 + 3H2 2NH3已达平衡状态( C )
下列哪种说法可以证明N2 + 3H2 2NH3已达平衡状态( C )
A.1个N≡N键断裂的同时,有2个N-H键断裂
B.1个N≡N键断裂的同时,有3个H-H键断裂
C.1个N≡N键断裂的同时,有6个N-H键断裂
 D.1个N≡N键断裂的同时,有6个N-H键生成
D.1个N≡N键断裂的同时,有6个N-H键生成
4.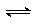 对于反应N2 + O2 2NO在密闭容器中进行,下列条件哪些不能加快反应的化学反应的化学反应速率(温度不变)( CD )。
对于反应N2 + O2 2NO在密闭容器中进行,下列条件哪些不能加快反应的化学反应的化学反应速率(温度不变)( CD )。
A.缩少体积使压强增大 B.体积不变充入N2使压强增大
C.体积不变充入 He使压强增大 D.减少压强使体积增大
3.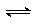 已知反应:3A + 4B C + 2D 其反应速率可以分别用V(A)、V(B)、V(C) 、V(D) [mol/(L·min)]表示,则正确的关系是( B )。
已知反应:3A + 4B C + 2D 其反应速率可以分别用V(A)、V(B)、V(C) 、V(D) [mol/(L·min)]表示,则正确的关系是( B )。
A.V(A)=1/3V(C) B.V(B)=4/3V(A)
C.V(C)=4V(B) D.V(D)=1/2V(C)
2.反应:A + 3B 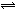 2C + D,在四种不同情况下的反应速率分别为:
2C + D,在四种不同情况下的反应速率分别为:
①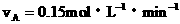 ②
②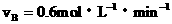
③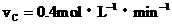 ④
④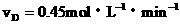
该反应进行得最快的是(B )
A.① B.④ C.①④ D.②③
1.下列反应在常温下均为非自发反应,则在高温下仍为非自发的是( A )
A. 2CO(g)====2 C(s)+ O2(g)
B. 2CuO(s) ====Cu2O(s)+1/2O2(g)
C. MgCO3(s)====MgO(s)+CO2 (g)
D.SnO2(s)+C(s) ==Sn(s)+ CO2 (g)
6.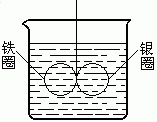 如右图所示,在盛有水的烧杯中,等质量的铁圈和银圈的连接处,吊着一根绝缘的细丝,使之平衡。小心地在 烧杯中央滴入CuSO4溶液。
如右图所示,在盛有水的烧杯中,等质量的铁圈和银圈的连接处,吊着一根绝缘的细丝,使之平衡。小心地在 烧杯中央滴入CuSO4溶液。
⑴经过一段时间后,观察到的现象是(指金属圈) 。
A.铁圈和银圈左右摇摆不定
B.保持平衡状态不变
C.铁圈向下倾斜 D.银圈向下倾斜
⑵产生上述现象的原因是 。
答案⑴D (3分)
⑵Fe和Ag形成原电池,Fe极Fe溶解, Ag极析出Cu增重。(3分)
5.在盛有饱和Na2CO3溶液的烧杯中插入惰性电极,保持温度不变,通直流电一段时间后,
则( C )
A.溶液的pH增大 B.溶液的浓度增大,有一定量的晶体析出
C.溶液的浓度不变,有晶体析出 D.溶液的pH减小
4.用铂作电极电解一定浓度的下列物质的水溶液。电解结束后,向剩余电解液中加适量水,能使溶液和电解前相同的是( C )
A.AgNO3 B.HCl C.NaOH D.NaCl
3、新近研制的溴-锌蓄电池的基本结构是用碳棒作两极,用ZnBr2溶液作电解液,现有四个电极反应:①Zn – 2e = Zn2+ ②Zn2+ + 2e = Zn ③Br2 + 2e = 2Br- ④2Br- - 2e = Br2 ,充电时的阳极和放电时的负极反应分别依次为(A)
A、④① B、②③ C、③① D、②④
2.银锌电池(钮扣式电池)的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为 Zn+2OH--2e-=ZnO+H2O;
Ag2O+H2O+2e- = 2Ag+2OH- ;总反应为:Ag2O+Zn=2Ag+ZnO,下列判断正确的是( BC )
A、锌为正极,Ag2O为负极
B、锌为负极,Ag2O为正极
C、原电池工作时,负极区PH减小
D、原电池工作时,负极区PH增大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com