
题目列表(包括答案和解析)
32.利用中和反应可以测定酸或碱溶液中溶质的质量分数。例如,在一定量的待测酸(或碱)溶液中逐滴滴入已知质量分数的碱(或酸)溶液(这种溶液被称为标准溶液),直到酸、碱恰好完全反应,根据消耗标准碱(或酸)溶液的多少即可求算出待测酸(或碱)溶液的溶质质量分数。
右下图为某次测定过程中,溶液的pH随所滴加的某标准溶液体积的变化而变化的关系图。
(1)根据右下图曲线可以判断在实验中是向 (填“酸”或“碱”,下同)溶液(待测液)中滴加 溶液(标准液)。
(2)在这次测定中,为了指示中和反应刚好完全,用酚酞做指示剂,即在待测溶液中先滴入几滴酚酞试液,若看到 现象,则证明中和反应刚好完全。
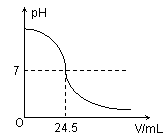 (3)如果实验中使用的酸是硫酸溶液,碱是氢氧化钠溶液,且待测液和标准液的密度均以1.0g/mL计。若测定中取用待测液25mL,标准液溶质的质量分数为4.5%,根据图中数据,计算待测液溶质的质量分数。
(3)如果实验中使用的酸是硫酸溶液,碱是氢氧化钠溶液,且待测液和标准液的密度均以1.0g/mL计。若测定中取用待测液25mL,标准液溶质的质量分数为4.5%,根据图中数据,计算待测液溶质的质量分数。
31.(7分)图1中的A为一种常见的金属单质的黑色粉末,实验时先预热试管再加热A物质,过一会儿加热湿沙子,实验收集的气体为H2,原A物质已变成了化合物B,但仍为黑色,并能被磁铁吸引.
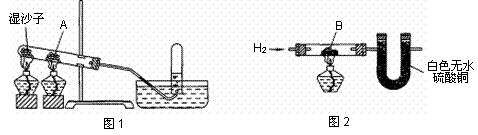

⑴ 请认真分析后指出:
A物质的化学式为: ;
化学方程式为 。
⑵ 如果将图2中由A物质反应后生成的B物质取出,按图2进行实验,结果白色无水硫酸铜粉末变为蓝色,黑色化合物B又变成了物质A.该反应化学方程式:
⑶ 欲证明镁、该金属、铜的金属活动性,若用三种物质证明其活动性顺序,所需要用到的试剂有 、 、 。
⑷ 将一定量的镁条投入过量的稀盐酸中,表示反应过程中变化关系的曲线正确的是




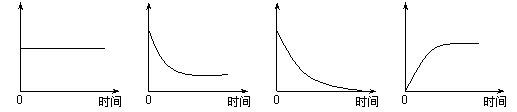

A B C D
30.(8分)回收废旧干电池、保护环境是我们每个公民的义务,下面是我校化学兴趣小组探究废旧干电池意义的过程(片断),请帮助他们完成相应报告:
[提出问题] 废旧干电池的组成物质有什么?
[查阅资料] 淀粉遇I2变蓝色
[活动探究1] 电池中含有的材料有哪些?请各举一例:金属 ;非金属 ;……
[活动探究2] 电池的内容物中有没有我们熟悉的离子?
[猜想1] 小组中一同学在剥开电池锌壳时,闻到一股淡淡的刺激性气味,因此他猜想:电池的内容物中含有NH4+
[设计方案1] 取少量白色糊状物与 混合、研磨,闻到氨味,证明上述猜想正确。
[猜想2] 可能含有OH-、CO32-、Cl-中的一种或几种。
[设计方案2] 为了验证猜想2,设计如下实验,请完成表格中相应内容。
|
操作步骤 |
实验现象 |
相应的结论 |
|
1.取样。溶于适量的水,静置,过滤。取少量滤液于试管中,滴加紫色石蕊试液。 |
石蕊试液不变蓝色 |
|
|
2.另取少量滤液于另一支试管中,滴加稍过量的稀硝酸。 |
无明显现象 |
没有
存在 |
|
3.向第2步所得溶液中滴加硝酸银溶液 |
有白色沉淀产生 |
有 存在 |
|
4.取白色糊状物,滴加少量碘液 |
有蓝色出现 |
则说明有淀粉存在 |
[结论]上述实验证明,电池内白色糊状物主要是 (一种盐)和淀粉等两种物质混合而成。
[交流与讨论] 若将上述步骤2中滴加稀硝酸改为滴加稀盐酸,你认为对本实验有无影响?说明你的理由。
29.(6分)现有A贮气瓶中的混合气体(主要有CO,内含少量CO2),以A为原料制备纯净干燥的CO用于还原氧化铜,并验证反应产物。依照图示装置回答:
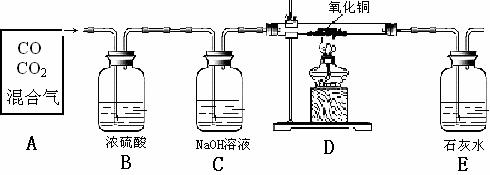
(1)B装置的作用是 , C装置的作用是 。
(2)E装置中观察到的现是 ,其反应的化学方程式为
(3)上述整套装置中有两处明显错误,请分别说明
;
28.
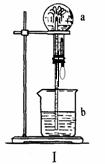
 在如图I装置中,烧瓶中充满干燥的气体a,将滴管中的b液体挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹,烧瓶内气体a由于极易溶解于液体b,使烧瓶内气压小于外界大气压,从而把烧杯内的液体压回烧瓶,呈喷泉状喷出,最终几乎充满烧瓶。则
在如图I装置中,烧瓶中充满干燥的气体a,将滴管中的b液体挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹,烧瓶内气体a由于极易溶解于液体b,使烧瓶内气压小于外界大气压,从而把烧杯内的液体压回烧瓶,呈喷泉状喷出,最终几乎充满烧瓶。则
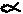 (2分)(1)a和b分别是( )
(2分)(1)a和b分别是( )
A.N2,H2O B.CO2,浓NaOH
C.NH3,盐酸 D.O2,H2O
 (2)写出上述能进行化学反应的一个化学方程式 。
(2)写出上述能进行化学反应的一个化学方程式 。
(4分)(3)某学生设计了如图Ⅱ的喷泉实验:
①在图中的锥形瓶里,分别加入足量的下列物质,反应后能产生
喷泉的是( )。
A.Cu和稀盐酸 B.HCl溶液和NaOH溶液
C.Fe2O3和稀硫酸 D.Zn和稀硫酸
②在图II的锥形瓶外放一水槽,向锥形瓶加入酒精,水槽中加入
冷水后,再分别加入足量的下列物质,可产生喷泉的是( )
A.生石灰 B.硫酸铜 C.浓硫酸 D.硫酸钾
27.
 (3分)氯气是一种黄绿色、有毒、能溶于水、密度比空气大的气体,实验室制备氯气的化学方程式为
(3分)氯气是一种黄绿色、有毒、能溶于水、密度比空气大的气体,实验室制备氯气的化学方程式为
MnO2 + 4HCl(浓)==== MnCl2 + 2H2O + Cl2↑
(1)右图为实验室制取氯气的装置图,请写出
仪器a的名称 ;
(2)该实验中收集氯气的方法是 ;
(3)通常烧杯中盛装氢氧化钠溶液,在此所起的作用是_____ _ 。
26.(9分)(1)检验无水酒精中是否含有微量水分的最简便的方法是:取少量无水酒精,向酒精中加入少量 粉末。若含有水,观察到的现象是 。
(2)肥皂的主要成分是硬脂酸钠(C17H35COONa),将其与稀盐酸混合,会产生白色沉淀,沉淀为 (写名称,下同);与硬水混合,也会产生沉淀,沉淀为 。
(3)20g氢气和氧气的混合气体完全燃烧,生成水18g,则氢气最多为 g。
氯气是一种有毒的气体,它能与水反应生成盐酸和次氯酸(HClO),反应为 次氯酸具有漂白性,它可以将某些有色物质氧化为无色物质。某同学将氯气的水溶液滴入含酚酞试液的NaOH溶液中,当滴到最后一滴时,红色突然褪去。红色褪去的原因可能有两种情况① ,② 。请设计一个实验,确定红色褪去的原因是①还是② 。
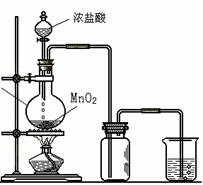
25.(6分)下图是初中化学所学的常见化合物之间的相互转化关系(反应条件和生成产物中的水已略去)。其中A是一种常见的建筑材料,B是一种常见的气体,H是一种含钠的化合物。
请回答下列问题:
⑴ 写出A、F、H的化学式 :A_____________ ;F____________ ;H______________。
⑵ 写出反应的化学方程式:
① E + HCl ___________________________________________;
② E + G _____________________________________________;
③ B + D 。
24.(2分)瑞奥丁托河是一条酸河,河水中含有硫酸亚铁和硫酸,经调查发现,酸河形成的原因是由于上游河床含有黄铁矿(FeS2)在水中氧的作用下发生反应所致,该反应的化学方程式 。
23.(3分)研究课上,小欣同学为了验证氨气(NH3)的某些性质,做了以下实验:下图中从左向右依次是她做的实验及相应现象。


通过实验,小欣得出氨气的三点性质,分别是:
① __________________,② __________________。③ ___________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com