
题目列表(包括答案和解析)
3.将3g某物质在氧气中充分燃烧生成8.8g CO2和5.4g水,则该物质的组成中 ( )
A.只含C、H B.可能含O
C.一定含O D.一定含有C、H、O
2.有反应3A+2B=2C+D,A、B两种物质完全反应时的质量比为3:4,若生成C和D共140g,则反应消耗B的质量为 ( )
A.60g B.90g C.80g D.120g
1.宣传科学知识,揭露伪科学是我们的义务,下列各项中不属于伪科学的是 ( )
A.用催化剂将水变成汽油 B.人可用眼睛直接观察到氧气分子
C.干冰可用于人工降雨 D.人发功可将银变成金
7.某学习小组用图示装置测定黄铜屑(锌铜合金)的组成,取一定量的黄铜屑放入烧杯中,并加入足量稀硫酸。不同时间电子天平的读数如下表所示(不考虑H2O逸出):
|
反应时间/min |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
烧杯及所盛物质总质量/g |
335.70 |
335.54 |
335.44 |
335.38 |
335.34 |
335.32 |
335.31 |
335.30 |
335.30 |
(1)反应生成H2的总质量为 g。
(2)若要计算黄铜屑中锌的质量分数,还缺少的数据是 ,
若该数据用a表示,求出黄铜屑中锌的质量分数(写出计算过
程)。
(提示:Zn+H2SO4=ZnSO4+H2↑,铜不与稀硫酸反应)
单元测试题
6. 下图为某加钙食盐包装袋袋上的标签。小明通过下列方法检查该食盐中的钙元素的含量:往装有稀硝酸的小烧杯(总质量为200.00g)加入30.00g该盐样品,充分反应后,无固体剩余。反应后烧杯和溶液的总质量为229.67g。
下图为某加钙食盐包装袋袋上的标签。小明通过下列方法检查该食盐中的钙元素的含量:往装有稀硝酸的小烧杯(总质量为200.00g)加入30.00g该盐样品,充分反应后,无固体剩余。反应后烧杯和溶液的总质量为229.67g。
(已知:CaCO3+2HNO3=Ca(NO3)2+H2O+CO2↑)
(1)反应过程中产生__________gCO2
(2)30.00g该食盐中含碳酸钙的质量是多少?
(3)此加钙食盐钙含量是否符合标签要求?
5. 请你利用下图中所提供的3个数据,自拟一道有关化学方程式的计算题,并写出解答过程。
请你利用下图中所提供的3个数据,自拟一道有关化学方程式的计算题,并写出解答过程。
4.工业上用电解氧化铝的方法制取单质铝的化学方程式为:
2Al2O3 通电 4Al+3O2↑,电解10t氧化铝最多可生产多少吨铝?小丽和小明两位同学分
别采用了两种不同的计算方法。
|
小丽同学的解法 |
小明同学的解法 |
|||
|
解:设铝的质量为x 2Al2O3 通电 4Al + 3O2↑ 204 108 10t x
答:最多可生产5.3t铝. |
 解:氧化铝中铝元素的质量分数: 解:氧化铝中铝元素的质量分数:铝的质量为:10t × 53% = 5.3t 答:最多可生产5.3t铝. |
请你回答下列问题:
(1)你认为他们的解题思路和方法都正确吗?
(2)对“34g过氧化氢完全分解,产生氧气的质量为多少g?”一题,你认为也能用上述两种方法解答吗?试试看,请把能用的解法过程写出来。
(3)你认为在什么情况下,小丽和小明同学的解法都能使用?
|
自拟试题内容部分 |
自拟试题解答部分 |
3.已知H2能在O2、Cl2中燃烧,右图中横坐标表示完全燃烧时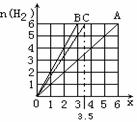 消耗气体X(X=A,B,C)的分子数n(X),纵坐标表示消耗H2的分子数n(H2),已知A、B是纯净物,C是由A和B组成的混合物,则C中的n(A):n(B)为( )
消耗气体X(X=A,B,C)的分子数n(X),纵坐标表示消耗H2的分子数n(H2),已知A、B是纯净物,C是由A和B组成的混合物,则C中的n(A):n(B)为( )
A.2:1 B.2:3
C.2:5 D.1:1
2.使12g镁分别在一定量氧气中燃烧,得如下实验数据:
|
|
第一次 |
第二次 |
第三次 |
|
所给氧气的质量g |
4 |
8 |
16 |
|
生成氧化镁的质量g |
10 |
20 |
20 |
下列关于以上实验的说法错误的是 ( )
A.第一次实验中镁没有燃烧完 B.只有第二次实验遵守质量守恒定律
C.第三次实验中氧气没有消耗完 D.三次实验中固体质量都增加了
1. 利用化学方程式计算的依据是 ( )
A.化学方程式表示了一种化学反应过程
B.化学方程式表示了反应物、生成物和反应条件
C.化学方程式表示了反应前后反应物和生成物的质量关系
D.化学方程式表示了各反应物质量比等于各生成物质量比
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com