
题目列表(包括答案和解析)
32. (7分)化学兴趣小组的同学对未贴标签的Na2CO3、NaOH、Ca(OH)2、稀盐酸四瓶溶液进行鉴别。老师给他们提供的药品只有紫色石蕊试液,实验仪器只有试管和胶头滴管。
(7分)化学兴趣小组的同学对未贴标签的Na2CO3、NaOH、Ca(OH)2、稀盐酸四瓶溶液进行鉴别。老师给他们提供的药品只有紫色石蕊试液,实验仪器只有试管和胶头滴管。
(1)甲组同学利用紫色石蕊试液鉴别四种溶液:
|
实验操作 |
实验现象与结论 |
|
步骤1:用四支试管,各取少量四种溶液,分别滴加紫色石蕊试液。 |
一支试管溶液由无色变成红色,则原溶液是 ① 溶液。其余三支试管溶液变蓝。 |
|
步骤2:另用三支试管,各取少量未确定的三种溶液,分别滴加步骤1检验出的溶液。 |
一支试管溶液中有气泡放出,则原溶液是 ② 溶液。其余两支试管无明显现象。 |
|
步骤3:另用两支试管,各取少量未确定的两种溶液,分别 ③ 。 |
④ 。反应的化学方程式为 ⑤ 。 |
(2)乙组三位同学认为,不用紫色石蕊试液也能鉴别出四种溶液,他们分别选定四种待测溶液中的一种,然后分别取其他三种溶液于试管中,分别滴加各自选定的溶液。三位同学观察到的实验现象及结论记录如下:
|
同学 |
实验现象 |
结 论 |
|
小峰 |
一支试管溶液中有气泡放出,其余两支试管溶液中无现象。 |
所滴加的溶液是稀盐酸。 |
|
小伟 |
一支试管溶液中有白色沉淀析出,其余两支试管溶液中无现象。 |
所滴加的是Na2CO3溶液。 |
|
小明 |
三支试管溶液中都无现象。 |
所滴加的是NaOH溶液 |
乙组三位同学经过交流后发现 ① 同学的结论是错误的,所滴加的溶液应是 ② 溶液,由此鉴别出了四种溶液。
31. (6分)根据下图回答问题。
(6分)根据下图回答问题。

(1)实验室用高锰酸钾制氧气的化学方程式是 ① ,反应的发生装置为 ② (填序号)。若采用C装置收集氧气,验满的方法是 ③ 。
(2)实验室制取二氧化碳应选用的发生装置和收集装置为 ① (填序号),该制取装置 ② (填“能”或“不能”)用于实验室制取氧气,其理由是 ③ 。
30.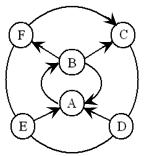 (5分)A~F为初中常见的六种物质,它们的相对分子质量依次增大,相互之间的关系如右图所示(图中弧线表示两端的物质能发生化学反应;箭头表示物质间存在转化关系。部分反应物或生成物以及反应条件已略去):
(5分)A~F为初中常见的六种物质,它们的相对分子质量依次增大,相互之间的关系如右图所示(图中弧线表示两端的物质能发生化学反应;箭头表示物质间存在转化关系。部分反应物或生成物以及反应条件已略去):
(1)B物质的化学式为 ① ;A转化为B的化学方程式为
② ;C与D反应的化学方程式为 ③ 。
(2)在所有相关反应中没有出现的基本反应类型是 ① ,
请补充一个属于该类型的化学方程式 ② (要求:至少有
一种反应物选自A~F)。
29.(4分)了解物质构成的微观奥秘,能帮助我们更好地认识物质变化的本质。
 (1)下列有关原子的结构说法正确的是____(填序号)。
(1)下列有关原子的结构说法正确的是____(填序号)。
A.原子不可再分 B.原子核一般是由质子和中子构成
C.电子带负电 D.原子核带正电
E.原子核体积很小,核外有相对很大的空间
F.电子的质量比原子核的质量大
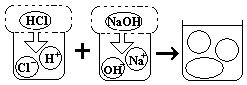 (2)右图是氢氧化钠溶液和盐酸反应实质的微观示意图。当它们恰好完全反应后,溶液中的三种粒子是____(填粒子符号)。
(2)右图是氢氧化钠溶液和盐酸反应实质的微观示意图。当它们恰好完全反应后,溶液中的三种粒子是____(填粒子符号)。
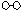

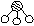 (3)2007年,化学家埃特尔证实了氢气与氮气在固体催化剂表面合成氨(NH3)的反应过程,获得诺贝尔化学奖。用 、 、 分别表示N2、H2、NH3三种分子。为了便于理解,我们将在固体催化剂表面(用
(3)2007年,化学家埃特尔证实了氢气与氮气在固体催化剂表面合成氨(NH3)的反应过程,获得诺贝尔化学奖。用 、 、 分别表示N2、H2、NH3三种分子。为了便于理解,我们将在固体催化剂表面(用  表示)合成氨的过程简化为下图中的五个步骤,请按照正确的步骤进行排序_____(填序号)。
表示)合成氨的过程简化为下图中的五个步骤,请按照正确的步骤进行排序_____(填序号)。
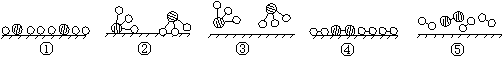
28.(7分)金属材料在生产、生活中应用广泛。
(1)下列铁制品中,利用金属导热性的是 (填序号)。




A.铁锅 B.铁丝 C.水龙头 D.铁锤
 (2)联合钢铁工业的基本生产流程示意图如下:
(2)联合钢铁工业的基本生产流程示意图如下:
石灰石、生铁和钢均属于 ① (填“纯净物”或“混合物”)。生铁和钢的主要区别是 ② 。写出以赤铁矿(主要成分是氧化铁)为原料,用一氧化碳冶炼生铁的化学方程式为 ③ 。
(3)颗粒达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”。实验室制备的方法是:以高纯氮气作保护气,在高温条件下用氢气和氯化亚铁发生置换反应,生成“纳米铁”,
反应的化学方程式为 。
(4)氯化铁能腐蚀铜(2FeCl3+Cu=2FeCl2+CuCl2),工业上常用此原理生产印刷线路板。

步骤Ⅱ中发生了两个反应:2FeCl3+Fe=3FeCl2和 ① ;滤渣的成分有 ② 。
27.(7分)水是生命之源,通过化学学习,我们进一步认识到水的重要作用。
(1)自然界的水常常遭到人为污染。污染物中氮和磷含量过高会造成水中藻类过度繁殖,使水质恶化,这里的“氮和磷”是指 (填序号)。
|
A.元素 |
B.原子 |
C.离子 |
D.分子 |
(2)自然界的水经过一系列净化处理后,成为比较清洁的自来水。自来水不是纯水,若要制取纯水,应采取的净化方法是 ① 。碗碟上的油污用自来水很难洗净,往水中滴加少量洗涤剂后,就很容易洗净,说明洗涤剂具有 ② 功能。
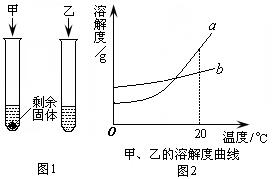 (3)20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10 g水,使其充分溶解,观察到如右图1所示的现象。20℃时,
(3)20℃时,向两支试管中加入等质量的甲、乙两种固体物质,分别加入10 g水,使其充分溶解,观察到如右图1所示的现象。20℃时,
① (填“甲”或“乙”)的溶液一定是饱和
溶液。右图2中表示甲物质的溶解度曲线的
是 ② (填“a”或“b”),要使试管中剩余的
甲固体继续溶解可采用的方法是 ③ 。将10℃
a的饱和溶液升温到20℃,其溶质质量分数 ④
(填“变大”、“变小”或“不变”)。
26.(6分)日常生活中注意膳食合理、营养均衡对人体健康很重要。
(1)下表为某品牌燕麦片标签中的一部分。
|
每100 g含有 营养成分 |
糖类 |
油脂 |
蛋白质 |
维生素C |
钙 |
钠 |
锌 |
|
7.6 g |
7.8 g |
7.4 g |
18 mg |
201 mg |
30.8 mg |
8.1 mg |
燕麦片的营养成分中能为人体提供能量的是 ① ;属于人体必需的微量元素是 ② 。
|
姓名:王晓明 性别:男 年龄:15 |
|||
|
编号 |
项目 |
结果 |
参考值 |
|
1 |
血清钾 |
4.15 |
3.50-5.50 |
|
2 |
血清钠 |
145.4 |
135.5-145.0 |
|
3 |
血清氯 |
100.7 |
95.0-108.0 |
|
4 |
钙 |
1.94 |
2.10-2.26 |
|
5 |
磷 |
0.55 |
0.18-1.55 |
|
6 |
镁 |
0.75 |
0.65-1.25 |
(2)右表是王晓明同学体检化验报告单中的部分内容。对比表中化验“结果”与“参考值”的数据,你能发现王晓明体内 ① 元素指标偏低,这可能会引起的疾病是 ② (填序号)。
A.佝偻病 B.贫血
C.坏血病 D.甲状腺肿大
 (3)添加了营养剂的“铁强化”酱油已经面市。根据卫生部的标准,每100 mL酱油中铁营养剂添加量是200
mg,
(3)添加了营养剂的“铁强化”酱油已经面市。根据卫生部的标准,每100 mL酱油中铁营养剂添加量是200
mg,
其中铁元素质量分数为12.5%。酱油中的铁只有10%能被人体吸收,如果食
用16 mL该酱油,能从酱油中吸收的铁元素为 ① mg,这相当于服用补铁
剂FeSO4 ② mg(最后结果保留一位小数)。
25.双氧水是过氧化氢的水溶液,一定溶质质量分数的双氧水可用于医疗消毒。某瓶双氧水中氢元素与氧元素的质量比为1∶10,则该瓶双氧水中溶质的质量分数为
|
A.3.1% |
B.30% |
C.35.2% |
D.38.6% |
24.下列四个坐标图分别表示四个实验过程中某些量的变化,其中正确的是
A.向一定量的氢氧化钠溶液中滴加稀盐酸直至过量
B.向一定量的硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液直至过量
C.将足量碳酸镁和氧化镁固体分别加入相同质量、相同溶质质量分数的稀盐酸中
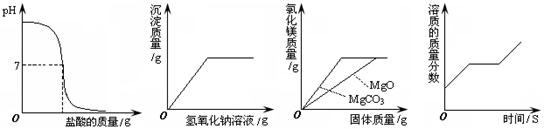 D.将一定质量的硝酸钾不饱和溶液恒温蒸发水分,直至有少量晶体析出
D.将一定质量的硝酸钾不饱和溶液恒温蒸发水分,直至有少量晶体析出
A. B. C. D.
23.向Na2CO3溶液里滴加稀盐酸,开始时无气泡产生,后来才有气泡产生;向稀盐酸里
滴加Na2CO3溶液时,立即就有气泡产生。下列推测合理的是
A.Na2CO3跟稀盐酸不反应 B.产生的气泡是挥发出来的氯化氢气体 C.稀盐酸不足量时,主要发生的反应是Na2CO3+2HCl=2NaCl+H2O+CO2↑
D.Na2CO3过量时,主要发生的反应是Na2CO3+HCl=NaHCO3+NaCl
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com