
题目列表(包括答案和解析)
31.(4分) 煤炭中往往含有硫,直接燃烧产生的二氧化硫会污染环境。计算含硫400g的煤炭完全燃烧所产生二氧化硫气体的质量。
30.(6分) 蛋白质是机体生长及修补受损组织的主要原料,人体通过食物获得的蛋白质在胃肠中与水反应,生成氨基酸,蛋氨酸(C5H11O2NS)就是其中的一种氨基酸。
⑴蛋氨酸中氧、硫元素的质量比为____________
⑵氮元素的质量分数为
⑶合格奶粉每100g中含蛋白质18g,蛋白质中氮元素的平均质量分数为16%,则每100 g合格奶粉中氮元素的质量至少为 g
29.(5分)某兴趣小组对“水的化学式是如何以实验方法确定的”进行研究。
[提出假设]设水的化学式为H2O;
[查阅资料]在标准状况下,氢气的密度ρH2= 0.09 g/L,氧气的密度ρO2=1.43g/L,氢的相对原子质量为l,氧的相对原子质量为16;
[研究原理]运用化合物中各元素的质量之比等于组成该化合物各元素的实际质量之比的原理,求出一个水分子中氢原子和氧原子的个数之比;
[实验探究]
|
实验操作 |
实验装置图 |
实验记录及结果 |
|
①
用如图所示的装置 电解水 ②检验产生的气体 |
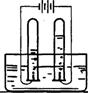 |
①经检验,负极产生的气体是
。 ②负极产生的气体与正极产生的气体体积之比约为 。由此实验说明:水是由氢、氧两元素组成的。 |
[数据处理]兴趣小组首先设水的化学式为HxOy,再根据实验结果及有关数据,并利用研究原理进行了计算。请你将其计算过程进行补充。(最后结果取整数)
[得出结论]兴趣小组提出的假设 。(填“正确”或”不正确”)
28.(7分)机动车排放的尾气是空气的重要污染源,其成分之一是NO。某化学兴趣小组的同学在查阅资料后得知:①NO常温下是一种无色、难溶于水的气体,它的密度比空气略大;②NO常温下能与氧气迅速反应,生成红棕色的NO2气体:2NO2+O2=2NO2;③实验室常用铜与稀硝酸反应制取NO:3Cu+8HNO3(稀) = 3Cu(NO3)2+2NO↑十4X。
根据以上信息完成下列问题:
⑴物质X的化学式为___________。
⑵写出下列仪器名称:a_______________ b_______________
⑶若选择合适的装置来制取并收集NO气体,你选择的发生装置是__ __,收集装置是_______。
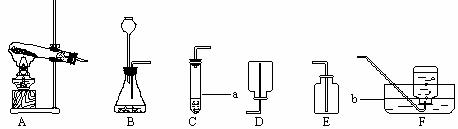
⑷实验时在发生装置中可以观察到:铜片不断溶解并得到蓝色溶液,还能观察到的现象有______________________________________________________________________。
⑸该小组的同学通过查阅资料还得知:①NO容易和血红蛋白结合而使人中毒;②NO能抗击侵入人体的微生物,并能阻止癌细胞的繁殖和肿瘤细胞的扩散。综合分析①和②可知:NO让人欢喜让人忧。请另仿一例:___________________ ______________________________ 。
27.(4分)化学实验基本操作在化学学习和研究中具有重要作用。错误操作常会引起不良后果,请说出可能引起下述后果的原因。
⑴过滤操作后得到的滤液仍然浑浊 ;
⑵铁丝在氧气中燃烧时集气瓶炸裂 ;
⑶实验室制氧气时试管破裂 ;
⑷加入锌粒时试管破裂____________________________________ ___________。
26.(8分) 水是一种极其重要的自然资源,没有水就没有生机勃勃的地球。今年世界水日主题为“应对水短缺”。“中国水周”活动宣传活动的主题为“水利发展与和谐社会”。水资源的保护和合理利用已受到人们的普遍关注。请参与讨论下列有关问题:
(1)不论是河水还是海水,你认为保持水的化学性质的最小粒子是____________。下列能确认水是由氧元素和氢元素组成的实验是 (填序号)。
A.水的蒸馏 B.水的蒸发 C.水的电解 D.水的净化
(2)小明家屋后刚开挖了一口深井,学了化学后,他知道长期饮用硬水会对健康有害。下列方法中,能鉴别井水是否为硬水的是 。
A.过滤 B.煮沸 C.吸附 D.加肥皂水
(3) 过滤操作可以除去水中难溶性的固体杂质,过滤操作中需用到的玻璃仪器有 、
和烧杯。
(4)右图是某些国家的人均水量和世界人均水量(m3/人) 。
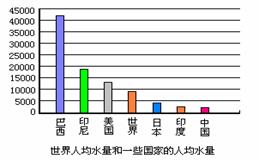 由图中可以看出我国是一个水资源_________的国家。
由图中可以看出我国是一个水资源_________的国家。
举出你在生活中节约用水的两点做法:
①_____________________________;② 。
25.(5分) A-D都是初中化学中的常见物质,且有如图所示转化关系(部分反应条件已略去)。
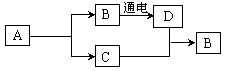
⑴请写出下列物质的化学式:
A ; B ; C ; D 。
⑵请写出上述转化关系中涉及到的分解反应的一个化学方程式_ 。
24.(5分) 有人将核电荷数为1-18的元素排成了如下形式,请你分析表中各元素的原子结构后,将得出的结论填写在横线上:
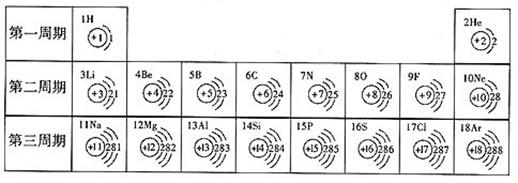
⑴原子序数为17的元素名称是 ,在化学反应中,该元素的原子容易 (填“得”或“失”)电子;原子序数为13的元素属于 元素(填:“金属”或“非金属”)
⑵我发现如下规律:
①原子序数与元素原子核电荷数在数值上相等:
②
③
23.(3分)下表是某市场销售的一种“加碘食盐”包装袋上的文字说明:
|
配料 |
含碘量 |
保质期 |
食用方法 |
储藏指南 |
|
氯化钠 碘酸钾 |
(20mg
~ 40mg)/Kg |
18个月 |
不要长时间炖炒 |
避热、避 光、密封 |
⑴该“加碘食盐”属于(填序号)___________
① 纯净物 ② 混合物 ③ 单质 ③ 氧化物 ⑤化合物
⑵写出碘酸钾中所含有的金属元素的元素符号 。
⑶由食用方法和储藏指南可推测碘酸钾的化学性质之一是 。
22.(5分) 食品保鲜可以防止食品腐坏,保持食品的营养和味道。食品保鲜的措施有添加防腐剂、充填气体、放置干燥剂和脱氧保鲜剂等。
⑴包装熟食制品常加入防腐剂。丙酸钠是一种食品防腐剂,化学式为C3H5O2Na,丙酸钠是由
种元素组成,每个分子中含有 个原子,其相对分子质量为 ;
⑵小包装糕点类食品常采用充气包装,氮气是常用的填充气体。请你根据氮气的性质写出选用氮气的主要原因是 ;
⑶生石灰和硅胶(主要成分是二氧化硅)是常用的干燥剂。二氧化硅的化学式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com