
题目列表(包括答案和解析)
1、下列各变化属于物理变化的是
A、用稀盐酸除去金属表面的铁锈 B、盐酸使指示剂变色
C、用小木棍蘸少量浓硫酸,小木棍逐渐变为黑色
D、浓盐酸在空气里敞口放置瓶口有白雾生成
30.实验室有一瓶久置的NaOH,称取13.3g 的NaOH样品(杂质为Na2CO3)于烧杯中,然后向烧杯中逐滴加入质量分数19.6%的稀硫酸,反应情况如图所示。
(1)试计算:
① 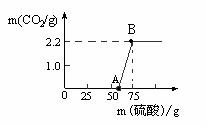 该样品中Na2CO3的质量为多少?
该样品中Na2CO3的质量为多少?
②B点所对应的溶液中溶质的质量分数为多少?
(2)从图中0-A点说明:在NaOH 与Na2CO3的混合溶液中,加入强酸,首先反应的物质是 ;②根据反应方程式分析,NaOH部分变质或全部变质,与没有变质的NaOH相比,中和反应时消耗强酸的量 (填“相等”、“不相等”或“无法确定”)。
29.(6分)2008年5月12日2点28分,我国四川省汶川等地区发生了里氏8级地震,给人们的生命财产带来了巨大的灾难。为保证灾区一些农村人民的生活用水,需对河水进行净化处理。
(1)从外观看,无色、澄清、透明的水是否一定可作饮用水?说明理由。
(2)净水时使用明矾的作用 。
(3)人们常用 方法将取用的浑浊的河水变澄清,在常用的净水措施中,
净化程度最高。
(4)请利用矿泉水瓶、小卵石、石英砂、活性炭、棉花、纱布等物质设计一个简易的净水装置(可图示)。
28.(6分)下图所示的是有关物质相互转化的关系图,其中A是一种金属氧化物,G是红褐色沉淀,I 的溶液呈浅绿色。
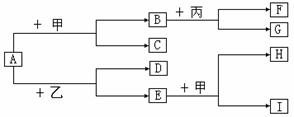
根据关系图回答:
(1)若F是由Na+和Cl-组成的溶液,则:①甲是 (填名称);
②B+丙→F+G: ,该反应属于 反应。
(2)若D是能使澄清石灰水变浑浊的气体,则:①乙可能是 或 ;
②I是 (填化学式)溶液。
27、(7分)某实验小组的四位同学在探究碱的性质时发现氢氧化钠、氢氧化钙等可溶性碱都能使酚酞试液变红。他们想进一步探究:不溶性的氢氧化镁是否也能使酚酞试液变红。为此,他们将适量的氢氧化镁加入到盛有热水的烧杯中搅拌,然后向浑浊的液体中滴加酚酞试液,发现酚酞试液变红,可是过一会儿红色又消失了。
[提出问题]上述酚酞试液变红、红色又消失的原因是什么?
[作出猜想]小明:可能是个偶然现象。
小东:可能是浑浊液中的固体氢氧化镁使酚酞试液变红,氢氧化镁沉降后溶液就变无色了。
小花:可能是酚酞试液与空气中的氧气反应,使红色消失;也可能是氢氧化镁溶液与空气
中的二氧化碳反应的缘故。
小红:可能是在热水中氢氧化镁的溶解度大,溶液中OH一离子较多,使酚酞试液变红;过一会儿温度降低,氢氧化镁的溶解度减小,溶液中OH一离子变少,酚酞试液又变无色。
[讨论交流]
(1)对小明猜想“是个偶然现象”,四位同学都认为可以用科学探究的一般方法排除偶然现象。他们的方法是: 。
(2)小花认为小东的猜想不正确,她从碱使酚酞试液变色的原因上给予了否定:
。
[实验验证]
(1)四位同学讨论后认为要验证小花的猜想,还需做如下实验,你知道其实验的目的吗?
|
实验步骤 |
设计目的 |
|
将氢氧化镁加入到热水中搅拌,滴入酚酞试液,并在上方滴一些植物油。 |
|
(2)小红设计了如下对比实验方案证明自己的猜想,请将其方案补充完整。
|
实验方法 |
可能观察到的现象 |
结论 |
|
|
|
红色消失与氢氧化镁的溶解度随温度降低而减小有关 |
[反思提高]将氢氧化镁加入到热水中搅拌,所得溶液的pH 7(填“<”、“>”、“=”);冷却后pH 。(填“变大”、“变小”或“不变”)
26、(10分)现有如图所示的下列实验装置。回答问题:
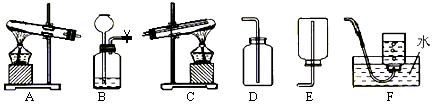
(1)检验B装置气密性方法是
。
(2)如果用高锰酸钾来制取干燥的氧气,反应方程式为 ;可选用的发生装置和收集装置是_ (填写序号)。
(3)质量分数为3%的医用双氧水在常温下难分解;但在双氧水溶液中加入铁锈,就会迅速分解且反应结束后过滤出的铁锈可重复使用。试写出该反应的化学方程式 ,选择气体发生装置的依据是 、 。
(4)某化学研究小组的同学欲对某种塑料袋的组成进行分析探究(资料显示该塑料只含C、H
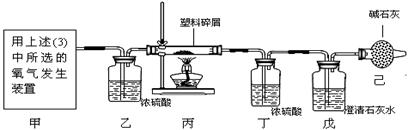 两种元素),他们设计了如下图所示的实验装置,使该塑料试样在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量。
两种元素),他们设计了如下图所示的实验装置,使该塑料试样在纯氧中燃烧,观察实验现象,分析有关数据,推算元素含量。
①仪器乙的作用是 ,仪器戊中的现象是 。
②若仪器丙玻璃管中放入塑料试样为Wg,塑料试样充分燃烧后,仪器丁增重ag,则Wg该塑料试样中含氢元素的质量为 g(计算结果用分数形式表示)。若装置中没有连接仪器乙,将使该塑料试样中氢元素的质量测算结果 (填“偏小”“偏大”、“无影响”)。
25. (5分)下图是配制一定质量分数的NaCl溶液的操作过程。请回答下列问题:
(5分)下图是配制一定质量分数的NaCl溶液的操作过程。请回答下列问题:
(1)指出图中a、b两种仪器的名称:a ,b 。
(2)写出图中的两处错误操作 、 。
(3)步骤⑤的操作是搅拌,其操作要领是 。
24.(5分)元素周期表是化学和研究化学的重要工具,它的内容十分丰富,下图是依据元素周期表画出的1~18号元素的原子结构示意图。请对它进行探究:
|
第一周期 |
1 H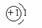 |
|
|
|
|
|
|
2 He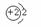 |
|
第二周期 |
3 Li |
4 Be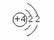 |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne |
|
第三周期 |
11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar |
(1)原子序数为17的元素名称是_______,在化学反应中,该元素的原子容易_____(填“得”或“失”)电子;原子序数为13的元素属于________元素(填“金属”或“非金属”)。
(2)请从上表中总结出一条原子排布的规律 。
(3)研究表明:第二周期从3号到9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力增大,故原子半径逐渐减小。请判断:钠原子半径_____镁原子半径(填“﹤”或“﹥”或“﹦”)。
23、(5分)九年级化学课学完后,实验学校化学兴趣小组学生对“金属活动性顺序”从内容、规律以及应用等方面进行了总结。请你认真填写下列空白:
(1)金属活动性顺序表:K Ca Na Al Zn Fe Sn Pb (H) Hg Ag Pt Au
(2)举出一个金属与酸反应的例子(用化学方程式表示)
(3)金属与盐发生置换反应,必须至少符合以下两点:
①K Ca Na三种金属非常活泼,不能将金属直接从其盐溶液中置换出来;
② 。
(3)写出一个有铜盐生成的反应的化学方程式 。
22、(4分) 体现“绿色奥运、科技奥运、人文奥运”三大理念的2008年北京奥运会,正快步向我们走来。
 (1)“祥云”火炬燃料为丙烷,丙烷在空气中完全燃烧后的产物是CO2和H2O,对环境没有污染。丙烷完全燃烧的化学方程式是
。
(1)“祥云”火炬燃料为丙烷,丙烷在空气中完全燃烧后的产物是CO2和H2O,对环境没有污染。丙烷完全燃烧的化学方程式是
。
(2)今年5月8日,奥运圣火成功登上的世界最高峰珠穆朗玛峰,5月23日奥运
圣火的传递将到达泰州。从燃烧条件考虑,“祥云”火炬在珠峰传递时比在泰州
传递时,应 (填“调大”或“调小”)火炬燃烧室里空气的进入量,
在强风下火炬不会熄灭的原因是 。
(3)作为北京奥运会主场馆的“鸟巢”是当今世界上最大的环保型体育场。在这里将采用绿色能源--太阳能光伏发电系统为整个场馆提供电力,用太阳能光伏发电系统发电时的能量转换是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com