
题目列表(包括答案和解析)
2.将两个枝条分别置于营养液中。其中一枝仅保留一张叶片(甲),另一枝保留两张叶片(乙、
丙),叶片置玻璃盒中密封(玻璃盒大小足以保证实验顺利进行),在甲叶和乙叶的盒中注
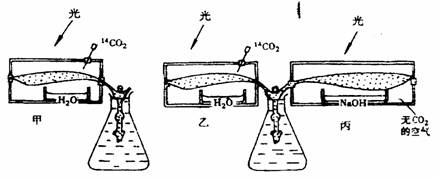 入14CO2,装置如图。照光一段时间后,可以检测到放射性的叶片 ( )
入14CO2,装置如图。照光一段时间后,可以检测到放射性的叶片 ( )
A.仅在甲中 B.仅在甲和乙中
C.仅在甲和丙中 D.在甲、乙和丙中
1.下列关于细菌代谢的叙述中,正确的是 ( )
A.细菌没有细胞器,只能进行无氧呼吸
B.细菌的蛋白质合成在自身的核糖体上进行
C.细菌的代谢产物全是CO2和H2O
D.细菌的储藏颗粒为蛋白质、淀粉、脂肪
31.(1) ,
, 。
。
(2) ;qE=mg;
;qE=mg;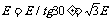 ;方向竖直向上。
;方向竖直向上。
(3)qvB=mv2/R。R=mv/qB; ;粒子与y轴交于p点,
;粒子与y轴交于p点,
 。粒子轨迹所对的圆心角为120°,t
= Mp/V + T/3。
。粒子轨迹所对的圆心角为120°,t
= Mp/V + T/3。
由(2)可知: 。
。 。
。
30.(15分,每空3分)
(1)B。(2)750;9.5。(3)9.5;50。
29.(18分)
(1)设C球与B球粘结成D球时,D的速度为v1,由动量守恒,有mv0=2mv1。
当弹簧压至最短时,D与A的速度相等,设此速度为v2,由动量守恒,有2mv1=3mv2,由以上两式得A的速度 v2=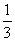 v0。
v0。
(2)设弹簧长度被锁定后,贮存在弹簧中的势能为Ep,由机械能守恒,有:
 ×2mv12=
×2mv12= 3mv22+Ep。
3mv22+Ep。
撞击P点后,A与D的动能都为零。解除锁定后,当弹簧刚恢复到自然长度时,势能全部转化成D的动能,设D的速度为V3。则有EP= (2m)v32,以后弹簧伸长。A球离开挡板P,并获得速度。当A、D的速度相等时,弹簧伸至最长。设此时的速度为v4,由动量守恒有2mv3=3mv4,当弹簧伸至最长时,其势能最大,设此势能为EP1,由机械能守恒有
(2m)v32,以后弹簧伸长。A球离开挡板P,并获得速度。当A、D的速度相等时,弹簧伸至最长。设此时的速度为v4,由动量守恒有2mv3=3mv4,当弹簧伸至最长时,其势能最大,设此势能为EP1,由机械能守恒有 ×2mv32=
×2mv32= 3mv42+Ep1,解以上各式得Ep1=
3mv42+Ep1,解以上各式得Ep1=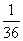 mv02。
mv02。
28.(16分)(1)木块A和滑板B均向左做初速为零的匀加速直线运动。


即
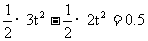 得t=1s
得t=1s
(2)1s末木块A和滑板B的速度分别为
VA=aAt=2×1=2m/s VA=aBt=3×1=3m/s
撤去外力F后,当木块A和滑板B的速度相同时,弹簧压缩量最大,具有最大弹性势能。
根据动量守恒守律,得mvA+MVB=(m+M)v。
得v=2.8m/s。
由能量守恒定律  。
。
 =0.4J。
=0.4J。
27.(19分,第一问4分,其余每空3分)
实验目的是“证明A装置中产生的气体成分”。在氯化铵溶液中加入金属钠,反应后会产生NH3、H2两种成分,所以实验要求证明的气体是氨气和氢气两种。
(1)由于氨气、氢气两种物质都能跟氧化铜反应,所以实验设计中要特别注意这一点。根
据氨和氢气的性质,可以用石蕊试纸来检验氨气,用灼热的氧化铜检验氢气。为了防止
氨气对检验氢气的干扰,就先检验氨气,再把过量的氨气吸收完后,最后检验氢气。所
以装置的连接顺序应为:A→C→D→C→B。
(2)D装置中应盛装浓硫酸,用于吸收过量的氨气。
(3)第一个装置C是用来检验是否有氨气;第二个装置C是用于检验氨气是否已被完全吸
收。
(4)检验是否有氢气生成。
2.11molNaOH与Cu(NO3)2 反应消耗掉,故固体酒精碱性很低。(5分)
(3)固体酒精是由硬脂酸钠、NaNO3、Cu(OH)2和乙醇组成,点燃后有的燃烧,有的分解,
所以残渣由CuO、NaNO2、Na2CO3组成。(4分)
(4)加入硝酸铜的目的,一是反应掉剩余的NaOH,二是生成的NaNO3和剩余的Cu(NO3)2 在
高温下具有强氧化性,能充分氧化硬脂酸钠,使固体酒精燃烧充分。(4分)
26.(16分)
(1)乙醇中含有极性基团-OH,是极性分子,NaOH是离子化合物,据相似相溶原理,
NaOH可溶于酒精溶液中。(3分)
(2)n(NaOH)=1000g/40g.mol-1=25mol,n(硬脂酸)=6.6×103g/284g.mol-1=22.89mol,
n[Cu(NO3)2]=0.5×103g/188g.mol-1=2.66mol。中和硬脂酸需NaOH为 22.89mol,剩下的
25.(15分)
(1)AlN跟氢氧化钠溶液反应,生成NaAlO2、并放出NH3,反应方程式为:
AlN+NaOH+H2O = NaAlO2+NH3↑(4分)
生成0.15molNH3,可计算出10.00g样品中含有AlN的质量为6.15g,所以AlN的质量分数为61.5%。(5分)
(2)加入氧气的物质的量为: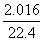 =0.09mol
=0.09mol
高温下2.016L(标准状况)O2充分反应,产物可能CO2和CO的混合气体。根据气体产物的密度可计算出气体产物的平均相对分子质量为30。设混合气体中含有CO2xmol,CO ymol,根据氧原子守恒和平均相对分子质量的计算方法可得出:
2x+y=0.18 44x+28y=30(x+y)
解得:x=0.02,y=0.14 。所以,样品中C的质量为:(0.02+0.14)×12 = 1.92g。(6分)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com