
题目列表(包括答案和解析)
5.(07文综)下表是“2002 一2006年我国城乡居民家庭思格尔系数情况”。根据材料,针对这段时期,下列说法正确的是
|
项目
年份 |
2002年 |
2003年 |
2004年 |
2005年 |
2006年 |
|
城镇居民家庭恩格尔系数(%) |
37.7 |
37.1 |
37.7 |
36.7 |
35.8 |
|
农村居民家庭恩格尔系数(%) |
46.2 |
45.6 |
47.2 |
45.5 |
43.0 |
A.城乡居民生活水平总体呈下降趋势 B.城乡居民生活水平总体呈上升趋势 C.城镇居民生活水平不断提高,农村居民生活水平不断下降
D.农村居民生活水平不断提高,城镇居民生活水平不断下降
4.(07文综)在同一时空条件下,生产同样的商品,不同生产者有的赚钱有的赔钱,其根本原因在于
A.生产技术条件不同 B.所耗费的个别劳动时间不同
C.出售产品的价格不同 D.所耗费的社会必要劳动时间不同
3.(07文综)气候、时间、地域、宗教信仰、习俗等因素的变化,都会引起商品价格的变动。它们对商品价格的影响,是因为改变了
A.该商品的供求关系 B.该商品的价值量 C.该商品的个别劳动生产率 D.该商品的社会劳动生产率
2.(07文综)货币在商品流通中起着重要作用。下列对于货币的正确认识是
A.货币只有流通手段的职能 B.货币就是金银,金银就是货币
C.有商品交换,就有货币 D.货币能表现一切商品的价值
1、(07理综)价值、价格和供求关系之间存在着密切联系,下列认识正确的是
A、价格决定价值,供求关系影响价格
B、供求关系决定价值,价格影响价值
C、价值决定价格,价格决定供求关系
D、价值决定价格,价格与供求关系相互影响
29.(15分)过氧化氢(H2O2)又称双氧水,常温下它是一种液体,它难电离,且易分解。随着社会需求的增长,尤其是生态环境保护的需要,过氧化氢近年来更受到人们的青昧,并称其为绿色氧化剂。为了贮存、运输、使用的方便,工业上采用“醇析法”将其转化成固态的过碳酸钠晶体(其化学式为2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。
根据上述材料,回答下列问题:
(1)依据你已有的知识,写出H2O2的结构式_______________________。你认为H2O2被称为绿色氧化剂的主要原因是:__________________________。
(2)S2Cl2的分子结构与H2O2类似,电子式为 ,属 分子(填极性或非极性)。
(3)H2O2是一种二元弱酸,其电离方程式为:
它与过量的Ba(OH)2反应的化学方程式为:________________________________。
(4)H2O2还有一定的还原性,能使酸性KMnO4溶液褪色,其离子反应方程式为 。
(5)我们知道,稀硫酸不与铜反应,但在稀硫酸中加人H2O2后,则可使铜顺利溶解,写出该反应的离子方程式:___________________________________。
(6)下列物质不会使过碳酸钠失效的是____________。
A.MnO2 B.H2S C.CH3COOH D.NaHCO3
30(20分).下表是科研人员在农田所做的三组水稻杂交实验的统计数据(D和d表示水稻株高的显、隐性基因,T和t表示抗性的显、隐性基因)。据表回答以下问题:
|
|
亲本组合 |
F1表现型和株数 |
|||
|
组别 |
表现型 |
高茎抗病 |
高茎易染病 |
矮茎抗病 |
矮茎易染病 |
|
甲 |
高茎抗病×矮茎抗病 |
627 |
203 |
617 |
212 |
|
乙 |
高茎抗病×矮茎易染病 |
724 |
0 |
0 |
0 |
|
丙 |
高茎易染病×矮茎抗病 |
517 |
523 |
499 |
507 |
⑴获得纯合矮茎抗病个体比例最大的杂交组合是 ,亲本的基因型是
⑵要通过乙组合尽快获得能稳定遗传的矮茎抗病水稻,应怎样育种?
⑶已知水稻(雌雄同株植物)体细胞有24条染色体,则我国进行水稻基因组计划时需测
个DNA分子上的碱基。
⑷科学家设想把圆褐固氮菌的固氮基因转到小麦根系的微生物中,获取圆褐固氮菌固氮的基因最常用 法;运载固氮基因的工具可以是 ;在形成重组DNA的过程中,能使两条DNA分子末端之间缝隙相互连接的物质是 。如果这一重组能够实现,欲检测固氮基因是否能表达,可以将转基因微生物培养在 培养基上,观察其是否能够生存。
⑸水稻正常植株叶片为绿色,患某种遗传病后植株的叶片具有白色斑,或为不能成活的白化苗。显微观察发现,白化苗和白色斑处的叶肉细胞不含叶绿体。为了探索该病的遗传机理,用人工授粉的方法进行了如下实验:
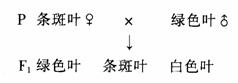
重复多次该实验,后代的性状不出现一定的分离比。
分析实验结果可知该病的遗传方式是 。此实验的后代中不同性状的个体的比例是随机的,其原因是在减数分裂形成卵细胞时 。
31(22分).下表所示为某微生物培养基的配方,请回答:
|
成分 |
NaNO3 |
K2HPO4 |
KCl |
MgSO4·7H2O |
|
含量 |
3g |
1g |
0.5g |
0.5g |
|
成分 |
FeSO4 |
(CH2O) |
H2O |
青霉素 |
|
含量 |
0.01g |
20g |
1000mL |
0.1万单位 |
⑴依物理性质划分,该培养基属于 培养基;依用途划分,则属于 培养基。
⑵依培养基的成分,所培养微生物的同化作用类型是 ,培养的微生物可能是
⑶该培养基中的碳源是 生长因子(填“有”或“无”)
⑷如要鉴定自来水中的大肠杆茵是否超标,至少要加入 、 和 ,除去 。
⑸.若将细菌置于适宜的营养基上,它会繁殖并形成细菌菌落。如图所示,用哪项适当的实验可以用来检验两种抗生素的杀菌作用 ( )
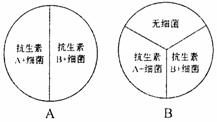
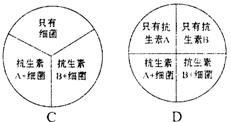
28.(14分)A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和X均可形成10个电子化合物;B与Z的最外层电子数之比2:3,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红。请回答下列问题。
(1)Z的原子结构示意图为 ;化合物BA4的电子式为 。
(2)化合物Y2X2中含有的化学键类型有 (填序号)。
A.离子键 B.极性共价键 C.非极性共价键 D.氢键
(3)化合物A2X和A2Z中,沸点较高的是 (填化学式),其主要原因是 。
(4)A与X和A与Z均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为 。
(5)常温常压下,由A、B、X可组成的液态物质甲。现有2.3g甲与足量的X的单质充分反应,生成标准状况下2.24L的BX2气体和2.7g的A2X液体,同时放出68.35kJ的热量,该反应的热化学方程式为: 。
27.(20分)D、E、X、Y、Z是周期表中的前20号元素,且原子序数逐渐增大,它们的最简单氢化物分子的空间结构依次是正四面体、三角锥形、正四面体、角形(V形)、直线型,回答下列问题:
(1)Y的最高价氧化物的化学式为______________。
(2)上述5种元素中,能形成酸性最强的含氧酸的元素是____________(填元素符号),写出该元素的任意3种含氧酸的化学式:_______________________。
(3)D和Y形成的化合物,其分子的空间构型为________________。
(4)D和X形成的化合物,其化学键类型属_______________,其晶体类型属________。
(5)金属镁和E的单质在高温下反应得到的产物是__________,此产物与水反应生成两种碱,该反应的化学方程式是___________________________。
(6)试比较D和X的最高价氧化物熔点的高低,并说明理由: 。
26.(本题共11分)
I.(3分)下列有关实验的叙述中,正确的是 (填序号)。
①将浓盐酸逐滴滴入装有浓硫酸的烧瓶中,可以制取HCl气体。
②配制一定物质的量浓度的NaCl溶液时,定容后摇匀,发现液面又低于刻度线,此时须再加入蒸馏水至刻线
③配置100 mL 1.00mol/L的NaCl溶液时,可用托盘天平称取5.85 gNaCl固体。
④用小刀切取少量金属钠做实验,切剩的钠要立即放入原试剂瓶。
⑤分液漏斗分液时,先将下层的液体从下口流出,然后再从下口流出上层的液体
⑥测定某溶液pH时,取一小块干燥的试纸放入玻璃片上,用玻璃棒蘸取溶液滴在试纸的中部,再与标准比色卡对比
⑦向试管中滴加液体时,为不使液体滴到试管外应将胶头滴管伸入试管中;
⑧测硫酸铜晶体中结晶水的含量至少需要称量3次
II.(8分)Na2CO3是一种很重要的化学物质,某中学某学生拟在实验室中用NaOH制备Na2CO3溶液。下面是他的制备实验过程:
用50mL NaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入的CO2气体过量,生成NaHCO3,他设计了如下实验步骤:①用25mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;②小心煮沸溶液1-2分钟;③在得到的溶液中加入另一半(25mL)NaOH溶液,使溶液充分混合。
(1)在步骤①中,刚通入CO2时发生反应的离子方程式是 ;而后又发生反应的离子方程式是 。
(2)步骤②中煮沸溶液的目的是 。
(3)步骤③中反应的离子方程式是 。
22.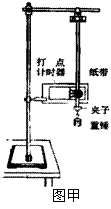 (18分)用如图甲所示的实验装置验证机械能守恒定律。实验所用的电源为学生电源,输出电压为6V的交流电和直流电两种。重锤从高处由静止开始落下,重锤上拖着的纸带通过打点计时器打出一系列的点,对纸带上的点的痕迹进行测量,即可验证机械能守恒定律。
(18分)用如图甲所示的实验装置验证机械能守恒定律。实验所用的电源为学生电源,输出电压为6V的交流电和直流电两种。重锤从高处由静止开始落下,重锤上拖着的纸带通过打点计时器打出一系列的点,对纸带上的点的痕迹进行测量,即可验证机械能守恒定律。
(1)下面列举了该实验的几个操作步骤:
A.按照图示的装置安装器件;
B.将打点计时器接到电源的直流输出端上;
C.用天平测量出重锤的质量;
D.释放悬挂纸带的夹子,同时接通电源开关打出一条纸带;
E.测量打出的纸带上某些点之间的距离;
F.根据测量的结果计算重锤下落过程中减少的重力势能是否等于增加的动能。
上述步骤中没有必要进行的或者操作不恰当的步骤是: 。(填字母代号)
(2)如图乙所示为实验中选出的一条符合要求的纸带,O点为重物开始下落的起点,选取纸带上打出的连续五个点A、B、C、D、E,测出A点距起始点O的距离为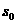 ,点A、C间的距离为s1,点C、E间的距离为s2,使用交流电的频率为f,则
,点A、C间的距离为s1,点C、E间的距离为s2,使用交流电的频率为f,则
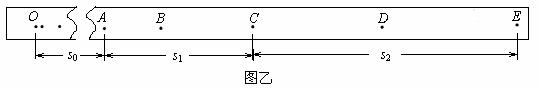
①打点计时器打C点时重锤的速度为
②如果验证重锤从O下落到C过程是否满足机械能守恒,请写出此过程验证机械能守恒的验证等式:
③根据打出的纸带计算重锤下落的加速度a的表达式为:a=_________________。
④在验证机械能守恒定律的实验中发现,重锤减小的重力势能总是大于重锤动能的增加,其原因主要是因为在重锤下落过程中存在着阻力的作用。已知当地重力加速度公认的较准确的值为g,若要计算出该实验过程中重锤受到阻力的大小,还需要测量的物理量是___________。试用这些物理量和纸带上的测量数据表示出重锤在下落的过程中受到的平均阻力大小为F= 。
23(16分).2007年10月24日18时05分,中国第一颗探月卫星“嫦娥一号”在西昌卫星发射中心成功升空,“嫦娥奔月”成为中国航天的现实. 为了方便研究,我们将“嫦娥奔月”的过程简化为:“嫦娥一号”升空后,首先进入近地圆轨道(其轨道半径近似等于地球半径),运行周期为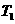 ,然后在地面的指令下经过一系列的变轨后最终被月球捕获,在距离月球表面为
,然后在地面的指令下经过一系列的变轨后最终被月球捕获,在距离月球表面为 的轨道上绕月球做匀速圆周运动. 已知地球半径为
的轨道上绕月球做匀速圆周运动. 已知地球半径为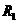 ,月球半径为
,月球半径为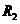 ,月球质量为M,万有引力常量为G,求:
,月球质量为M,万有引力常量为G,求:
(1)“嫦娥一号”绕月球运动时的周期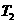
(2)月球与地球表面的重力加速度之比
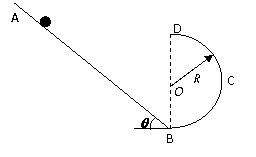 24(18分).如图所示有一固定在竖直平面内的轨道ABCD,AB段为表面光滑倾角为
24(18分).如图所示有一固定在竖直平面内的轨道ABCD,AB段为表面光滑倾角为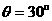 的直轨道,BCD部分为内表面粗糙的半圆轨道,B为半圆轨的最低点,D为最高点,轨道半径为R.现在直轨道上某一位置静止释放一个质量为
的直轨道,BCD部分为内表面粗糙的半圆轨道,B为半圆轨的最低点,D为最高点,轨道半径为R.现在直轨道上某一位置静止释放一个质量为 的小球,小球沿ABCD轨道运动,经过B点时对轨道的压力为6mg,从D点飞出后又落在AB轨道上,其落点与半圆轨的圆心O等高,忽略空气阻力,求:
的小球,小球沿ABCD轨道运动,经过B点时对轨道的压力为6mg,从D点飞出后又落在AB轨道上,其落点与半圆轨的圆心O等高,忽略空气阻力,求:
(1)释放小球的位置距离B点的竖直高度
(2)小球沿BCD轨道从B点运动到D点过程中克服摩擦力所做的功。
 (2)加工一块铁板过程中电动机做功的平均功率为多大?(不考虑电动机自身的能耗)
(2)加工一块铁板过程中电动机做功的平均功率为多大?(不考虑电动机自身的能耗)

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com