
题目列表(包括答案和解析)
2.某含铁盐溶液能够在高浓度的碱性环境下长期稳定存在,且具有较强的灭菌消毒功能,该盐是一种绿色、无污染的净水剂,其化学式为Na2FeO3 。则其中铁元素的化合价是( )
(A)+2 (B)+3 (C)+4 (D)+6
1.下列变化属于化学变化的是( )
(A)潮湿的衣服经太阳晒,变干了
(B)寒冷的冬天在玻璃窗前呼吸,玻璃上出现一层水雾
(C)铜在潮湿的空气里生成铜绿
(D)下雪天把一团雪放在温暖的房间里,雪融化
6.其他单质、氧化物、酸、碱、盐的除杂方法:
|
操作方法 |
示
例 |
|||||
|
物 理 方 法 |
过滤法 |
粗盐提纯(只除去不溶性杂质)、Na2CO3(可溶)与CaCO3(不溶)混合物分离 |
||||
|
结晶法 |
粗盐提纯实验中滤液蒸发得NaCl晶体--[蒸发结晶] NaCl与KNO3混合物的分离------[降温结晶:KNO3析出] |
|||||
|
磁吸法 |
分离铁粉与铜粉的混合物[铁粉被磁铁吸引,铜粉未被吸引] |
|||||
|
化 学 方 法 |
沉淀法 |
除去NaCl中混有的Na2SO4:[加BaCl2溶液]Na2SO4+BaCl2=BaSO4↓+2NaCl KNO3(KCl)[加AgNO3溶液]:KCl+AgNO3= AgCl↓+KNO3 [转化] |
||||
|
气化法 |
除去NaCl中混有的Na2CO3:[加稀HCl溶液] [转化] Na2CO3+2HCl=2NaCl+H2O+CO2↑ NaCl(NH4Cl):[加NaOH溶液]NH4Cl+NaOH= NaCl+NH3↑+H2O |
|||||
|
置换法 |
除去FeSO4中混有的CuSO4:[加Fe粉]CuSO4+Fe=FeSO4+Cu[转化] |
|||||
|
吸收法 |
除去CO中混有的少量CO2:[通过NaOH溶液]2NaOH+CO2 = Na2CO3+H2O [CO2(CO):[通过灼热的CuO] CuO+CO △Cu+CO2] [转化] |
|||||
|
加热法 |
除去CaO中混有的CaCO3:[高温]CaCO3
高温 CaO+CO2↑ [转化] |
|||||
|
溶解法 |
BaSO4(CaCO3)[加稀盐酸碳酸钙溶解,然后过滤];
[转化] Cu(CuO)[加酸或通足量CO加热]; Cu(Zn)[加酸或CuSO4溶液后过滤] |
|||||
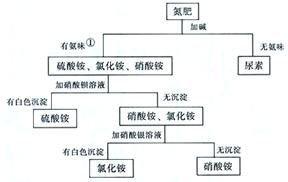
7.化肥的检验 |
 |
|||||
|
8.氢氧化钠的变质探究: 验证已经变质:加足量稀盐酸--有气泡冒出。 验证部分变质:加足量CaCl2溶液后,用石蕊(变蓝)或酚酞(变红)或pH试纸(pH大于7)。 除去变质生成的Na2CO3:溶解后,滴加Ca(OH)2溶液至无沉淀产生,然后过滤、蒸发。 |
||||||
|
植物缺乏氮肥:叶片发黄。缺乏磷肥:植株特别矮小。缺乏钾肥:易倒伏,叶片的边缘和尖端呈褐色 |
||||||
|
9.尾气处理装置:有CO生成或参加的反应如下: CO2与C--黑粉消失;CO与CuO--黑变红;CO与Fe2O3--红变黑。 尾气中CO的处理方法:用酒精灯点燃或用气球收集或用排水法收集。 |
||||||
|
10.电解水装置:通电后,电极上出现气泡,一段时间后试管1(O2)和试管2(H2)中所收集的气体体积比约为1∶2。 [负氢] [O2、H2的质量比为8∶1。] 结论:水由氢、氧两种元素组成;在化学反应中分子可分,原子不可分。 |
 |
|||||
|
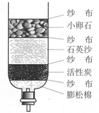
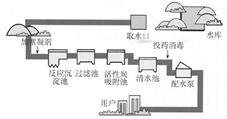
11.净化水装置及多种方法: 自来水厂:取、沉淀、过滤、吸附、消毒、供 明矾:胶状物→小颗粒聚集→大颗粒沉降。 活性炭:有吸附性,起脱色去味作用。 蒸馏:净化程度最高。[蒸馏水可视为纯水] 上述净化水的方法中,只有蒸馏能使硬水软化。 |
  |
|||||
|
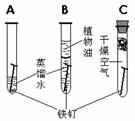
12.铁(铜)生锈实验、防锈方法: ⑴探究铁生锈条件:A:Fe、O2、H2O;B:Fe、H2O;C:Fe、O2。 防锈:洁净干燥、涂油、喷漆、镀其他金属、烤蓝、制成合金。[资源保护] ⑵铜生锈的条件:铜、氧气、水、二氧化碳四种物质共同作用。 如何探究铜生锈的条件?[可做七个对比实验][铁生锈做三个对比实验] |
 |
|||||
|
12.模拟炼铁:验纯后[防爆],通CO、加热[防爆],停止加热、继续通CO至冷却。[尾气处理] |
||||||
计算题
|
1.盛不同药品的装置的总质量的变化: 甲--无水硫酸铜或无水氯化钙--吸收H2O质量增加 甲--碱石灰--吸H2O或吸收CO2或同时吸收H2O和CO2增 乙--氧化铜或氧化铁--通过H2或CO后失去氧元素质量减少 乙--氧化铜和碳粉--释放CO2质量减少 丙--氢氧化钠溶液--吸收CO2质量增加 丙--浓硫酸--吸收H2O质量增加 |
   |
|
2.不同物质混合后总质量的变化:氢氧化钠溶液吸收CO2--质量增加、碳酸钙高温分解释放CO2--质量减小、铁合金遇酸以及黄铜(铜锌合金)遇酸释放H2--质量减小、石灰石或大理石或碳酸钠遇酸释放CO2--质量减小、过氧化氢与二氧化锰混合释放O2--质量减小 |
|
3.计算公式: 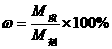 ; M质=M液×w; M=ρ×V; M质=ρ×V×w; M纯=M混×w。 ; M质=M液×w; M=ρ×V; M质=ρ×V×w; M纯=M混×w。 |
7.我国使用的燃料主要是煤炭和石油。含有硫的煤炭燃烧时排放出污染空气的有毒气体主要是SO2,它遇到雨水成为酸雨降落到地面会带来很大危害,请回答下列问题:
(1)请举出三个方面的危害实例:
① ,② ,③ ;
(2)许多植物有抗御污染空气的有毒气体的能力,在常见植物中对这些气体有较强的吸附能力的是 (填写植物名称);
(3)当SO2污染严重时,目前有一种有效的方法,即用直升机喷洒碳酸钙粉末,脱硫效果可达85%,其化学方程式为:2CaCO3+2SO2+O2==2CaSO4+2CO2。实验证明石灰浆[Ca(OH)2]在空气中可吸收SO2生成CaSO4和其他物质,请写出该反应的化学方程式: 。
6.空气、水、天然气、石油和煤等自然资源对人类的生存、日常生活和工农业生产都有着极其广泛和重要的用途。请将与下列用途相对应的物质名称填在空白处:
(1)常用作溶剂的是 ;
(2)可用作生活燃料、并能通过管道长途输送的是 ;
(3)直接供给人和动物呼吸的是 ;
(4)可用于生产城市居民生活用管道煤气的是 ;
(5)是重要的化工原料而被称为“工业血液”的是 ;
(6)可用于获取充置霓虹灯的气体的是 。
5. “人类只有一个地球!”为了保护人类赖以生存的环境,下列做法中正确的是( )
A.回收垃圾,变废为宝
B.污水经处理就排放
C.扑杀、私卖野生动物
D.开发新能源,逐步减少使用化石燃料
4.下列说法不正确的是( )
A.太阳能、水能、风能是可持续发展的能源
B.煤、石油、天然气三种矿石燃料是永不枯竭的能源
C.地下水资源不能无限量地开发利用
D.大量排放SO2、NO2等气体,会形成酸雨
3.绿色化学实验是在绿色化学的思想指导下,对常规实验进行改革而形成的实验的新方法。它能极大地减少或消除实验中的“三废”、污染和浪费等。下列符合绿色化学实验的操作是( )
A.将一氧化碳还原氧化铜的尾气直接排入空气中
B.将锌和稀硫酸反应后的废液直接倒入下水道中
C.将跟氧气反应后剩余的硫磺放在空气里燃烧完
D.将氯酸钾和二氧化锰共热残余物回收分离
2.氢气是一种绿色能源,科学家们最新研制出利用太阳能产生激光、再用激光使海水分解得到H2的新技术,其中海水分解可用方程2H2O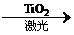 2H2↑+O2↑表示。下列说法不正确的是( )
2H2↑+O2↑表示。下列说法不正确的是( )
A.水分解产物不污染环境
B.TiO2是催化剂
C.该技术可将太阳能转化为氢能
D.在海水分解过程中应不断添加TiO2
1.一种新型绿色电池--燃料电池,是把H2、CO、CH4和空气不断输入,直接氧化,使化学能转变成电能,被称为21世纪的“绿色”发电站。这三种气体可以作为燃料的原因是( )
A.都是无毒无害的气体
B.都可以燃烧并放出大量的热
C.燃烧产物均为二氧化碳和水
D.均在自然界大量存在
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com