
题目列表(包括答案和解析)
26.(20分)A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中A,C及B,D分别是同一主族元素,B,D元素的原子核中质子数之和是A,C两元素原子核中质子数之和的两倍,又知四种元素的单质中有两种气体、两种固体。 (1)写出四种元素的名称: A_____________;B_____________;C_____________;D_____________; (2)写出两种均含A,B,C,D四种元素的化合物相互间发生反应,且有生成气体的离子方程式_____________________________________; (3)写出C、D两元素形成化合物的电子式:_____________________; (4)用A元素的单质和B元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的金属惰性电极浸入KOH溶液,两极均有特制的防止透过的隔膜,在一极通入A的单质,另一极通入B的单质,写出该电池发生的电极反应式: A______________________________;B________________________________。
25.(22分)2007年3月1日,国家重大科学工程项引"EAST超导托卡马克核聚变实验装置"在合肥顺利通过了国家发改委组织的国家竣工验收.作为核聚变研究的实验设备,EAST可为未来的聚变反应堆进行较深入的工程和物理方面的探索,其目的是建成一个核聚变反应堆,届时从l升海水中提取氢的同位素氘。在这里和氚发生完全的核聚变反应,释放可利用能量相当于燃烧300公升汽油所获得的能量.这就相当于人类为自己制造了一个小太阳。可以得到无穷尽的清洁能源.作为核聚变研究的实验设备,要持续发生热核反应,必须把温度高达几百万摄氏度以上的核材料约束在一定的空间内,约束的办法有多种.其中技术上相对较成熟的是用磁场约束核材料.
如图所示为EAST部分装置的简化模型:垂直纸面的有环形边界的匀强磁场b区域,围着磁感应强度为零的圆形a区域,a区域内的离子向各个方向运动。离子的速度只要不超过某值,就不能穿过环形磁场的外边界而逃逸,从而被约束.设离子质量为m,电荷量为q,环形磁场的内半径为 ,外半径
,外半径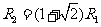 .
.
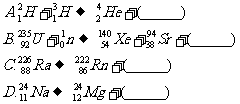
 (1)将下列核反应方程补充完整,指出哪个属于核聚变方程.并求出聚变过程中释
(1)将下列核反应方程补充完整,指出哪个属于核聚变方程.并求出聚变过程中释
放的核能  .已知
.已知  的质量为
的质量为 ,
,  的质量为
的质量为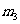 。
。 粒子的质量为
粒子的质量为
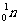 的质量为
的质量为 质子质量为
质子质量为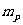 ,电子质量为
,电子质量为 ,光速为c
,光速为c
(2)若要使从a区域沿任何方向,速率为v 的离子射入磁场时都不能越出磁场的
外边界,则b区域磁场的磁感应强度至少为多大?
(3)若b区域内磁场的磁感应强度为B.离子从a区域中心o点沿半径OM方向
以某一速度射入b区域,恰好不越出磁场的外边界.请画出在该情况下离子在
a b区域内运动一个周期的轨迹,并求出周期.
24.(18分)水平固定的光滑U型金属框架宽为L,足够长,其上放一质量为m的金属棒ab,左端连接有一阻值为R的电阻(金属框架、金属棒及导线的电阻均可忽略不计),整个装置处在向下的匀强磁场中,磁感应强度大小为B。现给棒一个初速v0,使棒始终垂直框架并沿框架运动,
(1)金属棒从开始运动到达稳定状态的过程中求通过电阻R的电量和电阻R中产生的热量
(2)金属棒从开始运动到达稳定状态的过程中求棒通过的位移
(3)如果将U型金属框架左端的电阻R换为一电容为C的电容器,其他条件不变,如图所示。求金属棒从开始运动到达稳定状态时电容器的带电量和电容器所储存的能量(不计电路向外辐射的能量)

 (1)他们应选用下图所示的哪个电路进行实验?答:( )
(1)他们应选用下图所示的哪个电路进行实验?答:( )
(2)按照正确的电路图连接下图的实物图

(3)实验测得元件Z的电压与电流的关系如下表所示。根据表中数据,判断元件Z是金属材料还是半导体材料?答: 。
|
U(V) |
0 |
0.40 |
0.60 |
0.80 |
1.00 |
1.20 |
1.50 |
1.60 |
|
I(A) |
0 |
0.20 |
0.45 |
0.80 |
1.25 |
1.80 |
2.81 |
3.20 |
(4)把元件Z接入如下左图所示的电路中,当电阻R的阻值为R1 = 2Ω时,电流表的读数为1.25A;当电阻R的阻值为R2 = 3.6Ω时,电流表的读数为0.80A .结合上表数据,求出电池的电动势为 V,内阻为 _____________Ω.(不计电流表的内阻,结果保留两个有效数字)
(5)用螺旋测微器测得线状元件Z的直径如上右图所示,则元件Z的直径是 mm.

.
23.(16分)如图所示,质量M=1.0kg的木块随传送带一起以v=2.0m/s的速度向右匀速运动,木块与传送带间的动摩擦因数μ=0.5。当木块运动至最右端A点时,一颗质量m=20g的子弹以v0=3×102m/s水平向左的速度击穿木块,穿出木块时的速度v1=50m/s。设传送带的速度始终恒定,子弹击穿木块的时间极短,且不计木块质量变化,g=10m/s2。求:
⑴木块在被子弹击穿后,向左运动离A点的最大距离
⑵子弹击穿木块过程中系统损失的机械能
 ⑶从子弹击穿木块到最终木块相对传送带静止的过程中,木块与传送带间由于摩擦产生的内能
⑶从子弹击穿木块到最终木块相对传送带静止的过程中,木块与传送带间由于摩擦产生的内能
的实验装置,实验时两小球的质
量分别为m1和m2,半径为r1和r2,
则应满足m1______m2 , r1______r2 ,
(填“<”、“=”或“>”),某次实
验得出小球的落点情况如图,假设
碰撞动量守恒,则碰撞小球质量m1
和被碰小球质量m2之比
m1:m2=_______
|
(1)取3支试管并注入可溶性淀粉溶液2ml; (2)向各试管中加入1ml唾液; (3)将3支试管分别放在37℃的热水、沸水和冰块中;两支试管中的pH=6.8,一支试管中pH=2,摇匀后各自维持温度5min; (4)各试管滴加1滴斐林试剂; (5)观察实验现象。 |
(1)你认为该方案存在哪些问题?指出并加以纠正或补充。
(2)已知唾液中含有淀粉酶,淀粉酶可以催化淀粉的水解;又知鸡蛋被加热到65℃后会变性,但不知唾液淀粉酶被加热到65℃后是否影响其生物活性。为探究此问题,请依据所给材料和用具,设计相应的实验方案(以表格形式呈现实验步骤)并预测实验结果得出相应结论。
材料用具:稀释的唾液、稀释并煮熟的淀粉糊、碘酒、酒精灯或其他加热设备、试管若干、量筒、滴管、大烧杯、温度计等。
方法步骤(用表格的形式表示出来):
结果预测及结论:
① ;
② ;
③ 。
 2009年普通高等学校招生全国统一考试(南开中学模拟卷)
2009年普通高等学校招生全国统一考试(南开中学模拟卷)
(8分)
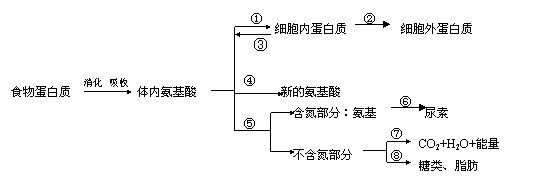
据图并结合你已有的生物学知识回答有关问题:
(1)动物冬眠后期形体消瘦,与此有关的蛋白质代谢过程主要是(填图中序号) 。
(2) 与①、②过程直接相关的细胞器依次: 。通过②过程到细胞外的蛋白质也有许多重要生理功能,如(答出两种功能蛋白质的名称和生理作用):① ;② 。
(3)肥胖者尽管不食油腻食物,仍然肥胖,与蛋白质代谢相关的可能原因
是: 。
(4)④过程可称为 ,仅通过该过程产生的大量氨基酸仍满足不了人体自身蛋白质合成的需要,主要原因是 。
(5)在实验动物小肠末的肠腔中提取内容物,经检测一般不含游离氨基酸。由此可见,小肠吸收氨基酸的方式是 。
31㈠(7分)家蚕的性别由ZW型性染色体决定,其方式与XY型刚好相反,即雌性个体的体细胞含2个异型的性染色体,用ZW表示。
家蚕中存在肤色正常(Os)和油纸样透明皮肤(os)(其他各项生命活动指标均正常)两个品种,控制该相对性状的基因均位于Z染色体上,W染色体无相应等位基因。雄蚕吃的桑叶少,蚕丝产量高,质量好。
现有正常肤色和油蚕两个品种的雌、雄尚未交配的纯种蚕蛾若干,请你以遗传图解的方式设计一种杂交方案,目的是在幼龄阶段就能区分雌、雄个体,以便分别喂养和缫丝,提高蚕丝的产量和质量。
答:
㈡赤霉素是一种重要的植物激素,其主要作用是调节植物生长。(14分)
I.已知豌豆矮蔓植株的形成与缺少赤霉素有关。没有赤霉素就不能刺激茎蔓伸长,如果用赤霉素处理,矮生植株也可以长得和高蔓植株一样高,矮株没有赤霉素是因为缺少了合成赤霉素的一种关键酶。
(1)高蔓植株合成此种酶要经过“翻译”的过程,进行“翻译”的条件除核糖体外还需要有__________________________________________________________;
(2)如果形成矮生植株的原因是由于编码合成赤霉素的酶的基因发生了隐性突变,如果让基因型为Aa的植株自交,其后代再分别自交,这样自交三代,请在坐标轴上绘出自交后代中能稳定遗传的非矮化个体所占的比例与自交代数的数量变化关系的直方图,并将比例值注明在直方图的上方:

Ⅱ.玉米矮化病毒能显著抑制玉米植株的生长,因而感染这种病毒的玉米植株非常矮小。推测病毒的作用可能是抑制了赤霉素的合成。请用被矮化病毒感染的玉米幼苗、适宜浓度的赤霉素溶液、刻度尺、喷壶等设计实验来验证这一假设。
(1)实验步骤:
 (2)右表是某生物小组所做实验的结果记录:
(2)右表是某生物小组所做实验的结果记录:
根据以上实验结果得出的实验结论是:
 2009年普通高等学校招生全国统一考试(南开中学模拟卷)
2009年普通高等学校招生全国统一考试(南开中学模拟卷)
30.(一)(7分)下表是对某水生生态系统营养级和能量流动情况的调查结果,表中A、B、C、D分别表示不同营养级生物,E为分解者。Pg表示生物同化作用固定能量的总量,Pn表示生物体内未被呼吸消耗的能量(Pn=Pg-R),R表示生物呼吸消耗的能量。(单位:102kJ/m2/年)请根据表中数据回答下列问题:
|
|
Pg |
Pn |
R |
|
A |
15.9 |
2.8 |
13.1 |
|
B |
870.7 |
369.4 |
501.3 |
|
C |
0.9 |
0.3 |
0.6 |
|
D |
141.0 |
61.9 |
79.1 |
|
E |
211.5 |
|
|
(1)此生态系统中能量流动是从表中的_________生物开始的,做出此判断的依据是
_______________________________________________________________。
(2)能量从第Ⅱ营养级传递到第Ⅲ营养级的效率是____________(保留一位小数)。
(3)从能量输出和输入角度看,该生态系统的总能量将会__________(增加、减少)。其原因是______________________________________________________。
(4)在测定此生态系统中鲢鱼的种群密度时,研究人员选择了40m×20m的区域,放置了40个捕鱼器,两次在相同时间段内捕获的鲢鱼数量如下:
|
|
捕获鲢鱼数量 |
被标记的鲢鱼数量 |
|
第一次 |
55 |
55 |
|
第二次 |
53 |
5 |
此生态系统中鲢鱼的总数量是_________尾,鲢鱼的种群密度是___________。
29.(14分)在元素周期表中处于相邻位置的元素在结构和性质上有许多相似的地方。第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除H2O外,还有H2O2;碳元素的氢化物除CH4外,还有C2H6等,与之相似的氮元素的氢化物除NH3外,还有N2H4等。
⑴碳原子之间可以结合成链状结构,氮原子之间也可以形成链状结构,假设氮原子间只以氮氮单键形式连接成链状,并形成氢化物,则该系列氢化物的通式为
⑵该系列中的N2H4是“神六”发射时火箭所用的液体燃料,液态的四氧化二氮作氧化剂,此液态燃料的优点是产生的能量大并没有污染。已知4gN2H4在上述反应中放出71kJ的热量,写出该反应的热化学方程式
⑶该系列物中NH3对农业、化学、国防工业具有重要意义。其合成原理为:
N2(g) +
3H2(g)  2NH3(g),DH= - 92kJ/mol。
2NH3(g),DH= - 92kJ/mol。
I.在一定温度下,将1.5molN2和6molH2通入到一个固定容积的密闭容器中,当反应达到平衡时,容器内气体的压强为起始时的80%,此时反应放出的热量为
II.保持温度不变,在相同的容器中,将起始时的物质的量改为a mol N2、b molH2、c mol NH3,使平衡时NH3的物质的量分数为25%,则:
①达到平衡时,I和II放出的热量 (填字母代号)
A.一定相等 B.前者一定小于后者
C.前者等于或小于后者 D.前者等于或大于后者
②欲使开始时反应正向进行,a的取值范围为
28.(18分)2005年的诺贝尔化学奖颁给了3位在烯烃复分解反应研究方面做出突出贡献的化学家。烯烃复分解反应实际上是在金属烯烃络合物的催化下实现C=C双键两边基团换位的反应。如下图表示了两个丙烯分子进行烯烃换位,生成两个新的烯烃分子--丁烯和乙烯。

 现以石油裂解得到的丙烯为原料,经过下列反应可以分别合成重要的化工原料I和G。I和G在不同条件下反应可生成多种化工产品,如环酯J。
现以石油裂解得到的丙烯为原料,经过下列反应可以分别合成重要的化工原料I和G。I和G在不同条件下反应可生成多种化工产品,如环酯J。
请按要求填空:
(1)写出下列反应的反应类型:
①______________,⑥______________,⑧______________。
(2)反应②的化学方程式是___________________________________________
(3)反应④、⑤中有一反应是与HCl加成,该反应是________(填反应编号),设计这一步反应的目的是__________________________________________物质E的结构简式是_______________________。
(4)反应⑩的化学方程式是__________________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com