
题目列表(包括答案和解析)
4.依据下图,下列关于生长素调节的说法正确的是
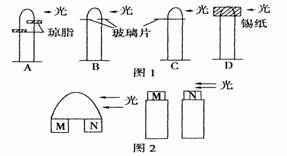
A.图1中可使其发生向右弯曲生长的处理只有A
B.图1中C、D都不弯曲,其原理相同
C.图2中放N的胚芽鞘长得比放M的快
D.图2中放M的胚芽鞘弯向一侧而放N的不弯曲
3.种群在理想环境中,呈“J”型曲线增长(如右图甲);在有环境阻力条件下,呈“S”型曲线增长(如右图乙)。下列有关种群增长曲线的叙述,正确的是

A.若该图表示草履虫种群增长曲线,当种群数量达到e点后,增长速率为O
B.种群中出现环境阻力是在d点之后
C.若该图表示蝗虫种群增长曲线,则虫害的防治应在c点之后
D.K值是环境的最大容纳量,不随环境的变化而改变
2.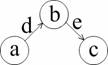 右图为人体和人体细胞内某些信息传递机制的模式图,图中箭头表示信 息的传递方向。下列叙述中,不正确的是
右图为人体和人体细胞内某些信息传递机制的模式图,图中箭头表示信 息的传递方向。下列叙述中,不正确的是
A.如果该图表示细胞中遗传信息的表达过程,则e过程发生
在核糖 体上
B.如果a表示抗原决定簇,b表示吞噬细胞和T细胞,c为B细胞,则该过程为体液免疫
C.如果该图表示反射弧,则其中的信息是以局部电流的形式传导的
D.如果该图中a为下丘脑,b为垂体,c为肾小管和集合管,则d和e为同一物质
1.在实验条件下,测试某种恒温动物离体细胞的呼吸作用强度(E)受温度变化的影响,结果如下图

(二)(10分)植物表现出的顶端优势--植物的顶芽优先生长而侧芽受到抑制的现象,就是因为顶芽产生的生长素向下运输,大量地积累在侧芽部位,在侧芽的生长受到抑制的缘故。
为了验证“植物顶芽产生的生长素能抑制侧芽的生长”,请根据所给的材料和用具设计实验:
材料和用具:生长状况相同的柳树幼苗若干,不含和含生长素的羊毛脂,剪刀等。
(1)实验步骤:
①
②
③
(2)实验结果:
(3)实验结论:
1. 2008年9月,中国爆发三鹿婴幼儿奶粉受污染事件,导致食用了受污染奶粉中含有三聚氰胺。一般来说,每100克蛋白质平均含氮16克,这些氮素主要存在于蛋白质的:
2008年9月,中国爆发三鹿婴幼儿奶粉受污染事件,导致食用了受污染奶粉中含有三聚氰胺。一般来说,每100克蛋白质平均含氮16克,这些氮素主要存在于蛋白质的:
A.肽键 B .游离的氨基 C.游离的羧基 D.R.基团
2. 据美国犯罪心理学家和生物遗传学家联合研究发现,XYY(性染色体组成)综合征患者有暴力倾向,有反社会行为。研究成果称,多出的这条Y染色体为“犯罪染色体”,是导致这类人出现异常犯罪行为的关键所在。下列关于XYY综合征的叙述正确的是
A.患者为男性,是由于母方减数第一次分裂产生异常的卵细胞所致
B.患者为男性,是由于父方减数第一次分裂产生异常的精子所致
C.患者为男性,是由于父方减数第二次分裂产生异常的精子所致
D.患者为女性,是由于母方减数第二次分裂产生异常的卵细胞所致
3.植物单个叶片的光合作用强度可以通过通气法来测定,如下模式简图(Ⅰ)所示。将 叶
片置于同化箱中,在特定的光照、温度条件下,让空气沿箭头方向流动,并检测通入和
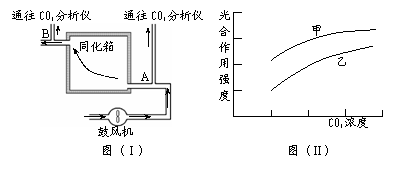 通出气体的CO2浓度变化。以下有关该实验的说法错误的是
通出气体的CO2浓度变化。以下有关该实验的说法错误的是
A.当B处气体的CO2浓度低于A处气体的CO2浓度时,说明植物光合作用强度大于呼吸作用的强度
B.控制特定的光照强度或空气中原有的CO2浓度,都可能使A处和B处检测到的CO2浓度相同
C.可以通过在黑暗条件下测定通入和通出气体的差值来检测叶片消耗O2的速率,从而确定叶片有氧呼吸的强度
D.在各自适宜条件下分别测定天竺葵、玉米光合作用强度,结果如曲线图(Ⅱ)所示,其中甲表示玉米光合作用强度曲线
4. 下列表格中,完全正确的一项是 
|
|
物质名称 |
化学本质 |
主要功能 |
|
A |
干扰素 |
多糖 |
几乎能抵抗所有病毒引起的感染 |
|
B |
促甲状腺激素 |
氨基酸 |
促进甲状腺生长发育,调节甲状腺激素合成和分泌 |
|
C |
RNA聚合酶 |
蛋白质 |
催化DNA转录为RNA |
|
D |
生长素 |
吲哚乙酸 |
促进植物细胞分裂 |
5. 哮喘是世界性顽症,最新研究发现哮喘的生化接触点潜伏在淋巴细胞中。
下图为人的淋巴细胞的体液免疫图解,下列哪项都不正确
①细胞①③④⑤依次是吞噬细胞、B细胞、记忆细胞、效应B细胞
②Ⅰ、Ⅱ、Ⅲ、Ⅳ四个过程属于体液免疫的感应阶段
③细胞①③④⑤都能特异性识别抗原
④阶段IV、V为体液免疫的反应阶段
⑤在Ⅳ、Ⅴ、Ⅵ的过程中细胞内要进行DNA的复制、 转录以及翻译
⑥物质⑥的化学本质是球蛋白,在细胞⑤内的内质网中加工到分泌到细胞外,共要穿过4层膜。 A、①②③ B、②③⑥
C、④⑤⑥
D、④⑤
A、①②③ B、②③⑥
C、④⑤⑥
D、④⑤
6、25℃,某溶液中水电离出的C(H+)=10-5mol/L,则该溶液可能是下列情况中的 A.该溶液是盐溶液 B.该溶液可能是酸或碱溶液 C.该溶液中C(OH-)=10-5mol/L D.该溶液与pH=9的氢氧化钠溶液等体积混合,混合后溶液可能呈中性
7.下列叙述正确的是 A.同周期非金属的原子半径越大,其气态氢化物越稳定 B.同周期元素的离子,核电荷数越大,半径越小 C.同主族元素电子层越多,金属元素越易失电子,非金属元素越难得电子 D.同主族元素一定含有金属元素和非金属元素
8. 下列操作或仪器的选用正确的
下列操作或仪器的选用正确的
A.滴定FeSO4溶液 B.制取O2 C.制备Fe(OH)2 D.除去乙醇中的乙酸 9、设NA表示阿伏加德罗常数的数值,下列说法正确的是 A.用惰性电极电解500mL饱和食盐水,若溶液的pH值变为14时,则电极上转移的
电子数目为NA B.常温常压下,6g石英晶体中,含有0.4NA个硅氧共价键 C.在标准状况下,各为1mol的二氧化硫和三氧化硫的体积均约为22.4L D.在1L 0.2mol·L-1的硫酸铁溶液中含有的铁离子数为0.4NA
10、某温度下体积一定的密闭容器中进行如下可逆反应:
X(g)+Y(g)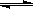 Z(g)+W(s);△H > 0;下列叙述正确的是
A.减少少量W,逆反应速率减小
B.当容器中气体的平均相对分子量不变时,反应达到平衡
C.降低温度,平衡正向移动
D.平衡后加入Z,上述反应的△H减小
11、下列离子方程式中正确的是
A.NaHCO3水解:HCO3-+ H2O = H3O+ +CO32-
B.向NH4HCO3溶液中加入过量NaOH溶液:HCO3-+ OH- = CO32-+ H2O
C.向KHSO4溶液中滴入Ba(OH)2溶液使pH = 7:SO42-+H+ +Ba2+ +OH- = BaSO4↓+H2O
D.氨水和醋酸反应:NH3·H2O
+ CH3COOH = NH4++ CH3COO- +H2O
12、实验室为标定一种烧碱样品配成的溶液的物质的量浓度,称取该烧碱样品4.Og配成1L溶液,
Z(g)+W(s);△H > 0;下列叙述正确的是
A.减少少量W,逆反应速率减小
B.当容器中气体的平均相对分子量不变时,反应达到平衡
C.降低温度,平衡正向移动
D.平衡后加入Z,上述反应的△H减小
11、下列离子方程式中正确的是
A.NaHCO3水解:HCO3-+ H2O = H3O+ +CO32-
B.向NH4HCO3溶液中加入过量NaOH溶液:HCO3-+ OH- = CO32-+ H2O
C.向KHSO4溶液中滴入Ba(OH)2溶液使pH = 7:SO42-+H+ +Ba2+ +OH- = BaSO4↓+H2O
D.氨水和醋酸反应:NH3·H2O
+ CH3COOH = NH4++ CH3COO- +H2O
12、实验室为标定一种烧碱样品配成的溶液的物质的量浓度,称取该烧碱样品4.Og配成1L溶液,
取出20.00mL置于锥形瓶中,用0.10mol·L-1 HCl标准溶液滴定,恰好完全中和时消耗标准盐酸19.00mL,若烧碱中只含有一种杂质,则不可能是 A. NaHCO3 B. Na2CO3 C. Ca(OH)2 D.NaCl
13、今有一混合物的水溶液,只可能含以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、
CO32-、SO42-,现取三份100mL溶液进行如下实验: (1)第一份加入AgNO3溶液有沉淀产生 (2)第二份加足量NaOH溶液加热后,收集到气体0.04mol (3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为
2.33g。根据上述实验,以下推测正确的是 A、K+一定存在 B、100mL溶液中含0.01mol CO32- C、Cl-一定存在 D、Ba2+一定不存在,Mg2+可能存在 二、选择题(本题包括8小题,共48分。每小题给出的四个选项中,有的只有一个选项
正确,有的有多个选项正确,全部选对的得6分,选对但不全的得3分,有选错的得0分)
14.下列关于静电场的说法正确的是
A.在点电荷形成的电场中没有场强相等的两点,但有电势相等的两点
B.正电荷只在电场力作用下,一定从高电势向低电势运动
C.场强为零处,电势不一定为零;电势为零处,场强不一定为零
D.初速为零的正电荷在电场力作用下一定沿电场线运动
15.如图所示,在波的传播方向上间距均为1 m的五个质点a、b、c、d、e均静止在各自的平衡位置。一列简谐横波以l m/s的速度水平向右传播,已知t=0时,波到达质点a,质点a开始由平衡位置向下运动,t = 3s时,质点a第一次到达最高点,则下列说法正确的是
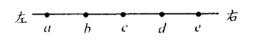 A.质点d开始振动后的振动频率为4 Hz
A.质点d开始振动后的振动频率为4 Hz
B.t = 4 s时,波恰好传播到质点e
C.t = 5 s时,质点b到达最高点
D.在4s<t<5s这段时间内,质点c的加速度方向向下
16.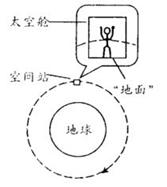 在圆轨道上做匀速圆周运动的国际空间站里,一宇
在圆轨道上做匀速圆周运动的国际空间站里,一宇
航员手拿一只小球相对于太空舱静止“站立”于舱内朝向
地球一侧的“地面”上,如图所示。下列说法正确的是
A.宇航员相对于地球的速度介于7.9km/s
与11.2km/s之间
B.宇航员将不受地球的引力作用
C.宇航员对“ 地面”的压力等于零
D.若宇航员相对于太空舱无初速释放小球,
小球将落到“ 地面”上
17.如图所示,一滑块恰能在一个斜面体上沿斜面匀速下滑;当用平行于斜面方向向下的力推此滑块时,滑块将沿斜面加速下滑。若滑块匀速下滑与加速下滑时,斜面体都保持静止,且用f1和f2分别表示上述两种情况下斜面体受到水平地面的摩擦力,则
 A.f1为零,f2不为零且方向向左
A.f1为零,f2不为零且方向向左
B.f1为零,f2不为零且方向向右
C.f1不为零且方向向右,f2不为零且方向向左
D.f1和f2均为零
18.某跳伞运动训练研究所,让一名跳伞运动员从悬停在高空的直升飞机中跳下,研究人员利用运动员随身携带的仪器记录下了他的运动情况,通过分析数据,定性画出了运动员从跳离飞机到落地的过程中在空中沿竖直方向运动的v – t图像如图7所示,则对运动员的运动下列说法正确的是
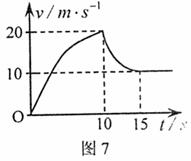 A.0–15末都做加速度逐渐减小的加速度动
A.0–15末都做加速度逐渐减小的加速度动
B.0–10s末做自由落体运动,15s末开始做匀速
直线运动
C.10s末打开降落伞,以后做匀减速运动至15s末
D.10s末–15s末加速度方向竖直向上,加速度的
大小在逐渐减小
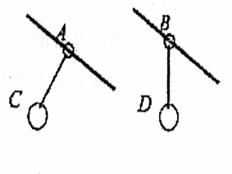
19.两滑杆上分别套A、B两圆环,两环上分别用细线悬
吊着两物体C、D,如图1所示,当它们都沿滑杆向
下滑动时,A的悬线始终与杆垂直,B的悬线始终竖
直向下,则
A.A环做的是匀速运动
B.B环做的是匀速运动
C.A环与杆之间一定有摩擦力
D.B环与杆之间一定有摩擦力
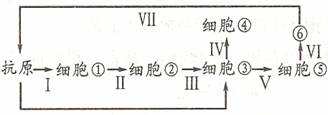
20.十七世纪七十年代,英国赛斯特城的主教约翰·维尔金斯设计了一种磁力“永动机”,其结构如图所示:在斜面顶端放一块强磁铁M,斜面上、下端各有一个小孔P、Q,斜面下有一个连接两小孔的弯曲轨道。维尔金斯认为:如果在斜坡底放一个铁球,那么在磁铁的引力作用下,铁球会沿斜面向上运动,当球运动到P孔时,它会漏下,再沿着弯曲轨道返回到Q,由于这时球具有速度可以对外做功。然后又被磁铁吸引回到上端,到P处又漏下…… 对于这个设计,下列判断中正确的是
 A.满足能量转化和守恒定律,所以可行
A.满足能量转化和守恒定律,所以可行
B.不满足热力学第二定律,所以不可行
C.不满足机械能守恒定律,所以不可行
D.不满足能量转化和守恒定律,所以不可行
 21.如图所示,空间的虚线框内有匀强电场,
21.如图所示,空间的虚线框内有匀强电场, 、
、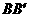 、
、 是该电场子的三个等势面,相邻等势面间的距离为0.5cm,其中
是该电场子的三个等势面,相邻等势面间的距离为0.5cm,其中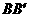 为零势能面,一个质量为m,带电量为+q粒子沿
为零势能面,一个质量为m,带电量为+q粒子沿 方向以初动能Ek自图中的P点进入电场,刚好从
方向以初动能Ek自图中的P点进入电场,刚好从 点离开电场,已知
点离开电场,已知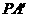 =2cm,粒子重力忽略不计,下列说法中正确的是
=2cm,粒子重力忽略不计,下列说法中正确的是
A.该粒子到达 点时的动能是2Ek
点时的动能是2Ek
B.该粒子通过等势面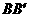 时的动能是1.25Ek
时的动能是1.25Ek
C.该粒子在P点时的电势能是Ek
D.该粒子到达 点时的电势能是0.5Ek
点时的电势能是0.5Ek
非选择题 (十大题 共174分)
22. (1)(3分)用自由落体仪(如图13所示)测量重力加
(1)(3分)用自由落体仪(如图13所示)测量重力加
速度。通过电磁铁控制的小铁球每次从同一点A处
自由下落,下落过程中依次经过并遮断两个光电门
B、C,从而触发与之相接的光电毫秒计时器,每次
下落,第一次遮光(B处)开始计时,第二次遮光
(C处)停止计时,并可读出相应的b、c两处位置
坐标。在第一次实验过程中,计时器所记录的从B
至C的下落时间为t1,B、C两光电门的高差为h1。
现保持光电门C位置不动,改变光电门B的位置,
再做第二次实验。在第二次实验过程中,计时器所
记录的从B至C的下落时间为t2,B、C光电门的
高差为h2。由此测得的重力加速度g的计算公式为:
g= 。
(2)(3分)下列有关高中物理学生实验的描述中,正确的是( )
 A.“验证机械能守恒定律”实验中,不需要
A.“验证机械能守恒定律”实验中,不需要
用天平测出下落重锤的质量
B.电火花打点记时器和电磁打点记时器均
在4-6V交流电压下正常工作,当频
率为50Hz时,每隔0.02s打一次点
C.“用单摆测定重力加速度”实验中,对秒
表读数时漏掉了小刻度盘(分针)的数字,
将导致重力加速度的测量值比实际值偏大
D.“验证动量守恒定律”实验中,在白纸上记下重锤线所指的位置O后,不小心将白纸和复写纸同时向右移动了少许,继续实验,得到小球在白纸上落点的平均位置A、B、C(如图),白纸的移动为实验结果没有影响
(3)(12分)请用所给器材设计两种估测手对小球做功的值.
器材:A.小球 B.毫米刻度尺 C.游标卡尺 D.秒表 E.天平和砝码 F.细绳 (重力加速度g已知) 。
方法一:选择器材______________________(填上器材所对应的字母);
简述方法并表示结果__________________________________________。
方法二:选择器材______________________(填上器材所对应的字母);
简述方法并表示结果______________________________________。
23.(16分)如图14所示,O点系一绝缘细线,线的另一端系一带电量为+q,质量为m的带电小球,空间存在电场强度为E,方向水平的匀强电场,电场所分布的区域足够大。
(1)若小球首先静止,烧断细线后小球做什么运动?(不要求分析)
(2)小球静止时,细线的拉力是多大?方向怎样?
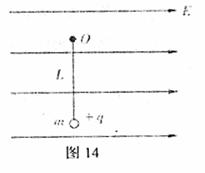 (3)若小球拉到O点右边等高水平位置由静止释放,绕O点在竖直平面内做圆周运动到最底点时细线的拉力是多大?
(3)若小球拉到O点右边等高水平位置由静止释放,绕O点在竖直平面内做圆周运动到最底点时细线的拉力是多大?
24.(16分)如图所示,在同一竖直平面内两正对着的相同半圆光滑轨道,相隔一定的距离,虚线沿竖直方向,一小球能在其间运动,今在最高点与最低点各放一个压力传感器,测试小球对轨道的压力,并通过计算机显示出来,当轨道距离变化时,测得两点压力差与距离x的图像如图,g取10 m/s2,不计空气阻力,求:
(1)小球的质量为多少?
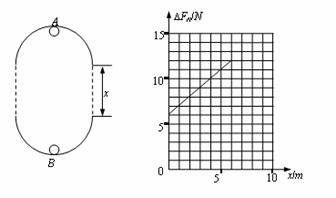 (2)若小球在最低点B的速度为20 m/s,为使小球能沿轨道运动,x的最大值为多少?
(2)若小球在最低点B的速度为20 m/s,为使小球能沿轨道运动,x的最大值为多少?
25.如图所示,光滑水平面MN上放两相同小物块A、B,左端挡板处有一弹射装置P,右端N处与水平传送带理想连接,传送带水平部分长度L=8m,沿逆时针方向以恒定速度v=6m/s匀速转动。物块A、B(大小不计)与传送带间的动摩擦因数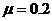 。物块A、B质量mA=mB=1kg。开始时A、B静止,A、B间压缩一轻质弹簧,贮有弹性势能Ep=16J。现解除锁定,弹开A、B。求:
。物块A、B质量mA=mB=1kg。开始时A、B静止,A、B间压缩一轻质弹簧,贮有弹性势能Ep=16J。现解除锁定,弹开A、B。求:
(1)物块B沿传送带向右滑动的最远距离。
(2)物块B滑回水平面MN的速度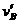 。
。
(3)若物体B返回水平面MN后与被弹射装置P弹回的A在水平面上相碰,且A、B碰后互换速度,则弹射装置P必须给A做多少功才能让AB碰后B能从Q端滑出。

26.(18分)已知由短周期元素组成的A、B、C、D四种常见化合物分子中所含原子数目依次为2、
3、4、5,其中A、B含有18个电子,C、D含有10个电子。请回答: (1)B的结构式为 ,D中含有的化学键类型是 ,已知8gD与O2完全燃烧,
生成稳定化合物时放出445kJ的热量,写出反应的热化学方程式:
。 (2)室温下,若向一定量C的稀溶液中逐滴加入物质的量浓度相同的A,直至A过量,生成化合
物XY4Z(X、Y、Z表示元素符号)。讨论上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH。试填写表中空白(要求填写有关粒子化学式):
|
|
离子浓度由大到小的顺序 |
溶质的化学式 |
溶液的pH |
|
I |
c(XY+4)>c(Z-)>c(OH-)>c(H+) |
|
pH>7 |
|
II |
c(XY+4)=c(Z-) |
XY4Z、XY3·H2O |
|
|
III |
|
XY4Z |
pH<7 |
|
IV |
c(Z-) >c(H+)>c(XY+4)>
>c(OH-) |
|
pH<7 |
(3)B在空气中完全燃烧生成E,在一定条件下发生E与O2反应生成F。 ①将0.05molE和0.03molO2放入容积为1L的密闭容器中,达到平衡,测得c(F)=0.04mol·L-1。
则该条件下反应达到平衡时E的转化率为: ②已知上述反应是放热反应,当该反应处于平衡状态时,下列措施中有利于提高E平衡转化率
的有 (填字母)。 A.升高温度 B.降低温度 C.增大压强
D.减小压强 E.加入催化剂 F.移出氧气 27.(15分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的
反应式:NO3-+4H++3e-== NO +2H2O;
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:______________________________________
(2)若1mol甲与某浓度硝酸反应时,被还原的硝酸的物质的量增加,原因是:
__________ ______。
(3)由物质甲与Cu和CuO组成的混合物,向其中加入100mL 0.6mol/LHNO3溶液刚好使其溶解,同时收集到224mLNO气体(标准状况)。请回答下列问题: a. 如混合物中含0.01molCu,则其中物质甲、CuO的物质的量分别是________mol、
__________mol; b.如混合物中Cu的物质的量为X,求X的取值范围________________。
28.(15分)化学中常用类比的方法可预测许多物质的性质。如根据H2+Cl2=2HCl推测:H2+Br2=2HBr。但类同是相对的,如根据2Na2O2+2CO2=
Na2CO3+ O2, 类推2Na2O2+2SO2= Na2SO3+
O2是错误的,应该是Na2O2+SO2=
Na2SO4。
(1)下列各组类比中正确的是________
A 由NH4Cl
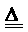 NH3↑+HCl↑
推测:NH4I
NH3↑+HCl↑
推测:NH4I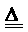 NH3↑+HI↑
NH3↑+HI↑
B.由CO2+Ca(ClO)2+H2O=CaCO3↓+2HClO推测:2SO2+Ca(ClO)2+H2O=CaSO3↓+2HClO
C.由2CO2+Ca(ClO)2+2H2O=Ca(HCO3)2+2HClO推测:CO2+NaClO+H2O=NaHCO3+HClO
D.由Na2SO3+2HCl=2NaCl+H2O+
SO2↑推测:Na2SO3+2HNO3=2NaNO3+H2O+
SO2↑
(2)根据2NaCl+H2SO4(浓) Na2SO4+2 HCl↑的反应原理例举一个制取类似气体的反应(写
Na2SO4+2 HCl↑的反应原理例举一个制取类似气体的反应(写
出方程式) 。 (3)由氢氧化铁与盐酸生成氯化铁和水,应用有关知识,推断氢氧化铁与氢碘酸的化学方程
式 。 (4)从2F2+ H2O=4HF+ O2反应预测2F2+ 4NaOH=4NaF+ O2,然而经过实验,物质的量相等的氟气和
氢氧化钠正好完全反应,生成氯化钠、水和放出一种气体,请根据实验结果写出该气体的电子式 。
(5)复分解反应中有一条规律:较强酸制较弱酸。请写出一种属于复分解反应且以较弱酸制较强酸的化学反应方程式: 。
29. (12分)莽草酸是合成治疗禽流感的药物-达菲(Tamiflu)的原料之
(12分)莽草酸是合成治疗禽流感的药物-达菲(Tamiflu)的原料之
一。莽草酸是A的一种同分异构体。A的结构简式如下: (1)A的分子式是 。 (2)A与氢氧化钠溶液反应的化学方程式(有机物用结构简式表示)是 :
___________________________________________________。 (3)已知相同物质的量浓度的A与醋酸溶液,由水电离的C(H+)前者比后者要大,则它们与氢氧
化钠恰好完全中和时溶液的PH的大小关系是前者_______后者(填“大于”、“小于”或“等于”)。
(4)A在浓硫酸作用下加热可得到B(B的结构简式为 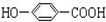 ),其反应类型是
。
),其反应类型是
。
(5)B的同分异构体中既含有酚羟基又含有酯基的共有 种,写出其中一种同分异构体的结构简式 。 30.(20分)糖尿病是日常生活中的常见病,发病率有上升的趋势。下图是人体内的血糖平
衡调节示意图,请据图回答问题。

⑴ 图中甲、乙分别表示 (结构),
A、B、C分别表示 (激素)。
⑵ 图中①的作用效果是 ,②的作用效果是 。
⑶ 图中具有协同作用与拮抗作用的激素分别是 、 (用图中字母表示)。
⑷ 人体内血糖浓度高于 时,会出现尿糖,可用尿糖试纸进行检测。
⑸ 当葡萄糖在细胞中进行无氧呼吸,其产物进入血液可与 (Na2CO3或
NaHCO3)发生反应,此反应的生理意义是 。
⑹ 某患者体温调节能力下降甚至丧失,最可能受损的是 。
31.实验题(一)(12分)LHRH(促性腺激素释放激素)和HCG(促性腺激素)都能引起
蛙排精。为验证这两种激素的作用部位不同,可设计如下实验。请你补充实验设计中
空缺的内容,预测并解释实验结果:
材料和用具:成体雄蛙,LHRH溶液,HCG溶液,生理盐水,注射器,滴管,剪刀,镊子,载玻片,显微镜等。(提示:给药剂量和仪器的用具操作不作要求,给药2小时后蛙排精)
(1)实验步骤;
①分别用滴管对每只蛙采尿液,滴于不同的载玻片上,用显微镜观察,选出尿液中无精子的蛙30只,平均分成A、B、C、D、E、F六组;
②用剪刀和镊子摘除A、B、C三组蛙的 ,D、E、F三组蛙不作处理;
③分别用注射器给蛙注射适量药剂。
|
组别 |
A |
B |
C |
D |
E |
F |
||
|
药剂 |
LHRH |
|
生理盐水 |
|
HCG |
生理盐水 |
④2小时后即分别用滴管对每只蛙采尿液,滴于不同的载玻片上,用显微镜观察。
(2)预测实验结果
|
组别 |
A |
B |
C |
D |
E |
F |
|
尿液中有无精子 |
|
有 |
无 |
有 |
|
无 |
(3)解释实验结果:
31. (共22分)Ⅰ(8分)菜豆种皮颜色由两对非等位基因A(a)和B(b)调控。A基因控制色素合成(A-显性基因-出现色素,AA和Aa的效
(共22分)Ⅰ(8分)菜豆种皮颜色由两对非等位基因A(a)和B(b)调控。A基因控制色素合成(A-显性基因-出现色素,AA和Aa的效
应相同),B基因为修饰基因,淡化颜色的深
度(B-显性基因-修饰效应出现,既有BB和
Bb的效应不同)。现有亲代种子P1(纯种,白色)
和P2(纯种、黑色),杂交实验如下:
(1)F2种皮颜色发生性状分离 (能/不能)
在同一豆荚体现。
(2)①P1的基因型是 ;
②F2中种皮为白色的个体基因型有 种,
其纯种个体大约占 。
II(14分)为了验证某大豆品种的矮化特性与赤霉素的含量有关,请用所给的实验材料,完成下列实验步骤并回答问题:
实验材料:具2片真叶且长势相同的该品种大豆幼苗若干、完全培养液、蒸馏水、适宜浓度的赤霉素溶液、喷壶等。
(1)实验步骤:
将上述大豆幼苗平均分成A、B两组,A组为对照组,B组为实验组,分别置于等量的完全培养液中培养。用喷壶分别将 和 喷洒在A、B两组幼苗上。将两组苗置于相同且适宜的温度和光照等条件下培养,一段时间后,测定两组植株的 。
(2)预测实验结果: 。
(3)上述试验中,如果A、B两组各选用1株幼苗进行实验,是否影响实验结果的可靠性?
为什么? 。
(4)为了确定赤霉素对该大豆品种的矮化特性的最适宜浓度,某同学用两种浓度的赤霉素溶液分别处理大豆幼苗作为两个实验组,用蒸馏水处理作为对照组进行实验,结果发现三组大豆幼苗无差异。请参考该同学的实验,在下一步实验中你应该如何改进,才能达到本实验的目的?
30.(共20分)I(10分):下图表示人体内三大营养物质代谢之间的关系。据图回答:

(1)从图中看出糖类、脂质和蛋白质之间可以转化,氨基酸必须通过______________作用才能转化成糖类和脂肪。
 (2)人体中主要的能源物质是______________。人在饥饿初期,血糖含量会暂时降低,这时_____________________可以分解成葡萄糖并进入血液,使血糖含量恢复正常。
(2)人体中主要的能源物质是______________。人在饥饿初期,血糖含量会暂时降低,这时_____________________可以分解成葡萄糖并进入血液,使血糖含量恢复正常。
(3)血红蛋白是由574个氨基酸经过图中⑦过程形成的一种具有四条肽链的蛋白质,在这些氨基酸形成1个血红蛋白分子的过程中,共脱去_______个水分子。
(4)标号④得到的氨基酸称之为 。
II(10分):下图表示C3植物的叶肉细胞在室温、一定的光照强度(N点后停止光照)条件下,O点开始提供14C标记的0.03%的CO2,叶肉细胞内C3和C5中14C含量相对值随时间变化曲线。分析回答:
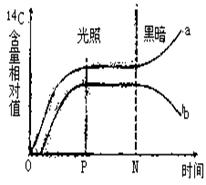 ①图中
(字母)曲线表
①图中
(字母)曲线表
示C3的14C含量相对值变化。
②N点后,b曲线下降的原因是
。
③在此过程中,叶肉细胞内糖类中14C含量
相对值随时间变化的趋势是 。
④如果用C4植物的叶肉细胞进行该实验,那么,
叶肉细胞中能否检测到含14C的糖类
(不考虑有机物运输)? 。
原因是 。
29.(12分)某研究性学习小组进行了一系列化学实验后,发现高锰酸钾分解后的含锰元素的化合物都能和浓盐酸反应制得氯气,锰化合物的还原产物都是MnCl2(如:K2MnO4+8HCl= MnCl2+2Cl2↑+2KCl+4H2O)。他们又进行了以下一些有关定量的实验,按要求填空(气体体积都折合成标准状况):
(1)称取了31.6gKMnO4粉末,放在试管中加热充分反应后,收集到气体的体积是 ;另取31.6gKMnO4粉末和足量盐酸反应,收集到气体体积是 。
(2)将31.6gKMnO4粉末加热一段时间,收集到1.12L气体后停止加热,冷却后放入足量的浓盐酸再加热,又收集到气体体积是 。
(3)将a molKMnO4粉末加热一段时间,收集到V1L气体后停止加热,冷却后放入足量的浓盐酸再加热反应充分后,又收集到气体体积V2L。则V2= (用a、V1表达)。
28.(15分)几种短周期元素的原子半径及其某些化合价见下表:
|
元素代号 |
A |
B |
D |
E |
G |
H |
I |
J |
|
化合价 |
-1 |
-2 |
+4、-4 |
+4、-2 |
+5、-3 |
+3 |
+2 |
+1 |
|
原子半径/nm |
0.071 |
0.074 |
0.077 |
0.102 |
0.110 |
0.143 |
0.160 |
0.186 |
分析上表中有关数据,并结合已学过的知识,回答以下问题。涉及上述元素的答案,请用元素符号表示。
(1)E元素在周期表中的位置 ;
(2)A、H、J对应离子的半径由大到小的顺序是(填离子符号) ;
(3)A与J所形成化合物的晶体类型是 ,该物质溶于水呈碱性的原因(用化学方程式表示) ;
(4)B与H所形成的化合物与J的最高价氧化物的水化物X的溶液发生反应的离子方程式为 ;D与B形成的某种化合物Y不仅能与X反应,还能与I的单质反应。则Y与I的单质反应的化学方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com