
题目列表(包括答案和解析)
2.在平直的公路上行驶的汽车内,一乘客以自己的车为参照物向车外观察,他看到的下述现象中不正确的是
A.与汽车同向行驶的自行车,尽管车轮转动正常,但自行车向后运动
B.公路两旁的树因为有根扎在地里,所以是不动的
C.有一辆汽车总在自己的车前不动
D.路旁边的房屋是运动的
1.关于重心,下列说法正确的是
A.重心就是物体内重力最大的点
B.任何几何形状规则的物体的重心必与几何中心重合
C.重心是重力的作用点,它总是在物体上,不可能在物体外
D.重心是物体各部分所受重力的合力的作用点
32.[生物--现代生物科技专题](10分)
据2008年1月17日《干细胞》杂志报道,某科学家使用了进行试管受精的年轻女性捐献的卵子,以及2名志愿者的皮肤成纤维细胞,成功克隆出了5个人体胚胎,进而可以开发出有研究价值的干细胞。请回答:
(1)上述过程中主要应用到的两项动物细胞工程技术为 ;若将某经过修饰的基因导入其中的部分胚胎干细胞,常用的方法是 。
(2)在使用合成培养基进行胚胎干细胞培养时,通常需要加入 等天然成分。在细胞培养时,要保证被培养的细胞处于一定的气体环境,所需要的气体主要有 。
(3)科学家欲进行胚胎分割移植,则应该选择发育良好、形态正常的 或囊胚,将其移入盛有操作液的培养皿中,然后用分割针进行分割。
泉州七中2009届高三年校第二次质检试卷
31.[化学---有机化学基础](13分)
双酚-A的二甲基丙烯酸酯是一种能使人及动物的内分泌系统发生紊乱,导致生育及繁殖异常的环境激素,其结构简式为:
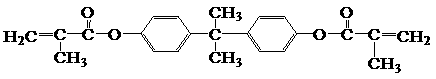
它在一定条件下水解可生成双酚-A和羧酸H两种物质。
Ⅰ.(1) 双酚-A的结构简式为_____________。
(2) 下列关于双酚-A的叙述中正确的是_________(填写字母)。
A.与苯酚互为同系物
B.可以和Na2CO3溶液反应,放出CO2气体
C.分子中最多有8个碳原子在同一平面上
D.1 mol双酚-A与浓溴水反应,最多可以消耗Br2的物质的量为4 mol
Ⅱ.已知与(CH3)3COH结构相似的醇不能被氧化为醛或酸。羧酸H可以由烯烃C通过以下途径制得(有的反应条件没有标出):
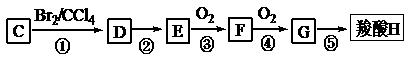
(3) C的结构简式_________________________。
(4) G中所含官能团为_________________(填名称),⑤的反应类型为______________。
(5) 羧酸H与甲醇反应后得到的酯,能形成一种高分子化合物,可用于制造高级光学仪器透镜,请写出该酯在一定条件下生成此高分子化合物的化学反应方程式:____________________________________________________。
30.[化学--物质结构与性质](13分)根据下列某些短周期元素中元素性质的有关句回答问题。
|
|
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
⑩ |
|
原子半径/10-10m |
0.37 |
1.86 |
0.74 |
1.43 |
0.77 |
1.10 |
0.99 |
1.52 |
0.75 |
0.71 |
|
最高价态 |
+1 |
+1 |
|
+3 |
+4 |
+5 |
+7 |
+1 |
+5 |
|
|
最低价态 |
-1 |
|
-2 |
|
-4 |
-3 |
-1 |
|
-3 |
-1 |
(1)元素①、②和⑧的第一电离能由大到小的顺序是_________(填元素符号);元素③、⑥和⑨的氢化物中沸点由高到低的顺序是__________(填化学式)。
(2)元素⑤、⑥和⑦的某两种元素形成的化合物中,每个原子都 满足最外层为8电子稳定结构的物质有__________(写化学式)。
(3)某元素R的原子半径为1.02×10-10m,它与钠形成Na2R2,其化学键类型有________,其电子式是_________(R用元素符号表示)。
(4)元素①和⑨形成阳离子 ,其结构式为_________,其中心原子以_______杂化轨道成键。
(5)元素⑤的原子基态电子排布式为____________。
(6)元素②和⑦形成晶体的部分结构可用下图中的______来表示(填序号)。
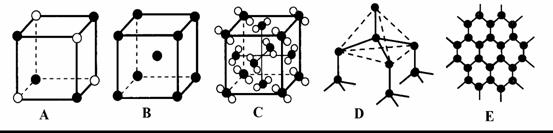
29.[物理-选修3-5](本题共有两小题,每小题6分,共12分。每小题只有一个选项符合题意)
(1)一个质子和一个中子聚变结合成一个氘核,同时辐射一个 光子。已知质子、中子、氘核的质量分别为m1、m2、m3,普朗克常量为h,真空中的光速为c。下列说法正确的是 (填选项前的编号)
光子。已知质子、中子、氘核的质量分别为m1、m2、m3,普朗克常量为h,真空中的光速为c。下列说法正确的是 (填选项前的编号)
①核反应方程是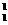 H+
H+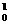 n
n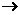
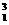 H+γ
H+γ
②聚变反应中的质量亏损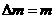 1+m2-m3
1+m2-m3
③辐射出的γ光子的能量E=(m3-m1-m2)c2
④γ光子的波长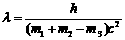
(2)质量为M=300kg的小船,长为L=3m,浮在静水中。开始时质量为m=60kg的人站在船头,人和船均处于静止状态。若此人从船头走到船尾,不计水的阻力,则船将前进_________(填选项前的编号)
① 2.5m ②0.6m ③0.5m ④ 2.4m
28.[物理-选修3-3](本题共2小题,每小题6分,共12分。每小题只有一个选项符合题意。)
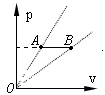 (1).如右图所示为一定质量的理想气体的P-V图,若使气体从图中的状态
A变化到状态B,则 (填选项前的编号)
(1).如右图所示为一定质量的理想气体的P-V图,若使气体从图中的状态
A变化到状态B,则 (填选项前的编号)
①气体内能减少,并放出热量
②气体内能减少,并吸收热量
③气体内能增加,并放出热量
④气体内能增加,并吸收热量
 (2) 在均匀玻璃管中有一段10cm长的水银柱,封住了一定质量的理想气体。若管口向下将玻璃管放置在一个倾角为30°的斜面上不动(如图所示),管内气体长度为8.5cm;如果管口向上竖直放置,管内气体长度为:
(填选项前的编号)
(2) 在均匀玻璃管中有一段10cm长的水银柱,封住了一定质量的理想气体。若管口向下将玻璃管放置在一个倾角为30°的斜面上不动(如图所示),管内气体长度为8.5cm;如果管口向上竖直放置,管内气体长度为:
(填选项前的编号)
(设温度不变,大气压强为P0=75cmHg)
① 6.5cm ② 7cm
③ 7.5cm ④ 8cm
27、(15分)某自花传粉植物灰种皮(Y)对白种皮(y)为显性,紫茎(A)对绿茎(a)为显性,抗病(B)对感病(b)为显性,各由一对等位基因控制,并分别位于三对同源染色体上,且当花粉含AB基因时不能完成受精作用。请回答:
⑴如果只考虑种皮颜色的遗传:将基因型为aabbYy的植株自交所结全部种子播种共得15株植株,其中有10株结灰色种子共300粒,有5株结白色种子共100粒,则子代的性状分离比与孟德尔定律预期分离比 (填相符或不相符)。
⑵如果只考虑茎的颜色和抗病性状的遗传:让基因型为AaBb的植株作父本和aabb的植株作母本,杂交产生的子代性状有 种,比为 。
⑶用基因为AAbb和aaBB的植株作材料,为获得基因型为AABB的紫茎抗病植株,可以采用杂交育种的方法吗? ;可以采用单倍体育种的方法吗? 。
(选考部分)
第II卷选考部分共5题,共35分。其中,第28、29题为物理题,第30、31为化学题,考生从两道物理题、两道化学题中各任选一题作答,若第28、29题都答,则按第28题计分,若第30、31题都作答,则按第30题计分,第32题为生物题,是必答题。请将答案都填写在答题卷选答区域的指定位置上。
26. (25分)请回答I、II题:
I、(10分)为探究环境因素对植物光合作用的影响,某同学进行了如下实验。所用材料和用具包括:符合实验条件的黑藻若干,蒸馏水,试管,25瓦、50瓦、100瓦的日光灯,精密pH试纸。请完成下列实验步骤并回答问题:
(注:默认实验中任意光照强度下,光合作用都大于呼吸作用) (1)实验步骤: ①在25℃条件下,将符合实验条件的黑藻平均分成若干组,放入相应的试管中并编号,加入等量蒸馏水浸没黑藻。 ②在黑暗条件下放置一段时间,用___________测定试管中水的pH,待其相对稳定时,记录数值。 ③将试管分别移到25瓦、50瓦、100瓦的日光灯下光照,每5分钟测定pH并记录一次,一段时间后,pH重新处于相对稳定状态。 (2)此实验的目的是探究_______________对黑藻光合作用的影响。 (3)此实验依据的原理是:当光合作用大于呼吸作用,黑藻吸收二氧化碳,使水中pH升高,通过测定不同光照条件下水中_____的变化,间接了解二氧化碳的消耗程度,以此探究不同光照强度对光合作用的影响。 (4)考虑到水中pH变化会受到非生物因素的影响,上述实验设计还应该补充________实验。具体做法是另取三支试管分别加入_______________________________,然后重复②③步骤。
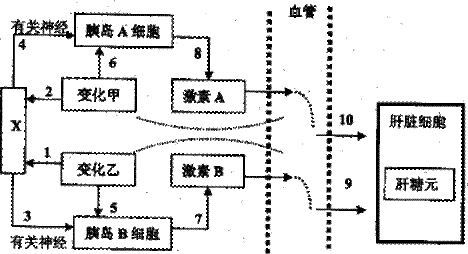
II、(15分)当人体血糖发生变化,可以直接刺激胰岛细胞,也可通过刺激下丘脑来刺激胰岛细胞,从而影响相关的激素的分泌,实现血糖的平衡调节。下图中“变化甲”、“变化乙”指的是血糖浓度的升高或下降,“X”指的是下丘脑。请据图和所学相关知识回答下列问题:
|
25.(15分)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,如果测得的pH逐渐变小且小于7,则证明NaOH溶液与稀盐酸发生了化学反应。
(1)用pH试纸测定溶液的pH时,正确的操作是: 。
(2)简述强调“测得的pH小于7”的理由: 。
方案二:先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加盐酸,如果观察到红色逐渐消失,则证明NaOH溶液与稀盐酸发生了化学反应。
该组同学在向NaOH溶液中滴加酚酞溶液时,发现了一个意外现象:氢氧化钠溶液中滴入酚酞溶液,溶液变成了红色,过了一会儿红色就消失了。该小组对这种意外现象的原因作了如下猜想:
①可能是酚酞溶液与空气中的氧气反应,使红色消失;
②可能是氢氧化钠溶液与空气中的二氧化碳反应,使红色消失。
(1)为验证猜想①,该组同学将配制的氢氧化钠溶液加热,并在液面上方滴一些植物油,然后在冷却后的溶液中滴入酚酞溶液。实验中“加热”和“滴入植物油”目的是 。实验结果表明酚酞溶液红色消失与空气中的氧气无关。
(2)为验证猜想②,该组同学做了如下实验:取了一定量的Na2CO3溶液,在其中滴入酚酞溶液,发现溶液也呈现红色。请用离子方程式解释这一现象产生的原因:
。
由此说明酚酞溶液红色消失与空气中的二氧化碳无关。
(3)该小组同学通过查阅资料得知:当氢氧化钠溶液浓度大于2mol/L时,就不会出现红色。该小组同学接着又做了对比实验:取3mol/L NaOH溶液,加入酚酞溶液后不显红色,加水稀释后,红色逐渐出现且不褪去,即可证明上述意外现象是因为取用的NaOH溶液浓度过大。
方案三:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。
 该组同学将不同浓度的盐酸和NaOH溶液各10 mL混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如下表)。
该组同学将不同浓度的盐酸和NaOH溶液各10 mL混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如下表)。
|
编号 |
盐酸 |
NaOH溶液 |
△t/℃ |
|
1 |
3.65﹪ |
2.00﹪ |
3.5 |
|
2 |
3.65﹪ |
4.00﹪ |
x |
|
3 |
7.30﹪ |
8.00﹪ |
14 |
(1)表中x = 。
(2)某同学在没使用温度计的情况下,通过右图所示装置完成了实验。则该同学
根据 (填实验现象)判断NaOH溶液与稀盐酸发生了中和反应。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com