
题目列表(包括答案和解析)
本部分包括21小题。每小题6分.共126 分。每小题只有一个选项符合题意。
1.下列关于生命活动调节的叙述,正确的是 ( )
A.注射大量甲状腺激素后,实验动物体内促甲状腺激素的含量将增加
B.凡是形响高等动物性行为的激素都是由性腺分泌的
C.动物生长激素和植物生长素的化学本质是一样的
D.刺激人的大脑皮层中央前回的顶部,可以引起下肢运动
(二)实验结果(见上右图曲线)
(1)以上实验不能准确说明赤霉素与生长素具有协同作用,其原因是
。
(2)请完善上述实验,写出你补充的实验设计,并预测整个实验的结果,同时对结果加以说明。①应补充的实验:
第一步:再取生长状况相同的豌豆幼苗,从豌豆幼苗的同一部位切取等长的茎段若干段。平均分成C、D两组;
第二步:
,在相同条件下培养;
第三步: 。
②实验结果的预测、说明:
a.
;
b.
;
c.
。
II.(8分)果蝇种群中常出现性染色体异常的个体,从而产生 不同的表现型。已知:性染色体组成为XXX和YO(细胞中只有一条Y染色体,没有X染色体)时表现为胚胎期致死,XXY时表现为雌性可育,XYY时表现为雄性可育,而XO(细胞中只有一条X染色体,没有Y染色体)表现为雄性不育。
为探究果蝇眼色的遗传方式,摩尔根做了下列杂交实验:①白眼雄果蝇×红眼雌果蝇→全部红眼;②白眼雌果蝇×红眼雄果蝇→1/2白眼雄、1/2红眼雌。但蒂更斯通过大量实验发现白眼雌果蝇与红眼雄果蝇的杂交子代有少数例外:2000~3000每只雌果蝇中出现一只白眼可育果蝇,每2000~3000只雄果蝇中出现一只红眼不育果蝇。请据上述信息回答:
(1)请用遗传图解解释蒂更斯实验中为什么会出现例外(设有关基因为B、b)。
(2)请提出一个验证蒂更斯实验中出现例外的简单思路,并预测结果。(提示:专业技术人员在光学显微镜下,可以根据有丝分裂中期染色体形态分辨性染色体和常规染色体)。
简单思路:
①取例外的果蝇分裂期的体细胞;②制做有丝分裂装片,在光学显微镜下观察;
③找出分裂期 的性染色体。
预期结果:_______________________________________________________________
(一)实验步骤:
①取生长状况相同的豌豆幼苗,从豌豆幼苗的同一部位切取等长的茎段若干段,平均分成两组;
②将两组豌豆茎切段分别放入两个标号为A、B的培养皿中(培养液成分见下图),在同样的条件下培养;
③每隔12h,测量茎切段长度一次,48h后,计算茎切段伸长的平均值
l4.如图所示,一物块位于光滑水平桌面上,用一大小为F 、方向如图所示的力去推它,使它以加速度a右运动。若保持力的方向不变而增大力的大小,则
 A . a 变大
A . a 变大
 B .a不变
B .a不变
C.a变小
D . 因为物块的质量未知,故不能确定a变化的趋势
15.氢原子的能级图如图所示。欲使一处于基态的氢原子释放出一个电子而变成氢离子,该氢原子需要吸收的能量至少是
A . 13.60eV
B .10.20eV
C . 0.54 eV
D . 27.20eV
16. 如图,闭合线圈上方有一竖直放置的条形磁铁,磁铁的N极朝下。当磁铁向下运动时(但未插入线圈内部),
如图,闭合线圈上方有一竖直放置的条形磁铁,磁铁的N极朝下。当磁铁向下运动时(但未插入线圈内部),
A.线圈中感应电流的方向与图中箭头方向相同,磁铁与线圈相互吸引
B.线圈中感应电流的方向与图中箭头方向相同,磁铁与线圈相互排斥
C. 线圈中感应电流的方向与图中箭头方向相反,磁铁与线圈相互吸引
D.线圈中感应电流的方向与图中箭头方向相反,磁铁与线圈相互排斥
17.水平放置的平行板电容器与一电池相连。在电容器的两板间有一带正电的质点处于静止平衡状态。现将电容器两板间的距离增大,则
A.电容变大,质点向上运动 B.电容变大,质点向下运动
C.电容变小,质点保持静止 D.电容变小,质点向下运动
18.两种单色光由水中射向空气时发生全反射的临界角分别为θ1、θ2 (θ1>θ2) 。用n1、n 2分别表示水对两单色光的折射率,v1、v2分别表示两单色光在水中的传播速度
A . nl<n2、v1<v2 B.nl<n2、v1>v2 C.nl>n2、v1<v2 D.nl>n2、v1>v2
19. 一定质量的气体经历一缓慢的绝热膨胀过程。设气体分子间的势能可忽略,则在此过程中
A.外界对气体做功,气体分子的平均动能增加
B.外界对气体做功,气体分子的平均动能减少
C.气体对外界做功,气体分子的平均动能增加
 D.气体对外界做功,气体分子的平均动能减少
D.气体对外界做功,气体分子的平均动能减少
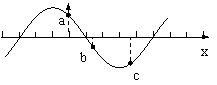
20.一列简谐横波在x轴上传播,某时刻的波形图如图所示,a 、b 、c为三个质元,a 正向上运动。由此可知
A.该波沿x 轴正方向传播
B. c 正向上运动
C. 该时刻以后,b比c先到达平衡位置
D. 该时刻以后,b比c先到达离平衡位置最远处
21.最近,科学家在望远镜中看到太阳系外某一恒星有一行星,并测得它围绕该恒星运行一周所用的时间为1200 年,它与该恒星的距离为地球到太阳距离的100 倍。 假定该行星绕恒星运行的轨道和地球绕太阳运行的轨道都是圆周,仅利用以上两个数据可以求出的量有
A.恒星质量与太阳质量之比 B.恒星密度与太阳密度之比
C.行星质量与地球质量之比 D.行星运行速度与地球公转速度之比
苍溪中学高2009级第五学段考试
理科综合能力测试
第Ⅰ卷
22.(18分)(1)以下四个实验中都要用到小球或者重锤,实验中必需测定小球或重锤质量的是 (选填下面正确选项前的代号字母)__________
A.验证动量守恒定律 B.用单摆测定重力加速度
C.验证机械能守恒定律 D.研究平抛物体的运动
 (2)在做利用双缝干涉测定光的波长的实验时,调节光源、滤光片、单缝和双缝的中心使其均位于遮光筒的中心轴线上,再调至屏上出现了干涉图样后,用直尺量得双缝到屏的距离为80.00cm,由双缝上的标识获知双缝间距为0.200 mm,光的波长为
(2)在做利用双缝干涉测定光的波长的实验时,调节光源、滤光片、单缝和双缝的中心使其均位于遮光筒的中心轴线上,再调至屏上出现了干涉图样后,用直尺量得双缝到屏的距离为80.00cm,由双缝上的标识获知双缝间距为0.200 mm,光的波长为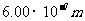 . 用测量头上的螺旋测徽器去测量,转动手轮,移动分划板使分划板中心刻线与某条明纹中心对齐,如图所示,此时螺旋测微器的读数为________mm,将此时条纹的序号定为1,其右侧的明纹序号依次是为第2条.第3条……,则从第1条明纹中心至第6条明纹中心的距离为_________mm.
. 用测量头上的螺旋测徽器去测量,转动手轮,移动分划板使分划板中心刻线与某条明纹中心对齐,如图所示,此时螺旋测微器的读数为________mm,将此时条纹的序号定为1,其右侧的明纹序号依次是为第2条.第3条……,则从第1条明纹中心至第6条明纹中心的距离为_________mm.
(3)(12分)某课题研究小组,收集了手机的电池以及从废旧收音机上拆下的电阻、电容、电感线圈等电子器件。现从这些材料中选取两个待测元件来进行研究,一是电阻Rx(约为2kΩ),二是手机中常用的锂电池(电动势E标称值为3.7V,允许最大放电电流为100mA)。在操作台上还准备了如下实验器材:
A.电压表V(量程4V,内阻RV约为10kΩ) B.电流表A1(量程100mA,内阻RAl约为5Ω)
C.电流表A2(量程2mA,内阻RA2约为50Ω) D.滑动变阻器R(0-40Ω,额定电流1A)
E.电阻箱R0 (0-999. 9Ω) F.开关S一只、导线若干
①为了测定电阻Rx的阻值,小组的一位成员,设计了如图甲所示的电路原理图,电源用待测的锂电池,则电流表应该选用 (选填“A1”或“A2”);他用电压表的读数除以电流表的读数作为Rx的测得值,则测得值 真实值(选填“大小”或“小于”)。
②小组的另一位成员,设计了如图乙所示的电路原理图来测量锂电池的电动势E和内阻r.
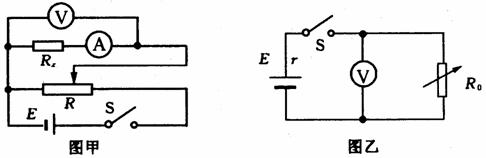
该同学闭合开关S,调整电阻箱的阻值为R1时,读出电压表的示数为U1;电阻箱的阻值为R2时,读出电压表的示数为U2,可求得该电池的电动势,其表达式为E= _______。
为了便于分析,一般采用线性图象处理数据,可以改变电阻箱阻值,取得多组数据,请写出与线性图象对应的相关物理量间的函数关系式: 。
23. ( 16分)如图所示,在倾角为θ的光滑斜面上有两个用轻质弹簧相连接的物块A 、B .它们的质量分别为mA、mB,弹簧的劲度系数为k , C为一固定挡板。系统处于静止状态。现开始用一恒力F沿斜面方向拉物块A 使之向上运动,求物块B 刚要离开C时物块A 的加速度a 和从开始到此时物块A 的位移d。重力加速度为g。

24.(18分)如图所示,第四象限内有互相正交的匀强电场E与匀强磁场B1,E的大小为
1.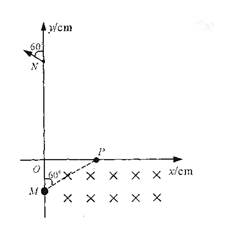 5×103V/m,Bl大小为0。5T;第一象限的某个矩形区域内,有方向垂直纸面的匀强磁场B2,磁场的下边界与x轴重合.一质量m=1×10-14kg、电荷量q=2×l0-10C的带正电微粒以某一速度v沿与y轴正方向60°角从M点沿直线运动,经P点即进入处于第一象限内的磁场B2区域.一段时间后,小球经过y轴上的N点并与y轴正方向成60°角的方向飞出。M点的坐标为(0,-10),N点的坐标为(0,30),不计粒子重力,g取10m/s2.则求:
5×103V/m,Bl大小为0。5T;第一象限的某个矩形区域内,有方向垂直纸面的匀强磁场B2,磁场的下边界与x轴重合.一质量m=1×10-14kg、电荷量q=2×l0-10C的带正电微粒以某一速度v沿与y轴正方向60°角从M点沿直线运动,经P点即进入处于第一象限内的磁场B2区域.一段时间后,小球经过y轴上的N点并与y轴正方向成60°角的方向飞出。M点的坐标为(0,-10),N点的坐标为(0,30),不计粒子重力,g取10m/s2.则求:
(1)微粒运动速度v的大小;
(2)匀强磁场B2的大小;
(3)B2磁场区域的最小面积。
25、(20分)如图所示,一边长L=0.5m,质量m1=2kg,电阻R= Ω的正方形导体线框abcd,与一质量为m2=0.5kg的物体通过轻质细线跨过两个滑轮相连,起初ad边距磁场的上边缘为h1=
Ω的正方形导体线框abcd,与一质量为m2=0.5kg的物体通过轻质细线跨过两个滑轮相连,起初ad边距磁场的上边缘为h1= m,磁场的高度为h2=
m,磁场的高度为h2= m,磁感应强度为B=2T,物块放在倾角
m,磁感应强度为B=2T,物块放在倾角 足够长的斜面上,且与斜面间的动摩擦因数μ=0.5,现将线框由静止释放,经一段时间以后发现当ad边从磁场的下边缘穿出时,线框恰好做匀速运动。其他摩擦及空气阻力不计,(g取10m/s2)求:
足够长的斜面上,且与斜面间的动摩擦因数μ=0.5,现将线框由静止释放,经一段时间以后发现当ad边从磁场的下边缘穿出时,线框恰好做匀速运动。其他摩擦及空气阻力不计,(g取10m/s2)求:
 (1)线框ad边从磁场下边缘穿出时的速度v2;
(1)线框ad边从磁场下边缘穿出时的速度v2;
(2)线框刚刚全部进入磁场时速度v1的大小;
(3)整个过程中线框中产生的焦耳热;
(4)半定量地画出物块的速度与时间的关系图象(即不标时间坐标值但要标出速度坐标值,不必写计算过程,只需画出图象)。
26.(15分)如图所示,B、K、R、Y和G均为元素周期表前20号元素的代号,它们还满足下列关系:
①相邻或相交的两元素均能形成常见化合物。其中Y元素原子的最外层电子数是内层电子数的0.6倍,且Y、K两元素同主族。
 ②相邻、相交的三元素也能形成常见化合物。其中由K、G、R三元素组成的化合物甲是大理石的主要成分。
②相邻、相交的三元素也能形成常见化合物。其中由K、G、R三元素组成的化合物甲是大理石的主要成分。
③B是宇宙中最丰富的元素,它也是周期表中原子半径最小的元素
回答下列问题:
(1)K元素在元素周期表中的位置是______ ______。G和R所形成的常见化合物中含有的化学键有_________(填字母)。
a.离子键 b.极性共价健 c.非极性共价健 d.氢健
(2)写出甲在某种工业生产中所发生反应的化学方程式:_________ __________________。
(3)由B和K所形成的化合物乙与由Y和K所形成的化合物丙能发生氧化还原反应,写出该反应的化学方程式_______________________________________。
(4)已知铁元素能与R、K两种元素形成原子个数比为1:2:4的化合物丁,当加热丁粉末时,只生成一种可使燃着木条熄灭的无色无味气体及一种反应活性很高能充当食品抗氧化剂的固体粉末。写出丁受热分解的化学方程式_______________________________________。
27.(16分)NaClO和KAl(SO4)2都是重要的化工产品,均可应用于造纸等工业。
(1)NaClO溶液pH>7,原因是(用离子反应方程式表示) 。
(2)根据NaClO的性质推测,在纸浆中加入NaClO溶液的目的是 ;某品牌消毒液主要成分为NaClO,可用于各类家具用品、餐具等的消毒,须密封、置于阴暗处保存。从该消毒液的保存要求分析,用化学用语表示导致其失效的原因:
____________________________________;______________________________________。
(3)在1 mol/L 的KAl(SO4)2溶液中离子浓度由大到小的顺序是 。
(4)某小组同学进行了探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。
① 向盛有饱和NaClO的烧瓶中加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀 。反应的离子方程式是: 。
② 将烧瓶中的混合液在强光照射下,不久烧瓶中有黄绿色气体产生。将产生的气体通过足量的NaOH溶液充分吸收后,逸出的余气能使带火星的木条复燃。写出混合液中反应的化学方程式: 。
 (5)若将V1 mL 0.1mol/L KAl(SO4)2溶液和V2 mL 0.1mol/LBa(OH)2溶液混合。当产生沉淀的物质的量最大时,V1:V2
= 。
(5)若将V1 mL 0.1mol/L KAl(SO4)2溶液和V2 mL 0.1mol/LBa(OH)2溶液混合。当产生沉淀的物质的量最大时,V1:V2
= 。
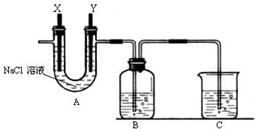
28.(16分) 某化学兴趣小组利用废铁屑制取FeCl3∙6H2O晶体。主要步骤如下:
①往工业废铁屑中加入适量的纯碱溶液,加热数分钟,用倾析法洗净废铁屑。
②洗净后的废铁屑放在烧杯内,用过量的工业盐酸浸泡至不再产生气泡,过滤。
③按上图组装仪器,并检查装置的气密性,将②得到的滤液放入试剂瓶B中。
④在石墨电极X.Y上连接直流电源通电,待FeCl2全部被氧化后断开电源。
⑤试剂瓶B中的溶液经过一系列操作;可得FeCl3∙6H2O晶体。
请回答下列问题:
(1)步骤①的目的是 。
(2)A中的X极应连接电源的 极,A中反应化学方程式是 。
B中溶液颜色的变化 。
(3)为检验B中FeCl2已全部转化为FeCl3,可以选用的试剂是 。
A.苯酚 B.酸性KMnO4溶液 C.KSCN溶液 D.NaOH溶液
(4)在整个实验过程中,盐酸必须保持过量,主要原因是 。
(5)C中的烧杯盛放的试剂以及其作用是 。
(6)由步骤⑤试剂瓶B中的溶液制得FeCl3∙6H2O晶体,需要进行的操作如下,其顺序依次是(填序号) 。
A.加热浓缩 B.洗涤 C.过滤 D.冷却结晶
29.(13分) 某烃A 2.9 g完全燃烧生成8.8 g CO2和4.5 g H2O,它的一氯取代产物有4种,B、C是其中的两种。B和C分别与强碱的醇溶液共热,都只能得到有机化合物D。请根据图示的各有机物之间的转化填空:
(1)H的分子式为: ;
(2)写出结构简式:C ,E ;
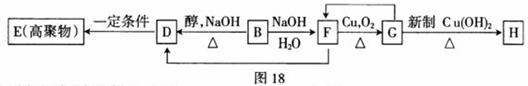
(3)写出下列反应的类型:F→C B→D ;
(4)物质D的名称: ;
(5)写出B→F的化学方程式: ;
(6)写出D→H的化学方程式: 。
30.(22分)回答下列I、II小题:
I.(10分)近期研究表明,我们面对新信息时大脑中需要建立起一个新的处理路径。此时,被新信息激活的神经元会生长出新的突起,一直延伸到邻近的神经元,形成突触。突触一旦形成,兴奋就可以从一个神经元传到另外一个神经元,我们也就获得了新的信息。若建立起的突触失灵了,大脑就忘记了这个信息。
(1)大脑在初次学习时需要的时间比再次学习时需要的时间长,原因是再次学习时不需要______________________;而随年龄的增长,神经元衰老,获得新信息需要的时间更长,是由于_______________________。
(2)突触形成后,兴奋在神经纤维上的传导是___________(单向/双向)。
(3)有关研究表明,人在安静时大脑的产热量是运动时的6倍,则人在_________时更容易记忆,原因是在该情况下脑细胞__________________强。
II.(12分)某池塘的水层由上至下分别为表水层、斜温层、静水层和底泥层,在冬夏两季分别对该池塘的温度和氧气进行垂直结构分析,统计数据如下表:
|
水层 |
表水层 |
斜温层 |
静水层 |
底泥层 |
|
|
温度(℃) |
夏 |
25 |
14 |
8 |
4 |
|
冬 |
2 |
3.8 |
4 |
4 |
|
|
O2(μL·L-1) |
夏 |
9.5 |
6.2 |
3.4 |
0.2 |
|
冬 |
12 |
11.8 |
10.6 |
10.2 |
(1)从表中数据分析,夏季池塘中随着水深的增加,O2含量下降,引起这种现象的非生物因素主要是________________________;夏季各水层的O2含量低于冬季,其生物学原因是____________________________________________________。
(2)夏季底泥层和表水层相比,O2含量非常低的原因是____________________。
(3)某同学为了测定斜温层水样的总光合作用生产量,先测出该水层的原始溶氧量,再取两个无色透明玻璃瓶A、B,其中A瓶先包上黑胶布,再包以锡箔,B瓶不包裹。在A、B两瓶内装入等量水样,密封后沉入水中一定深度,24小时后取出测定溶氧量。
①在实验中,A、B两瓶密封后沉入水中“一定深度”,此深度指______________深度。
②A瓶中所测得的数据可以得知正常的____________________量,B瓶中含氧量的变化可以确定____________________量。
31.(20分)回答下列Ⅰ、Ⅱ小题
 I.(12分)赤霉素能促进豌豆茎节间的伸长,生长素也可以促进茎的仲长。某同学设计了如下的实验,验证赤霉素与生长素具有协同作用。
I.(12分)赤霉素能促进豌豆茎节间的伸长,生长素也可以促进茎的仲长。某同学设计了如下的实验,验证赤霉素与生长素具有协同作用。
13.浓度均为0.1 mol·L-1的小苏打溶液与烧碱溶液等体积混合,所得溶液中各离子浓度关系13.以惰性电极电解CuSO4溶液。一段时间后取出电极,加入9.8gCu(OH)2后溶液与电解前相同,则电解时电路中流过的电子为
A.0.4mol B.0.3mol C.0.2mol D.0.1mol
12.己烯雌酚是一种激素类药物,结构如图5所示,下列有关叙述中不正确的是
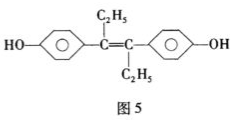 A.1mol该有机物最多与7 mol H2发生反应
A.1mol该有机物最多与7 mol H2发生反应
B.该有机物的分子式为C18H20O2
C.1mol该有机物最多与3 mol Br2发生反应
D.该有机物分子中,可能有18个碳原子共平面
11.下列各组离子能在指定溶液中共存的是
A.酸性溶液中:K+、Na+、Fe2+、SO42-、MnO4-
B.使pH试纸变红的溶液中:Na+、CO32-、S2-、AlO2-
C.水电离的c(H+)=10-13mol·L-1的溶液中:Cl-、HCO3-、NO3-、NH4+
D.加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、Na+、SO42-
10. NA代表阿伏加德罗常数,下列说法正确的是
A.标准状况下,2.24 L NH3气体溶于1L水中得到0.1 mol/L的氨水
B.质子总数为10 NA的重水(D2O)的质量为20 g
C.8.96L乙炔和乙醛混合气体.在氧气中完全燃烧.消耗氧气的分子数为NA
D.0.2 mol/L的K2CO3溶液500 mL中含有的离子总数为0.3 NA
9.下列文字表述与反应方程式对应且正确的是:
A.新制的得硫酸亚铁溶液和过氧化氢溶液反应:Fe2++2H++H2O2==Fe3++2H2O
B.硫化钾晶体溶于水:S2-+2H2O 2OH-+H2S
2OH-+H2S

 C.实验室用液溴和苯在催化剂作用下制溴苯:
C.实验室用液溴和苯在催化剂作用下制溴苯:
D.亚硫酸氢铵和与足量的氢氧化钠的反应:NH4++OH_= NH3↑+H2O
8.下列实验操作或对实验事实的叙述正确的是
①用碱式滴定管量取20.00 mL 0.10 mol/L KMnO4溶液;②配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止;③做硫酸铜晶体结晶水含量的测定实验,加热后的坩埚冷却时未放入干燥器,将导致所测结果数据偏高;④为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量;⑤测定中和反应的反应热时,利用玻璃搅拌器匀速搅拌;⑥保存FeCl2溶液时常加入少量铁粉以防止Fe2+水解。
A.②⑤ B.①②⑤ C.④⑥ D.②④⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com