
题目列表(包括答案和解析)
1. 高中生物实验常用到盐酸和酒精,以下对盐酸和酒精使用描述不正确的是( )。
A.低温诱导植物染色体数目的变化和观察根尖分生组织细胞的有丝分裂实验中用15%的盐酸和95%的酒精混合作解离液
B.观察DNA、RNA在细胞中的分布实验中,水解时需加入30mL质量分数为8%的盐酸
C.用花生子叶观察脂肪颗粒时,需用体积分数为95%的乙醇洗去浮色
D.橙色的重铬酸钾溶液在酸性条件下与乙醇发生反应变成灰绿色
32.(10分)(生物-现代生物科技专题)
2008年诺贝尔化学奖授予了三位在研究绿色荧光蛋白(GFP)方面做出突出贡献的科学家。绿色荧光蛋白能在蓝光或紫外光的激发下发出荧光,这样借助GFP发出的荧光 就可以跟踪蛋白质在细胞内部的移动情况,帮助推断蛋白质的功能。下图为我国首例绿色荧光蛋白(GFP)转基因克隆猪的培育过程示意图,据图回答:
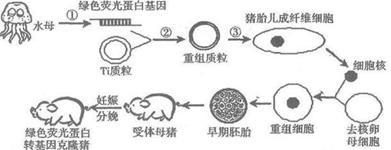
(1) 绿色荧光蛋白基因在该实验中是 基因。在构建基因表达载体中,启动子位于基因的首端,是___________ _酶识别和结合的部位,有了它才能驱动基因转录出 mRNA 。
(2)为了获得更多的猪卵母细胞,可通过对母猪注射促性腺激素的方法,进行 处理,并将所采集到的卵母细胞在体外培养才可通过显微操作将其细胞核去除。
(3)早期胚胎的培养液成分较复杂,除一些无机盐和有机盐类外,还需添加维生素、激素、氨基酸、核苷酸等营养成分,以及 等物质。
(4)绿色荧光蛋白转基因克隆猪的培育过程属于 生殖。
31.(化学--有机化学基础,13分)
丙烯是重要的工业原料,以丙烯为原料合成有机玻璃和药物喹啉的流程如下:

回答下列问题:
(1)结构简式A为 ,C为 ;
(2)①-⑩反应中属于属于消去反应的有 ;
(3)设计反应①、②的目的是 ;
(4)D的同分异构体E能进行银镜反应,分子中有两种不同化学环境的氢原子,其个数比为2∶1,则E的结构简式为 ;
(5)反应⑦的化学反应类型是 。
30.(化学--物质结构与性质,13分)
氮元素可形成卤化物、叠氮化物及络合物等。
(1)NF3构型为三角锥体,沸点-129 ℃;可在铜催化下由F2和过量NH3反应得到。则NF3属于 晶体,写出制备 NF3的化学反应方程式: 。
(2)氢叠氮酸(HN3)是一种弱酸,它的酸性类似于醋酸,微弱电离出H+和N3-。叠氮化物、氰化物能与Fe3+及Cu2+及Co3+等形成络合物,如:Co[(N3)(NH3)5]SO4、(Fe(CN)64-。写出钴原子在基态时的价电子排布式: 。Co[(N3)(NH3)5]SO4中钴的配位数为 。
(3)化学式为Pt(NH3)2Cl2的化合物有两种异构体,其中一种异构体易溶于水,则此种化合物是 (填“极性”、“非极性”)分子。
(4)由叠氮化钠(NaN3)热分解可得纯N2:2NaN3(s)=2Na(l)+3N2(g),有关说法正确的是 (选填序号)
 A.NaN3与HN3结构类似,都存在N3-离子
A.NaN3与HN3结构类似,都存在N3-离子
B.第一电离能(I1):N>P>S
C.钠晶胞结构如右图,该晶胞分摊2个钠原子
D.氮气常温下很稳定,是因为氮的电负性小
29.[物理――选修3-5](本题共两小题,每小题6分,共12分。每小题只有一个选项符合题意。)
(1)甲、乙两车相向运动,碰撞后一同沿乙车的方向运动,这是因为______。(填选项前的编号)
① 乙车的质量比甲车的大
② 乙车的速度比甲车的大
③ 乙车的动量比甲车的大
④ 乙对甲的作用力大于甲对乙的作用力
(2)质子和中子的质量分别为 和
和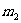 ,当这两种核子结合成氘核时,并以
,当这两种核子结合成氘核时,并以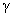 射线的形式放出能量E。已知普朗克常量为
射线的形式放出能量E。已知普朗克常量为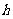 ,真空中的光速为
,真空中的光速为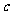 ,则氘核的质量和
,则氘核的质量和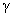 射线的周期的表达式分别为 (填代号)
射线的周期的表达式分别为 (填代号)
①.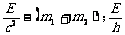 ②.
②.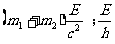
③.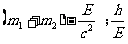 ④.
④.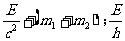
28.[物理――选修3-3](本题共两小题,每小题6分,共12分。每小题只有一个选项符合题意。)
(1)根据下面哪组数据可算出阿伏加德罗常数的是____。(填选项前的编号)
① 水的密度和水的摩尔质量 ② 水分子的质量和水的摩尔质量
③ 水分子的体积和水分子的质量 ④ 水的摩尔质量和水分子的体积
(2)在温度均匀且恒定的水池中,有一小气泡正在缓慢向上浮起,体积逐渐膨胀,在气泡上浮的过程中,气泡内的气体______。(填选项前的编号)
① 向外界放出热量
② 与外界不发生热传递,其内能不变
③ 对外界做功,其内能减少
④ 对外界做功,同时从水中吸收热量,其内能不变
27.(15分)
回答小麦遗传育种的有关问题:
(1)小麦是自花授粉植物,为使小麦产量、品质、抗性等性状在个体间、年度间表现一致,可以从麦田留种繁殖,因为组成小麦某一品种的所有植株都是 。通过自交产生的后代,其性状表现 。
(2)让光颖、抗锈、无芒(ddRRAA)小麦和毛颖、感锈、有芒(DDrraa)小麦杂交(三对相对性状自由组合),得F1,F1自交得F2。若要从F2自交的后代F3中选出毛颖、抗锈、无芒(DDRRAA)的小麦10株,则在F2群体中至少应选择表现型为毛颖、抗锈、无芒(D_R_A_)小麦 株。 ,
(3)若只考虑小麦的无芒(A)和有芒(a)一对相对性状,则小麦三倍体的基因型有 。
(4)在小麦的一个野生群体X中,如果抗锈病和感染锈病这对相对性状的显隐性未知,发现抗锈病对感染锈病的性状表现比例是3∶1,这是否说明抗锈病是显性的(假设这对相对性状是由一对等位基因引起的)?为什么? 。
选考部分
第Ⅱ卷选考部分共5题,共35分。其中,第28、29题为物理题,第30、31题为为化学题,考生从两道物理题、两道化学题中各任选一题作答,若第28、29题都作答,则按第28题计分,若第30 、31题都作答,则按第30题计分;第32题为生物题,是必答题。请将答案填写在答题卡选答区域的指定位置上。
26.(25分)
I.“漳州水仙花”及其图案是我国第二个花卉类驰名商标,是我国人民春节时最 喜欢的室内陈设的花卉之一。为了研究人工合成的生长素类似物a-萘乙酸 (NAA)是否对植物的开花具有影响,某研究小组以水仙鳞茎为实验材料进行 探究。请根据所给的材料,完成实验设计的思路。
实验材料:品种、大小一致水仙鳞茎20个,0.1mg/mL的NAA溶液适量。
实验设计的思路:
(1)材料处理:需要先剥去水仙鳞茎部分鳞片叶;
(2)实验组(A组)为 ;
(3)对照组(B组)为 ;
(4)因变量为 ;
(5)无关变量有 (写出2点)。
(6)最可能的实验结果和结论: 。
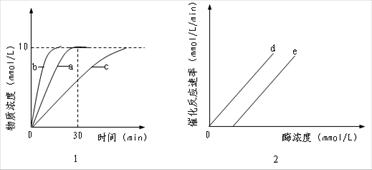 Ⅱ.动物脑组织中含有丰富的谷氨酸脱羧酶,能专一催化1mol谷氨酸分解为1mol γ-氨基丁酸和1molCO2。某科研小组从小鼠的脑中得到该酶后,对该酶的催化反应过程进行研究,结果见下图1和图2。
Ⅱ.动物脑组织中含有丰富的谷氨酸脱羧酶,能专一催化1mol谷氨酸分解为1mol γ-氨基丁酸和1molCO2。某科研小组从小鼠的脑中得到该酶后,对该酶的催化反应过程进行研究,结果见下图1和图2。
(1)图1中的a是在谷氨酸起始浓度为10mmol/L、最适温度、最适pH值、酶 浓 度固定的条件下得到的曲线。请给该曲线拟定一个合理的名称 。b、c两曲线是通过改变温度、酸碱度或酶浓度得到的曲线,图1中曲线b产生的可能原因是 ;30min后a曲线不再上升的原因可能是 。
(2)图2是在反应物浓度过量添加下,酶催化反应速率随酶浓度变化曲线。图2中曲线e是在谷氨酸脱羧酶和谷氨酸混合溶液中加入一定量的汞离子后,得到的酶催化反应速率随酶浓度变化的曲线(汞离子能与谷氨酸脱羧酸按比例牢固结合不可解离,迅速使酶失活)。你认为出现这种现象的最可能原因是: 使一定量的酶失活,当加入的酶量 后,继续加入的酶开始表现酶活力,此时酶的催化反应速率与酶浓度变化的直线关系不变。
25.(15分)
铁在冷的浓硫酸中能发生钝化。某兴趣小组同学发现将一定量的铁与浓硫酸加热时,铁完全溶解,得到溶液A,并产生大量气体B。实验室现有下列试剂: 0.01 mol/L 酸性KMnO4溶液、0.1 mol/L KI溶液、3%H2O2溶液、淀粉溶液、蒸馏水。请你协助他们探究所得溶液和气体的成分,并将有关实验操作、预期现象和结论填入下列表格中。
[提出猜想]
Ⅰ.所得溶液中的金属离子可能含有Fe2+和Fe3+中的一种或两种;
Ⅱ.所得气体中可能含有 中的一种或两种。
Ⅲ.任意写出一个铁与浓硫酸加热时,可能发生的有关反应方程式
[实验探究]
|
|
实验操作 |
预期现象 |
结 论 |
|
验证猜想Ⅰ |
步骤①:取少量溶液A,滴入0.01 mol/L 酸性KMnO4溶液 |
|
|
|
步骤②: |
|
含有Fe3+ |
|
|
验证猜想Ⅱ |
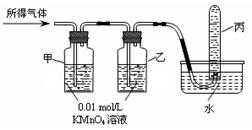
将所得气体B通入如下图装置 |
|
含有两种气体 |
[问题讨论]
 有同学提出,若另外选用KSCN溶液,则仅利用KSCN和H2O2两种溶液即可完成猜想Ⅰ的所有探究,请对该观点进行评价:
有同学提出,若另外选用KSCN溶液,则仅利用KSCN和H2O2两种溶液即可完成猜想Ⅰ的所有探究,请对该观点进行评价:
。
24.(15分)减少SO2的排放、回收利用SO2成为世界性的研究课题。我国研究人员研制的,利用低品位软锰矿浆(主要成分是MnO2)吸收废渣高温焙烧产生的SO2,制备硫酸锰的生产流程如下:
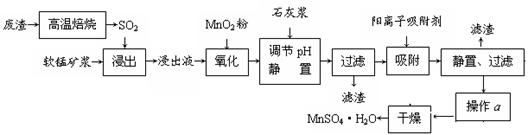
 浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、 Pb2+等其他金属离子。(提示:①在工业上,用沉淀法不能完全除去的离子还可以用 吸附法除去②有关金属离子的半径以及形成氢氧化物沉淀时的pH见下表③阳离子 吸附剂吸附金属离子的效果见下图。 ④已知PbO2的氧化性大于MnO2。)
浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、 Pb2+等其他金属离子。(提示:①在工业上,用沉淀法不能完全除去的离子还可以用 吸附法除去②有关金属离子的半径以及形成氢氧化物沉淀时的pH见下表③阳离子 吸附剂吸附金属离子的效果见下图。 ④已知PbO2的氧化性大于MnO2。)
|
离子 |
离子半径(pm) |
开始沉淀pH |
完全沉淀pH |
|
Fe2+ |
74 |
7.6 |
9.7 |
|
Fe3+ |
64 |
2.7 |
3.7 |
|
Al3+ |
50 |
3.8 |
4.7 |
|
Mn2+ |
80 |
8.3 |
9.8 |
|
Pb2+ |
121 |
8.0 |
8.8 |
|
Ca2+ |
99 |
- |
- |
请回答下列问题:
(1)写出浸出过程中主要反应的一个化学反应方程式 , 氧化过程中主要反应的一个离子反应方程式 。
(2)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至 。
(3)决定阳离子吸附剂吸附效果的因素是 (填写序号)。
a.溶液的pH b.金属离子的电荷 c.金属离子的半径 d.吸附时间
(4)操作a包括 过滤、洗涤等过程。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com