
题目列表(包括答案和解析)
9.下列做法存在安全隐患的是
①将水沿着烧杯内壁缓缓加入浓硫酸中,用玻璃棒不断搅拌;②实验室制取氯气结束时,
先撤水中的导管后撤酒精灯;③取用金属Na或K时,剩余的药品要放回原瓶;④夜间厨
房发生煤气泄漏时,应立即开灯检查煤气泄漏的原因,并打开所有的门窗通风;⑤干冰是
干粉灭火器的常见成分,可用作镁、铝等金属的灭火;⑥做苯酚性质实验时,因为常温时
苯酚在水中的溶解度较小,所以可以将废液直接排入下水道。
 A.①④⑤⑥ B.①②③④ C①③④⑤ D.全部
A.①④⑤⑥ B.①②③④ C①③④⑤ D.全部
8.下列说法正确的是
A.二氧化碳分子内存在非极性共价键和分子间作用力
B.甲烷、氨和水都是由极性键结合而成的极性分子
C.同主族不同元素的最高价氧化物,一定具有相同的晶体结构
D.氟化氢的沸点高于氯化氢,正丁烷的沸点高于异丁烷
7.用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
A.常温常压下,16g臭氧中含有的氧原子数目为1/3NA
B.标准状况下,2.24L三氧化硫所含的分子数为0.1NA
C.电解精炼铜时,若转移了NA个电子,则阴极析出32 g铜
D.1 mol FeCl3跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA
6.下列表示物质结构的化学用语或模型图正确的是
A.CO2的比例模型 B.H2O2的电子式:H+
B.H2O2的电子式:H+ H+
H+
C.HClO的结构式:H一O一Cl D. 的原子结构示意图:
的原子结构示意图:
31.(22分)请回答下列有关生物多样性的问题:
(1)2008年奥运吉祥物福娃“迎迎”原型来自我国青藏高原特有的动物藏羚羊,分布在可可西里的自然保护区。人们保护藏羚羊的目的是 ( )
A.保护可可西里的植被 B.保护生态系统的多样性
C.防止外来物种的入侵 D.保护遗传的多样性和物种的多样性
(2)从进化角度来看,生物性状具有多样性是 的结果。
(3)从红豆杉的树皮和针叶中分离纯化出的紫杉醇,是一种对子宫癌、乳腺癌、白血病等癌症有特殊疗效的抗癌药物。体现了生物多样性的 。
(4)为了保护红豆杉植株,人们正在探究应用植物组织培养的方法,以便从大量培养的红豆杉的 组织中获得紫杉醇;为了较快地增加红豆杉植株的数量,用诱导离体的组织形成 结构来制备人工红豆杉种子。
(5)某生态学家以“保护和利用草原生态系统生物多样性”为课题,对某草原进行了几项专题研究,并绘制了单位面积的放牧量与生产者的净生产量的关系图,如右图所示,图中的横虚线代表未放牧时,草原中生产者的净生产量。请据图分析并回答下列问题:
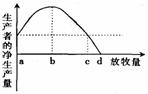 ①放牧量应控制在图中 点之间。
为什么?
。
①放牧量应控制在图中 点之间。
为什么?
。
②如果该草原生态系统的放牧量长期在图中c点以上,会造成草原生物多样性 。
③生态学家建议在此草原中适当引入鼠类的天敌、草食性昆虫的天敌。从能量流动的角度看,其目的是 。
④草原生态系统如果发生大火后,随着时间推移,该地方的群落结构重新趋于稳定。其需要时间相对森林生态系统 ,说明草原生态系统的稳定性特点是 。
30.(20分)报春花的花色表现为白色(只含白色素)和黄色(含黄色锦葵色素)一对相对性状,由两对等位基因(A和a,B和b)共同控制,其生化机制如右图所示。据此回答;
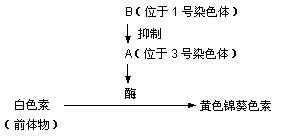
(1)上述基因通过____________________________________,从而控制报春花的花色性状。开黄花的报春花植株的基因型可能是 ______________ 。
(2)为了培育出能稳定遗传的黄色品种,某同学用开白花的纯种植株设计了如下实验,请帮助他完成。
①选择基因型为 、 的两个品种进行杂交,得到F1种子;
②F1种子种下得F1植株,F1自交得F2种子;
③F2种子种下得F2植株,F2自交,并选择开黄花植株的种子混合留种;
④重复步骤③若干代,直到 。
(3)根据上述实验,回答相关问题:
①F1植株能产生比例相等的四种配子,说明其遵循_______________________遗传规律。
②由于报春花的雌蕊和雄蕊不等长,在自然状态下可以进行异花传粉。为使上述实验更完善,应该怎样处理? 。
③F2植株中开黄花的植株上所结的种子中黄色纯合子占 。
④有的同学认为这不是一个最佳方案,请你在原方案的基础上进行修改,使培育年限最短。请简要概述你的方案: 。
29. (14分)下图中A、B、C、D、E、F、G均为有机化合物。
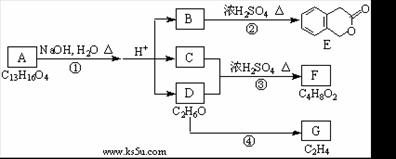
根据上图回答问题:
(1)D的化学名称是_____________;
(2)反应③的化学方程式是 ;
反应④的化学方程式是 ;
(3)B的分子式是_____________;
A的结构简式是__________________________;反应①的反应类型是___________;
(4)符合下列3个条件的B的同分异构体的结构简式(任写两个) ;
①含有邻二取代苯环结构; ②与B有相同官能团; ③不与FeCl3溶液发生显色反应。
28. (13分)
A-L为中学化学已学过的物质,相互间有如下转化关系(部分产物如H2O已略去)。其中C、D、G、I均为短周期元素形成的单质,D、G、I为常见气态单质;D的原子最外层电子数是次外层电子数的3倍;C、G的元素同周期,且原子最外层电子数相差4,它们的简单离子电子层结构不同;K为红棕色固体粉末。

请回答下列问题:
(1)D的元素与I的元素能形成原子个数比为1∶1的共价化合物,其电子式为 。
(2)写出用石墨作电极,电解E的水溶液的离子方程式 。气体G在 极逸出(填“阳”或“阴”)。
(3)写出C+K→L+A的化学方程式: ;该反应被称为 反应。
(4)写出A+F→J的离子方程式 。
27. (17分)现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。
(17分)现有某铁碳合金,某化学兴趣小组为了测定铁碳合金中铁的质量分数,并探究浓硫酸的某些性质,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。
Ⅰ 探究浓硫酸的某些性质
(1)按图示的连接装置,检查装置的气密性,称量E的质量。
(2)将m g铁碳合金样品放入A中,再加入适量的浓硫酸。仪器A的名称为______________。
 未点燃酒精灯前,A、B均无明显现象,其原因是:
_______________________________________。
未点燃酒精灯前,A、B均无明显现象,其原因是:
_______________________________________。
(3)点燃酒精灯一段时间后,A、B中可观察到明显的现象。
写出A中发生反应的化学方程式___________、 。B中的现象是______________,由此可知浓硫酸具有_________性。
(4)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是_____________________________________。
Ⅱ 测定铁的质量分数
(5)待A中不再逸出气体时,停止加热,拆下E并称重。E增重b g。
铁碳合金中铁的质量分数为_____________________(写表达式)。
(6)某同学认为上述方法较复杂,使用下图所示的装置和其他常用实验仪器测定某些数据即可。为了快速准确的计算出铁的质量分数,最简便的实验操作是_____________(填写代号)。
A. 用排水法测定H2的体积
B. 反应结束后,过滤、洗涤、干燥、称量残渣的质量
C. 测定反应前后装置和药品的总质量
26.(14分)U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。请回答下列问题: (1)V的单质分子的结构式为 ;XW的电子式为 。
(2)U元素形成的同素异形体的晶体类型可能是(填序号) 。
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体 (3)U、V、W形成的10电子氢化物中,U、V的氢化物沸点较低的是(写化学式) ______ ;V、W的氢化物分子结合H+能力较强的是(写化学式) ,用一个离子方程式加以证明 。 (4)YW2气体通人BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为 ,由此可知VW和YW2还原性较强的是(写化学式) 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com