
题目列表(包括答案和解析)
28.向100克稀硫酸中滴加硝酸钡溶液直到不再产生沉淀,共消耗100克硝酸钡溶液。把
得到的沉淀洗涤、干燥后,称其质量为23.3克。求反应后所得溶液中溶质的质量分数。

本资料由《七彩教育网》 提供!
27.(10分)蕾蕾同学跟妈妈学烧紫甘蓝(紫卷心菜),用油炒后加入
食醋,发现紫色的叶片立即变红,激发了她的探究欲望。
[提出问题]紫甘蓝的汁液能做酸碱指示剂么?
[进行实验]取紫甘蓝叶片少许在研钵中捣烂,用少量水浸泡,滤出蓝紫色的汁液。将汁液
分别滴入下列液体中,观察其显示的颜色并记录。
|
液体名称 |
白醋 |
蒸馏水 |
食盐溶液 |
氢氧化钠溶液 |
|
紫甘蓝溶液显示的颜色 |
红色 |
蓝紫色 |
蓝紫色 |
蓝色 |
[得出结论]紫甘蓝的汁液__________(填“能”或“不能”)作酸碱指示剂。
[拓展应用]柠檬酸是制碳酸饮料的原料之一,为探究其固体是否显酸性,蕾蕾同学联想到教材上二氧化碳相关实验的设计,准备了三朵用紫甘蓝的汁液染成的蓝紫色的干燥小花。
取干燥的花①和喷上水的花②,分别放入盛满二氧化碳的两个集气瓶中,发现花①不变色,
花②变成了_______色。在干燥的花③上直接撒少量柠檬酸固体,花不变色,说明了_________
______________;再向该花喷水,蓝紫色的花上出现了红色。
[反思]上述的花变色均与水有关,水的作用分别是:
花②中____________________________________________;
花③中)___________________________________________。
[反思2]如何证明碳酸饮料中含柠檬酸?蕾蕾同学用试管取了少量碳酸饮料,将其加热煮
沸(煮沸的目的是________________________________),然后加入______________,观察
到__________________________________现象,就证明了碳酸饮料中含柠檬酸。
26.(6分)下函是配制50克溶质质量分数为5%的氯化钠溶液的实验操作。

请回答下列问题:
(1)该实验的正确操作顺序为_____________________________________(填序号);
(2)称取2.5克固体氯化钠:在天平两盘各放一张质量相同的纸片,天平平衡。然后往
左盘放2克砝码,游码调至0.5克处,往右盘加氯化钠固体至天平重新平衡。请改正称量中
的错误操作________________________________,如果按错误操作的结果计算所配溶液中溶质
的质量分数为____________(结果保留到0.1%位);
(3)在量取水时,最好选择的量筒为_________________(填序号①10mL@50~L③100mL)(水
的密度为1g/ ),将量筒中的水倒入烧杯时,量筒中有少量水残余,则会引起所配溶液的
),将量筒中的水倒入烧杯时,量筒中有少量水残余,则会引起所配溶液的
 溶质量分数为____________(填“偏大”、“偏小“或”不变“)
溶质量分数为____________(填“偏大”、“偏小“或”不变“)
(4)按正确的操作溶解配制后,将溶液装瓶并贴好标签。
请填写右侧的标签。
25.(4分)下图是制取气体的一些仪器,请回答以下问题:

(1)图中所示的D和F的仪器名称分别是___________________、_________________
(2请你用图中所示的仪器,组装一套实验室既能制取二氧化碳,也能制取氧气的装置
(包括发生装置和收集装置,请填写仪器序号)__________________________________
(3泻出此装置制取二氧化碳或氧气的化学方程式:_____________________________
24.(4分)小峰的衣服上沾上油污,打算洗干净。小雨说用水洗,小云说用汽油洗,而小雪
说用洗涤剂洗。小峰不知听谁的好,请你根据所学的化学知识帮小峰判断谁说的对,并说出其
中的道理。
23.(2分)小红在做分组实验时不小心将稀硫酸滴到了裤子上,当时没有察觉。过了几天,
小红发现裤子上出现了几个漏洞,请你结合自已学的知识解释这是为什么?
22.(2分)气体的溶解度随温度和压强的改变而改变,生活中有很多现象与此有关。比如:
夏吞,暴雨前夕,池塘里的鱼常浮出水面吸氧气,就是因为温度高了,压强小了,导致气体溶解度减小。请你再各举出一个生活中的现象,分别说明温度和压强对气体溶解度的影响。
21. (4分)如图是A、B、C三种物质的溶解度曲线,据图回答:
(4分)如图是A、B、C三种物质的溶解度曲线,据图回答:
(1) ℃时,A、B、C三种物质的溶解度由大到小的顺序
℃时,A、B、C三种物质的溶解度由大到小的顺序
是____________:
(2) ℃时,将等质量的A、B、c三种物质分别加到100
℃时,将等质量的A、B、c三种物质分别加到100
克水中,充分搅拌后只得到一种饱和溶液,该饱和溶液中
的溶质是___________:
(3)将 ℃时A、B、C三种物质饱和溶液的温度升高到
℃时A、B、C三种物质饱和溶液的温度升高到
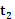 ℃时,三种溶液的溶质质量分数由大到小的顺序是_____
℃时,三种溶液的溶质质量分数由大到小的顺序是_____
_______________;
(4)若A中混有少量B时,提纯A可采用的结晶方法是_____________________________.
1 9.(2分)金属材料是现代生活和工业生产中应用极为普遍的一类物质。钛合金就是一种
重要的金属材料,具有熔点高、可塑性好、抗腐蚀性强、与人体有很好的“相容性”等优良性能。金属的下列用途:①用来做保险丝;②用来制人造骨;③用来制造船舶;④用于制造航天飞机。其中与钛合金性能符合的是____________(填序号)。
20.(6分)写出满足下列要求的化学方程式:
(1)有蓝色溶液生成的中和反应______________________________________;
(2)用稀盐酸除去铁锈的反应________________________________________;
(3)有三种氧化物生成的分解反应____________________________________;
18.把一铁片放入稀盐酸中反应,直到没有气体放出,若铁有剩余,则反应后溶液中的溶质为_________(填名称,下同),溶剂为 ! ;若铁片完全溶解,则液体中的溶质一定有________。
可能还有__________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com