
题目列表(包括答案和解析)
16.A、B两物体的质量分别为mA、mB, 且mA> mB.它们与水平面间的摩擦因数相同,两物体具有相同的动能,它们在水平面上同时开始运动,最终停止. A物体运动的时间为tA,位移为SA,B物体运动的时间为tB,位移为SB . 则有 ( )
A.SA<SB tA<tB C.SA< SB tA> tB
B.SA> SB tA> tB D.SA= SB tA=tB
15. 一质量为m的小球
用长为L的轻绳悬挂于O点 小球在水平力F的作用下,从平衡
位置甲处缓慢移动到乙处.则力F所做的功为
一质量为m的小球
用长为L的轻绳悬挂于O点 小球在水平力F的作用下,从平衡
位置甲处缓慢移动到乙处.则力F所做的功为
A. mgLcosα
B. FLsinα
C.mgL(1-cos α)
D.FLtanα
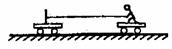
14.质量为m1、m2的两部小车,静止在光滑的水平面上,质量为m的人站在m1上用恒力F拉绳子,经过一段时间后,两小车的速度大小分别为v1和v2,位移分别为s1和s2,如图所示. 则这段时间内此人所做的功的大小等于( )
 A.
A. 
B. 
C.

D. 
13.已知:①1 mol H2分子中化学键断裂时需要吸收436kJ的能量
②1 mol Cl2分子中化学键断裂时需要吸收243kJ的能量
③由H原子和Cl原子形成1 mol HCl分子时释放431kJ的能量
下列叙述正确的是
A.氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)=2HCl(g)
B.氢气和氯气反应生成2 mol氯化氢气体,反应的△H=183kJ/mol
C.氢气和氯气反应生成2 mol氯化氢气体,反应的△H=-183kJ/mol
D.氢气和氯气反应生成1 mol氯化氢气体,反应的△H=-183kJ/mol
12.若溶液中由水电离产生的c(OH-)=1×10-12mol/L ,满足此条件的溶液中可能大量共存的离子组是
A.K+、Na+、Cl-、AlO2- B.K+、Na+、Cl-、HCO3-
C.Al3+、Na+、NO3-、I- D.K+、NH4+、SO42-、CO32-
11.下列方程式正确的是
A. 碳酸钠溶液呈碱性:CO32- + H2O  H2CO3 + 2OH-
H2CO3 + 2OH-
B.碳酸氢钠的电离: HCO3- + H2O  CO32-+ H3O+
CO32-+ H3O+
C. 泡沫灭火器原理:3CO32- + 2Al3+ + 3H2O = 2Al(OH)3 ↓+ 3CO2↑
D.大理石与醋酸溶液反应:CaCO3 + 2H+ = Ca2+ + CO2↑+ H2O
10. 在一固定容积的密闭容器中充入2 mol A和2 mol B,发生反应 2 A(g ) +
B(g)  x C(g ),达平衡后,C的体积分数为w,若维持容器体积和温度不变,按0.6 mol A、 1.3 mol B和1.4 mol C为起始物质,达到平衡后,C的体积分数也为w,则x 值为
x C(g ),达平衡后,C的体积分数为w,若维持容器体积和温度不变,按0.6 mol A、 1.3 mol B和1.4 mol C为起始物质,达到平衡后,C的体积分数也为w,则x 值为
A.1 B.2 C.2或3 D.4
9.在一定条件下,将1molCO和1molH2O(g)混合后,发生如下反应:
CO(g)+H2O(g)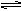 CO2(g)+H2(g)。反应达到平衡时,测得CO的转化率为21.75%,则平衡时混合气体密度为相同条件下H2密度的
CO2(g)+H2(g)。反应达到平衡时,测得CO的转化率为21.75%,则平衡时混合气体密度为相同条件下H2密度的
A.11.5倍 B.15.75倍 C.30.67倍 D.46倍
8.下列叙述正确的是
A. 同一主族的元素,原子半径越大,其单质的熔点一定越高
B. 同一周期元素的原子,半径越小越容易失去电子
C. 同一主族的元素的氢化物,相对分子质量越大,它的沸点一定越高
D. 稀有气体元素的原子序数越大,其单质的沸点一定越高
7. .NA代表阿伏加德罗常数,下列说法正确的是
A.0.5 mol Al与足量盐酸反应转移电子数为1 NA
B.标准状况下,11.2 L SO3所含的分子数为0.5 NA
C. 0.5 mol CH4所含的电子数为1 NA
D.46 g NO2和N2O4的混合物含有的分子数为1 NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com