
题目列表(包括答案和解析)
4. 下图为电子显微镜视野中观察到某细胞的一部分。下列有关该细胞的叙述中,不正确的是
下图为电子显微镜视野中观察到某细胞的一部分。下列有关该细胞的叙述中,不正确的是
A.此细胞是真核细胞不可能是原核细胞
B.此细胞是动物细胞不可能是植物细胞
C.结构2不含磷脂,其倍增发生在间期
D.结构1、3、5可发生碱基互补配对
3.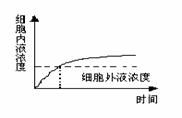 右图表示某物质进出细胞后细胞内液和细胞外液浓度随时间变化的曲线,下列说法正确的是
右图表示某物质进出细胞后细胞内液和细胞外液浓度随时间变化的曲线,下列说法正确的是
A.此物质进出细胞的方式是自由扩散
B.此细胞刚开始时细胞内液浓度大于细胞外液浓度
C.此物质进出细胞的方式是主动运输
D.此物质进出细胞时不需要消耗能量
2.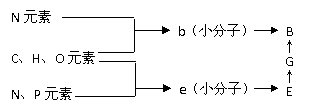 下列是人体细胞中两种重要有机物B、E的元素组成及相互关系图。关于此图的叙述正确的是:
下列是人体细胞中两种重要有机物B、E的元素组成及相互关系图。关于此图的叙述正确的是:
①E→G发生的主要场所是细胞核
②G→B发生的场所是细胞质
③B具有多种重要功能是由于b的种类、数目、排列次序以及B的空间结构不同
④B具有多种重要功能根本原因是因为E的排列次序不同
⑤E在氯化钠中的溶解度是随着氯化钠浓度的变化而变化的
A.①② B.①②③⑤ C.①②④⑤ D.①②③④⑤
1.生命活动离不开细胞,对此理解不正确的是
A.没有细胞结构的病毒需要寄生在活细胞内才能繁殖
B.单细胞生物体具有生命的基本特征--新陈代谢、应激性、繁殖……
C.多细胞生物体的生命活动由不同的细胞密切合作完成
D.细胞是一切生物体结构和功能的基本单位
33. (18分)谷氨酸是生物体内一种重要的有机小分子,谷氨酸钠是它的钠盐,是味精等调味品的主要成分。目前利用微生物发酵生产的氨基酸中,谷氨酸是产量最大的种类之一。
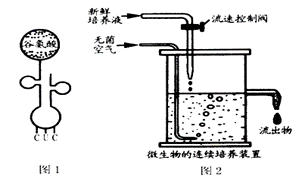
(1)谷氨酸的R基为-CH2-CH2-COOH,其结构式为 。
(2)如果在蛋白质合成过程中,携带谷氨酸的转移RNA如图1所示,可知谷氨酸的密码子为 。
(3)我国微生物发酵工程生产谷氨酸常用的菌种有谷氨酸棒状杆菌和黄色短杆菌,下列生物中与这些菌种在结构上存在明显区别的是 。
A.噬菌体 B.人类免疫缺陷病毒(HIV) C. 禽流感病毒
D.肺炎双球菌 E.酵母菌 F.硝化细菌 G.乳酸菌
(4)谷氨酸发酵的培养基成分,主要有葡萄糖.氨水.磷酸盐.生物素等,发酵装置如图2所示。可以判断谷氨酸棒状杆菌的新陈代谢类型是 。某厂用谷氨酸棒状杆菌发酵生产谷氨酸,结果代谢产物中出现了大量的乳酸,从发酵条件看,其原因很可能是 。
(5)谷氨酸发酵生产过程中,需要添加氨水,它不仅是细菌生长所需的 ,而且还有调节培养液PH的作用,所以应该分次加入。
(6)某厂的发酵液曾不慎被噬菌体污染,菌群死亡殆尽,但人们却侥幸从中获得了少数可抵抗噬菌体的新菌种,细菌这种新性状的产生来自于 。
(7)图2所示连续培养的方法,以一定的速度不断添加新的培养基,同时又以同样的速度放出旧的培养液,此工艺流程可以大大提高生产效率,试阐述其原因
。(至少说出两种)
31. (10分)两场筹备了
10年的“太空结合”首次
在神 舟四号飞船上举
行了, “新人”之一是小
白鼠B淋巴细胞和骨髓瘤
细胞,新人在 “产房”
--电融合仪内孕育新生
命。160min后,中国首批
“太空娃娃”终于顺利诞
生。“太空娃娃”诞生和地
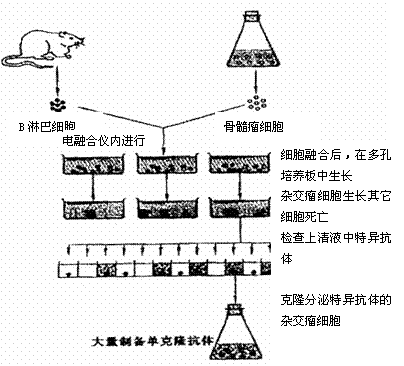
面实验如图所示。请回答:
(1)淋巴细胞的细胞膜是由______________(化学成分)组成的。小白鼠B淋巴细胞和骨髓瘤细胞能融合在一起,体现了细胞膜具有_____________的特点。
(2)B淋巴细胞和T淋巴细胞都是由造血干细胞形成的。这种相同细胞的后代,在形态、结构和生理功能上产生稳定差异的过程,叫做 。
(3)鼠的淋巴细胞和骨髓瘤细胞融合后,在培养时通过_____________分裂方式大量繁殖。
(4)融合的细胞具有两种细胞的特性,即_____________________________________。
32 I(14分)抗生素作为治疗细菌感染的药物,其高效性和巨大的经济价值使抗生素工业经久不衰。其中青霉素的发现和应用具有划时代的意义。·
(1)青霉菌发酵产生青霉素。青霉菌的新陈代谢类型是 ,青霉素是青霉菌 的 代谢产物。
(2)在生产和科研中,常选用处于 期的青霉菌作为菌种或研究材料.
II某中学生物兴趣小组选择“探究青霉素对细菌生长的影响”作为研究性课题,若你是其中一员,请你根据提供的实验材料完成实验方案的设计,并预测可能的实验结果,作出相应的结论。
(1)实验材料:经过灭菌的培养皿若干,适合细菌生长的固体培养基、大肠杆菌咱,接种环、无菌青霉素溶液、无菌蒸馏水、洒精灯、恒温培养箱等。
(2)实验方案:
①取培养皿两个,编号为A、B;
②将培养基加热融化,在A、B培养皿中分别倒入等量的培养基,在A中加入 在B中加入___________ ;
③待培养基冷却凝固后,在酒精灯火焰上方向两个培养皿中分别接种等量大肠杆菌菌种
④放在恒温培养箱中培养1d-2d;⑤观察并记录细菌生长情况
(3)可能的实验结果及相应结论:6分
_______________________________________________________________________;
_______________________________________________________________________;
_______________________________________________________________________;
(4)最可能的结果是______________________________________________________;
30.(15分)(1) 配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏低的原因是__________
A. 称量时NaOH已经潮解
B.向容量瓶中转移溶液时,容量瓶事先用蒸馏水洗涤过
C.定容时俯视容量瓶的标线
D.摇匀后发现液面低于标线,滴加蒸馏水至标线再摇匀
(2) 实验室用50mL 1.0mol/L盐酸跟50mL 1.1mol/L
氢氧化钠溶液在下图装置中进行中和反应,并通过测定
反应过程中所放出的热量来计算中和热。试回答下列问题:
①大小烧杯间填满泡沫塑料的作用是____________________________
②_____(填“能”或“不能”)将环形玻璃棒改为环形金属(如铜)棒
③大烧杯上如不盖硬纸板,对求得的中和热数值的影响是___________(填“偏高”“偏低”或“无影响”)
④如果改用60mL 1.0mol/L盐酸跟50mL 1.1mol/L氢氧化钠溶液进行反应,则与上述实验相比,所放热量______________(填“增加”“减少”或“不变”)所求中和热的数值_______________(填“增加”“减少”或“不变”)
29.(15分)黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)冶炼铜的反应为
8CuFeS2+21O2=8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是 (填元素符号)。
( 2 )上述冶炼过程产生大量SO2。下列处理方案中合理的是 (填代号)。
a.高空排放
b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3
d.用浓硫酸吸收
( 3 )过二硫酸钾(K2S2O8)具有强氧化性可将I-氧化为I2:S2O82-+2I-=2SO42-+I2
通过改变反应途径,Fe3+、Fe2+ 均可催化上述反应。试用离子方程式表示Fe3+对上述反应催化的过程。 、 。(不必配平)
( 4 )利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO 、SiO2、Al2O3)可制备Fe2O3。方法为① 用稀盐酸浸取炉渣,过滤。
② 滤液先氧化,再加人过量NaOH 溶液过滤,将沉淀洗涤、干澡、煅烧得Fe2O3。据以上信息回答下列问题:
a.除去Al3+的离子方程式是 。
b.选用提供的试剂设计实验验证炉渣中含有Fe2O3。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水
所选试剂为 。
证明炉渣中含有FeO 的实验现象为 。
28.(15分)
X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W三种元素的原子最外层电子数之和为17。
请填空:
(1)Y、Z和W三种元素是否位于同一周期(填“是”或“否”): ,理由是 ;
(2)Y是 ,Z是 ,W是 ;
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8∶2∶4∶1。写出该化合物的名称及化学式 。
27.(15分)Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物,其固态属于______________晶体,俗名叫_______________;
(2)R的氢化物分子的空间构型是________________,属于________分子(填“极性”或“非极性”) ;它与X形成的化合物可作为一种重要的陶瓷材料,其化学式是______________;
(3)X的常见氢化物的空间构型是________________;它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是__________________;
(4)Q分别与Y、Z形成的共价化合物的化学式是_____________ 和________________;Q与Y形成的分子的电子式是_____________________,属于________分子(填“极性”或“非极性”)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com