
题目列表(包括答案和解析)
36. ( 18 分)随着越来越高的摩天大楼在各地的落成,至今普遍使用的钢索悬挂式电梯已经渐渐地不适用了.这是因为钢索的长度随着楼层的增高而相应增加,这样这些钢索会由于承受不了自身的重量,还没有挂电梯就会被扯断.为此,科学技术人员正在研究用磁动力来解决这个问题.如图所示就是一种磁动力电梯的模拟机,即在竖直平面上有两根很长的平行竖直轨道,轨道间有垂直轨道平面的匀强磁场B1和B2,且B1和B2的方向相反,大小相等,即B1= B2=1T,两磁场始终竖直向上作匀速运动.电梯桥厢固定在如图所示的一个用超导材料制成的金属框abcd内(电梯桥厢在图中未画出),并且与之绝缘.电梯载人时的总质量为5×103kg,所受阻力f=500N,金属框垂直轨道的边长Lcd
=2m,两磁场的宽度均与金属框的边长Lac相同,金属框整个回路的电阻R=9.5×10-4Ω,假如设计要求电梯以v1=10m/s的速度向上匀速运动,取g=10m/s2,那么,
( 18 分)随着越来越高的摩天大楼在各地的落成,至今普遍使用的钢索悬挂式电梯已经渐渐地不适用了.这是因为钢索的长度随着楼层的增高而相应增加,这样这些钢索会由于承受不了自身的重量,还没有挂电梯就会被扯断.为此,科学技术人员正在研究用磁动力来解决这个问题.如图所示就是一种磁动力电梯的模拟机,即在竖直平面上有两根很长的平行竖直轨道,轨道间有垂直轨道平面的匀强磁场B1和B2,且B1和B2的方向相反,大小相等,即B1= B2=1T,两磁场始终竖直向上作匀速运动.电梯桥厢固定在如图所示的一个用超导材料制成的金属框abcd内(电梯桥厢在图中未画出),并且与之绝缘.电梯载人时的总质量为5×103kg,所受阻力f=500N,金属框垂直轨道的边长Lcd
=2m,两磁场的宽度均与金属框的边长Lac相同,金属框整个回路的电阻R=9.5×10-4Ω,假如设计要求电梯以v1=10m/s的速度向上匀速运动,取g=10m/s2,那么,
(1)磁场向上运动速度v0应该为多大?
(2)在电梯向上作匀速运动时,为维持它的运动,外界必须提供能量,那么这些能量是由谁提供的?此时系统的效率为多少?
35. (18分)如图所示,质量M=0.45kg的带有小孔的塑料块沿斜面滑到最高点C时速度恰为零,此时与从A点水平射出的弹丸相碰,弹丸沿着斜面方向进入塑料块中,并立即与塑料块有相同的速度.已知A点和C点距地面的高度分别为:H=1.95m,h=0.15m,弹丸的质量m=0.050kg,水平初速度v0=8m/s,取g=10m/s2.求:
(1)斜面与水平地面的夹角θ.(可用反三角函数表示)
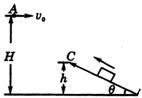 (2)若在斜面下端与地面交接处设一个垂直于斜面的弹性挡板,塑料块与它相碰后的速率等于碰前的速率,要使塑料块能够反弹回到C点,斜面与塑料块间的动摩擦因数可为多少?
(2)若在斜面下端与地面交接处设一个垂直于斜面的弹性挡板,塑料块与它相碰后的速率等于碰前的速率,要使塑料块能够反弹回到C点,斜面与塑料块间的动摩擦因数可为多少?
34.(1)(12分)某实验小组利用如图甲所示的气垫导轨实验装置来探究当合外力一定时,物体运动的加速度与其质量之间的关系.

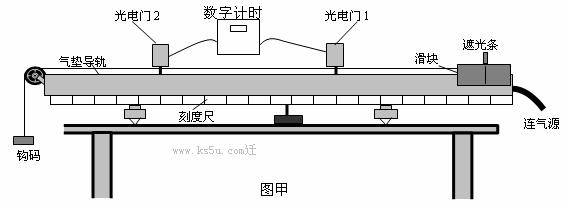
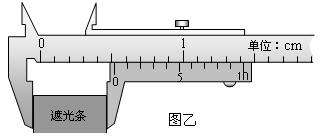
1由图甲中刻度尺读出两个光电门中心之间的距离s=24cm,由图乙中游标卡尺测得遮光条的宽度d= cm.该实验小组在做实验时,将滑块从图甲所示位置由静止释放,由数字计时器可以读出遮光条通过光电门1的时间Δt1,遮光条通过光电门2的时间Δt2,则滑块经过光电门1时的瞬时速度的表达式v1= ,滑块经过光电门2时的瞬时速度的表达式v2 = ,则滑块的加速度的表达式a= .(以上表达式均用字母表示)

23现需通过图像进一步验证你的结论,请利用表格数据,在坐标系中描点作出相应图像.
(2)(7分)多用电表是一种重要的电路检测工具,其用途很广,以下是某研究性学习小组利用一个量程合适的电压表测量一个多用电表欧姆档的内部电源的电动势的实验,假设你组员,请你按要求完成以下任务:
1用多用电表测量电压表的阻值。为此,应先对多用电表进行机械调零,具体操作是 ;然后把多用电表的选择开关旋到欧姆档,选择合适的倍率档后进行欧姆调零;最后进行电压表的电阻测量。以下是实验用的电压表和待测多用电表,请你把实验电路连接好.

2小组其他成员从多用表刻度盘上读出电阻刻度中间数值为30,电压表的读数为U,欧姆表指针所指的刻度为n,此时欧姆档的选择开关拨至倍率“×1K”档,并且在实验过程中,一切操作都是正确的,请你导出欧姆表电池的电动势表达式: .(不要求写出推导过程)

33. (16分)工业上以乙烯为原料经不同途径,可合成化学式均为C3H6O3的化合物。请回答相关的问题:
(16分)工业上以乙烯为原料经不同途径,可合成化学式均为C3H6O3的化合物。请回答相关的问题:
途径一:
 已知:
已知: (1)写出下列物质的结构简式:
A:
; C:
。
(2)指出反应②的反应类型
。
(3)写出反应③的化学方程式
。
(4)反应④的目的
。
途径二:
(1)写出下列物质的结构简式:
A:
; C:
。
(2)指出反应②的反应类型
。
(3)写出反应③的化学方程式
。
(4)反应④的目的
。
途径二:
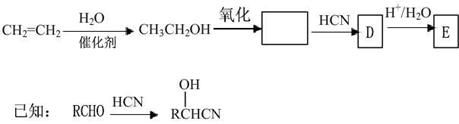
(1)请在合成路线框图中填入相应有机物的结构筒式。
(2)E在浓硫酸存在的条件下加热,可生成六原子环状化合物F(C6H8O4),请写出反应的化学方程式是:
___________________________________________________________________________
32.(16分)电子产品更新换代速度快,电路板(主要含Cu 和少量的Zn、Fe)回收利用是富有价值的研究课题,以下是某个从电路板中回收金属铜的生产流程。回答下列问题:
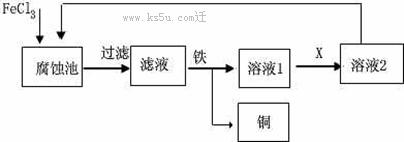
(1)写出腐蚀池中铜与氯化铁反应的离子方程式
(2)在溶液1中加入适量稀盐酸,然后加入试剂X,若从“绿色化学”角度考虑,X试剂应选 ;写出反应的离子方程式
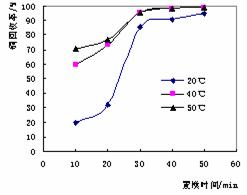 (3)随着印刷工业和电子工业的发展,三氯化铁腐蚀液的用量不断增加,废腐蚀液量也随之增加,而废液一般含铜量高达0.09kg/L以上,为了提高铜的回收率,取溶液1做了如下实验(第二次浸取):
(3)随着印刷工业和电子工业的发展,三氯化铁腐蚀液的用量不断增加,废腐蚀液量也随之增加,而废液一般含铜量高达0.09kg/L以上,为了提高铜的回收率,取溶液1做了如下实验(第二次浸取):
实验:分别取X mL的溶液1,加入15g的铁,在温度为10℃-50℃下浸取,待置换完全后取出铁片,将所有置换的铜过滤,洗净,烘干称重所得数据如图所示。
则从实验中可得出的结论是
(4) 除上述回收方法外,还可以用以下方法:在滤液中加入适量的盐酸调节溶液的 pH = 1 ,用铜和石墨作电极进行电解。当观察到阴极上有少量气泡产生时,即停止电解,这时要回收的 Cu 已全部析出。请写出铜电极上所发生的电极反应(若有多个电极反应,请按照反应发生的先后顺序全部写出)__________________________________________________________________________________________________________________________________________________________________________。
31. (16分)二氧化硫是常用的化工原料,但也是大气的主要污染物。请回答相关问题:
(1)有人提出如下方案防治酸雨:常温下将含有SO2的废气通入FeCl3 溶液中,然后在所得溶液中提取晶体而实现SO2的回收利用。
①参加反应的SO2和Fe3+的物质的量之比是 。
②若要从所得溶液中提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有 (填序号)。
A.蒸发皿 B.石棉网 C.漏斗 D.烧杯 E.玻璃棒 F. 坩埚
 (2)将SO2和O2的混合气体通入容积为2.0L的密闭容器内,在一定温度和催化剂存在的条件下,反应达平衡时测得SO2、O2和SO3物质的量分别为2.0mol、1.0mol和3.0mol。 则该条件下,试计算2SO2+O2 2SO3 反应的平衡常数为 及SO2的转化率(写出计算过程)。
(2)将SO2和O2的混合气体通入容积为2.0L的密闭容器内,在一定温度和催化剂存在的条件下,反应达平衡时测得SO2、O2和SO3物质的量分别为2.0mol、1.0mol和3.0mol。 则该条件下,试计算2SO2+O2 2SO3 反应的平衡常数为 及SO2的转化率(写出计算过程)。
(3)若用过量的铁粉与浓硫酸在加热条件下制SO2,发现生成的气体冷却后体积比理论计算所得的SO2的体积要多。请你对气体的组成提出合理猜想,并说明验证的方法。
①猜想:_____________________________________________;
②验证方法 :_____________________________________________________________
______________________________________________________________________________________

30. (16分)已知FeC2O4·2H2O 在受热先失去结晶水,继续加热FeC2O4分解为气体和一种铁的氧化物,某实验小组利用如下装置(部分固定和加热装置略)探究草酸钙分解气体部分产物及固体产物的实验式。
(16分)已知FeC2O4·2H2O 在受热先失去结晶水,继续加热FeC2O4分解为气体和一种铁的氧化物,某实验小组利用如下装置(部分固定和加热装置略)探究草酸钙分解气体部分产物及固体产物的实验式。
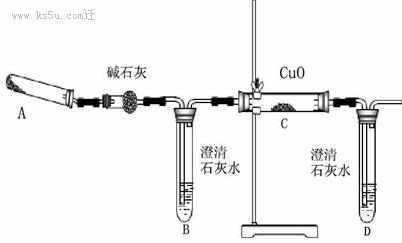
(1)请指出该装置一处缺陷:
(2)完善并连好装置后,需进行的实验操作有:①__________________________;②加药品和试剂;③给A、C装置加热……
(3)若分解的气体中含有CO,则观察到的现象是
_______________________________________________________________________________________。
(4)甲同学欲要检测得到的固体是否含有+3价的铁元素,他应该选择的试剂是 (填序号)
A.KSCN溶液 B.稀硝酸 C.稀硫酸 D.铁粉
(5)若实验前将3.6g草酸亚铁晶体(FeC2 O4·2H2O)加入大试管加热分解,充分反应后得到1.44g黑色固体,则该铁的氧化物是 。(填化学式)
29、(14分)目前,H1N1流感传染非常快,H1N1流感疫苗是预防甲流的最好方法,而H1N1甲流疫苗的研制过程要经历三个阶段:第一阶段减毒处理H1N1流感病毒;第二阶段接种经减毒处理的H1N1流感病毒的蛋白质;第三阶段运用生物技术成功生产DNA疫苗,请运用生物学知识回答:
(1)H1N1流感病毒RNA在 酶作用下合成DNA。
(2)合成的DNA运用PCR扩增技术获得更多的DNA,请简述PCR的过程。(3分)
(3)DNA在 酶作用下获得病毒基因,此酶的作用是
,并在 酶作用下与质粒结合形成重组质粒(即DNA疫苗)。注入人体细胞后,即可产生具有免疫性质的蛋白质,该步骤相当于基因工程中的 步骤。
(4)DNA疫苗提高人体免疫力过程中包括哪几阶段?(3分)
(5)DNA疫苗是否产生对人体不利的影响?为什么?(2分)
28、(21分)请回答下面人体生命活动调节与生态有关有关的Ⅰ、Ⅱ小题:
Ⅰ兴奋剂是国际体育界对所有违禁药物的总称,包含种类很多,常用兴奋剂有雄激素及其衍生物、促红细胞生成素等。请根据下图回答问题:(15分)

(+)↓
(+)↓ (一)
(+)↓
(1)由上图可知,促红细胞生成素(EPO)能够增强骨髓造血干细胞的活动,从而增加血液中 细胞的数量,促进机体细胞进行 呼吸提供能量。运动员长期注射EPO会使机体血液中血浆比例相对 (填“增大”或“减小”),从而影响内环境的稳态。
(2) 雄激素及其衍生物类兴奋剂属于 类化合物,男性运动员长期服用此类兴奋剂会使血液中雄激素含量过高,从而 下丘脑和垂体的活动,导致相关激素(如促性腺激素等)的分泌量 ,进而引起自身雄激素分泌异常,严重时甚至会导致性腺萎缩。
(3)利用健康老鼠80只(雌雄各半), 低浓度、中浓度、高浓度的雄激素溶液和必备的材料进行实验(实验条件满足要求),探究雄性激素作用及不同浓度(低、中、高)的雄性激素溶液对老鼠性腺大小的影响,并预测结果。
实验步骤:(3分)
 ________________________________________________________________________________________________________________。
________________________________________________________________________________________________________________。
实验结果预测:(6分)
__________________________________________________________________________________________________________________________________________________________________________________________________。
II下图为现代农业生态系统的结构模式图(6分)。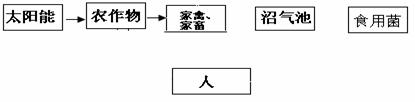
(1) 用箭头完成该生态系统能量流动和利用图解(各生物呼吸和分解者耗能可不标明)(2分)
(2) 该生态系统的能量能更多地被人类利用是因为
(2分)。
(3) 该生态系统的结构充分体现了生态工程基本原理的 原理和 和工程学原理。
27、(14分)用纯种有色饱满籽粒的玉米与无色皱缩籽粒玉米杂交。(实验条件满足要求),F1全为有色饱满籽粒,F1自交后,F2出现:有色饱满73%,有色皱缩2%,无色饱满2%,无色皱缩23%。请回答:
(1)上述一对相对性状的结果符合 定律。
(2)上述两对相对性状的结果是否符合基因自由组合定律?为什么?(3分)
(3)请设计一个实验方案,验证这两对相对性状的遗传是否符合基因自由组合定律。(实验条件满足要求)(10分)
实验实施步骤:
方案:
结果与结论:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com