
题目列表(包括答案和解析)
8.(08江苏南京)在反应2A+5B=2C+4D中,C、D的相对分子质量之比为9:22。若2.6gA与B完全反应后,生成8.8 gD。则在此反应中,B与D的质量比为 ( )
A.4:9 B.8:11 C.10:11 D.31:44
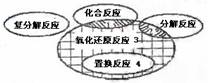
7.(08山东青岛)在化学反应前后,物质所含元素化合价发生变化的反应是氧化还原反应,它与化学反应基本类型间的关系如图所示,下列示例中错误的是 ( )
 A.阴影1:C+O2 点燃 CO2
A.阴影1:C+O2 点燃 CO2
B.阴影2:2H2O 通电 2H2↑+O2↑
C.阴影3:Mg(OH)2+2HCl=MgCl2+2H2O
D.阴影4:Fe+CuSO4=FeSO4+Cu
6.(08山东青岛)2008年奥运会“祥云”火炬中燃料燃烧后不会对环境造成污染,体现了“绿色奥运”的理念。反应的化学方程式为CxH8+5O2 点燃 3CO2+4H2O,则x的数值是 ( )
A. 1 B.2 C.3 D.4
5.(08湖北咸宁)下列四个反应生成物都是C,如果C化学式为A2B5,则该反应化学方程式为 ( )
A.2AB2 + B2 == 2C B.3AB2 + B2 == 2C
C.4AB2 + B2 == 2C D.AB2 + 4B2 == 2C
4.(08哈尔滨)下列应用的原理用化学方程式表示正确的是 ( )
A.用适量的稀盐酸除铁锈 Fe2O3 + 6HCl =2FeCl2 + 3H2O
B.用一氧化碳作燃料 C0+02 点燃 C02
C.高温煅烧石灰石制取生石灰 CaC03 高温 CaO+C02 ↑
D.用红磷燃烧测定空气中氧气含量 S + O2 点燃 SO2
3. (08黑龙江)CO2是产生温室效应的罪魁祸首,只用C、CO、CuO、CaCO3、稀盐酸五种物质,进行单一(一种反应物)或两两反应,可写出产生CO2的化学方程式有: ( )
A.2个 B.3个 C.4个 D.5个
2. (08福建福州)发射“嫦蛾一号”的火箭用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作常规推进剂,其完全反应的化学方程式:C2H8N2+2 N2O4=3X+2CO2+4H2O,则X的化学式为 ( )
A.N2 B.H2 C.O2 D.CO
1. (08福建福州)钛台金是2l世纪的重要材料,工业上制取钛的一个反应是:TiCl4+2Mg Ti +2MgCl2该反应类型属于
( )
Ti +2MgCl2该反应类型属于
( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
1、下列操作中不应该接触的是( )。 A、向试管中加入液体试剂时,试剂瓶口与试管 B、滴加试剂时,滴管与试管内壁 C、过滤时漏斗管口与烧杯内壁 D、过滤时盛待过滤液体的烧杯口与玻璃棒 [解析]本题考查学生化学实验基本操作的掌握程度,涉及液体药品的取用、过滤的基本操作。向试管内倾到液体时,试管应斜持,瓶口挨管口,防止液体洒落。滴管用于取用少量液体,滴加液体时,应把它悬空放在容器上方,不要接触容器内壁,以免玷污滴管或造成试剂的污染。过滤的操作要求注意“一贴、两低、三靠”。即滤纸紧贴漏斗内壁;滤纸边缘低于漏斗边缘,滤液要低于滤纸;倾到液体的烧杯靠玻璃棒靠三层滤纸处,漏斗下端管口靠烧杯内壁。故答案选B 2、某学生使用带游码的托盘天平称量食盐放在右托盘,砝码放在左托盘,他称得食盐重10.6 g(1 g以下用游码),则食盐的实际质量为( )。 A、10 g B、11.2 g C、9.4 g D、10.6 g [解析]了解托盘天平的原理是正确称量的关键,天平的正确操作为“左物右码”,拨动游码使天平平衡,实际上相当于右托盘增加砝码,即左盘物质质量=右盘物质质量+游码所对的刻度值。根据这一思路,就可计算出食盐的实际质量:10 g=食盐质量+0.6 g ,食盐质量=9.4 g 答案选C [例题精讲] 3、粗盐中混有Mg2+、Ca2+、SO42-和泥沙,为了除去杂质,在实验室中可将粗盐溶于 水,然后进行下列操作:①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加适量Na2CO3 溶液 ⑤加过量BaCl2溶液。其正确的操作顺序是( )。 A、⑤④②①③ B、①②③④⑤ C、⑤④③②① D、①⑤④②③ [解析]需要除去Mg2+、Ca2+、SO42-和泥沙,选择的除杂试剂为Mg2+→NaOH、Ca2+→Na2CO3、 SO42-→BaCl2,Na2CO3同时还能除去溶液中过量的BaCl2,而HCl用于除去过量的Na2CO3 和NaOH,但在加HCl之前,应先把沉淀过滤。因为生成的CaCO3、BaCO3沉淀能溶于 HCl,因此可判断其有两个关键的顺序①加HCl及过滤应放在实验末尾,且过滤的操作在 加HCL之前;②Na2CO3溶液应在BaCl2溶液之后加,以便同时除去Ba2+。所以正确的顺 序为⑤④②①③或⑤②④①③。 [错解]B 先过滤的目的,是要先除去泥沙,但生成沉淀后,加HCl之前仍要再过滤一次, 而B选项没有,完全可以一次性把沉淀及泥沙过滤。另一处错误是BaCl2在Na2CO3之后 加,溶液中多余的Ba2+没有除去,成为新的杂质。故答案为A 4、在室温下的饱和食盐水中放了一个塑料小球,(1)现加入少量食盐晶体,充分搅拌和静置后,在温度不变的情况下,小球在液面沉浮情况有何变化,并简述原因__________;(2)若要在不用外力的情况下使小球略上浮,你准备采取的具体方法是__________。 [解析]此题的第(2)此题为开放性试题,它需要采用一些方法使溶液的密度增大而使小球上浮,有一定的思维深度和广度,给学生以施展才能的舞台,使学生将化学方法和力学原理相结合,从多角度思考,多方位实施,很有效地达到考查学科科学素质的目的,对今后初中教学向综合课过渡,加强学科间的综合素质的考查,奠定了基础。 答案:(1)沉浮情况不变,因为将氯化钠晶体投入氯化钠饱和溶液中,不会继续溶解,溶液密度不变,小球排开液体的体积(质量)不变。(2)可能的答案有:A.可加入硝酸钾等(不反应的其他可溶性)晶体;B.可加入密度比饱和食盐水大的其他可与食盐水混溶的溶液;C.可加入硝酸银等(反应但使溶液质量和密度上升)晶体;D.可升高温度后加入氯化钠晶体,使溶液密度上升。 5、著名化学家罗博特。波义尔在一次实验中,不小心将盐酸溅到紫罗兰花瓣上,过一会儿,发现紫色花瓣出现红点点。他对这一意外的发现作出各种假设,经过多次实验验证,探究普遍规律,终于获得成功。对紫罗兰花瓣遇盐酸变红现象,你有哪些假设?写出你的各种假设以及验证假设的实验方案。 [解析]试题以指示剂的发现为素材,要求学生根据科学探究过程,提出设想并制定方案。解题的关键在于作出合理的假设。由于素材仅涉及盐酸和紫罗兰花瓣,结合中学实际,学生应敏锐地感知,试题旨在考查酸的性质(指示剂遇酸变色)。由于实验条件没有限制,思维角度和试题答案具有开放性的特点。根据已有的知识,本题可从宏观和微观的角度对现象作出假设:1)宏观的角度,从物质的属类出发,可考虑其它酸是否具有同样的现象;或者考虑中性、碱性溶液是否存在该现象;2)微观的角度,可从盐酸所含的微粒出发,探究变色是由H+、Cl-、还是H2O引起的。对应的实验就可以依据假设来进行设计和展开。 答案为:其它酸能使紫罗兰花瓣变色吗? 将稀硫酸、稀硝酸等滴到花瓣上,观察现象;盐酸能使其它种类的花瓣变色吗?将盐酸分别滴到其它种类的花瓣上,观察现象; 碱液也能使紫罗兰花瓣变色吗? 将NaOH、Ba(OH)2溶液滴到花瓣上,观察现象;是溶液中的Cl-使花瓣变红吗? 将NaCl、KCl溶液滴到花瓣上、观察现象。
本资料由《七彩教育网》 提供!
17、甲、乙、丙是初中化学中常见的物质,其转化关系如下图所示:

(1)若甲、乙组成元素相同,甲、乙、丙中有一种物质为水,则甲为(填化学式) ;实验室制丙的化学方程式为 (写出一种)。
(2)若甲、乙、丙都含有三种元素,甲、乙、丙的相对分子质量依次增大,其中一种物质广泛用于玻璃、造纸、纺织和洗涤剂的生产。由甲到乙反应的化学方程式为 。乙也可以转化成甲,其反应方程式为 。
(3)若甲、乙、丙都含有三种元素,其中两种元素的质量比均为1:2。图示反应中,一个有难溶物生成,另一个有气体生成,第三个有难溶物和水生成。则生成气体可能为(填化学式) ;丙为(填化学式) 。
本资料由《七彩教育网》 提供!
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com